Благодаря своим многочисленным преимуществам данный металл получил широкое распространение. На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
Для этого понадобится:
Гальваническое меднение в домашних условиях
Медный купорос
Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора в соляную кислоту. После приготовления раствора медного купороса его следует тщательно размешать, чтобы не было частиц. Далее нужно соляную кислоту тонкой струйкой добавить в этот раствор. Не следует забывать про технику безопасности и использовать перчатки и защитные очки. После того, как вы добавили в раствор соляную кислоту, его следует тщательно перемешать.
Итак, раствор готов и можно приступать к меднению в домашних условиях. Для этого нужно взять металлическую деталь, на которую вы собрались наносить слой меди и подготовить ее к работе. Подготовка включает в себя ее обработку наждачной бумагой. Данная процедура позволяет не только зачистить металлическую поверхность, но и обезжирить ее. Такая же процедура будет актуальна и для детали из латуни или свинца. После этого, покрытие нужно тщательно промыть в растворе кальцинированной соды. Это позволит более тщательно обезжирить материал.

Кальцинированная соды для обезжиривания материала
Далее поверхность нужно погрузить в раствор медного купороса и соляной кислоты. Следует обратить внимание на то, что первый слой меди является очень тонким и слабым, поэтому его желательно снять при помощи металлической щетки. После того, как вы это сделали, поверхность стали или свинца следует повторно промыть в растворе кальцинированной соды и опять погрузить в раствор для меднения. Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
Этот способ позволяет сделать очень качественное медное покрытие, которое можно снять только наждачкой. Для улучшения медного покрытия в домашних условиях следует деталь еще раз погрузить в раствор. Указанный способ отличается своей простотой и высокой эффективностью в том числе и для изделий из свинца.
Меднением принято называть процедуру гальванического нанесения меди, толщина слоя меди в таких случаях может составлять-от 300 мкм и больше. Меднение стали это один из наиболее важных процессов в гальванике, поскольку используется, как дополнительный процесс перед нанесением других металлов для хромирования, никелирования, покрытие серебром.
Слой меди прекрасно держится на стали и способен выравнивать различные дефекты на поверхности.
Для медных покрытий характерно высокое сцепление с другими поверхностями, изделиями из свинца особенно металлическими, а также высокая электропроводность и пластичность. Нанесенное недавно покрытие имеет ярко-розовый матовый или же блестящий цвет. Под воздействием влияний атмосферы медные покрытия могут окисляться, покрываться налетом окислов с различными пятнами радужного вида.
 Как правило, гальваническое омеднение может использоваться:
Как правило, гальваническое омеднение может использоваться:
Меднение происходит вместе с нанесением других гальванических покрытий
Первый способ предполагает обработку металлического изделия наждачной бумагой, щеткой и промывки водой. После чего обезжиривания в горячем содовом растворе с повторной промывкой. Далее в стеклянную емкость опускают на медных проволочках две медные пластины –аноды. Между пластинками на проволоке подвешивают деталь, после чего пускается ток.
Второй способ актуальный для изделий из стали, алюминия и цинка.
Данная процедура актуальна для различных случаев, поскольку нанесение слоя меди может использоваться для алюминиевых столовых приборов, сувениров, подсвечников и т. д. Неповторимый эффект оказывают изделия не из металла, на которые был нанесен слой меди. Это могут быть стебли растений, листья и др. Ввиду того, что в покрываемых предметах отсутствует токопроводящий слой, вместо него используется специальный электропроводный лак, который наносят на поверхности.
В состав лака входит ряд органических растворителей, пенкообразователей и тонкодисперсионный графитовый порошок, благодаря которому создается электропроводность. Лак наносят тонким слоем на сухую поверхность, и после высыхания через час можно приступать к омеднению. При желании можно меди придавать различные цветовые оттенки, используя для этого специальные способы. Высокое качество и уникальность таких изделий вполне заслуженно приравнивается к настоящим ювелирным украшениям.
Если перед вами стоит задача омеднения каких-либо деталей в автомобиле, то оказывается это вполне возможно сделать в домашних условиях. Для этого не потребуется особых знаний и умений, да и все материалы и реагенты вполне можно найти в магазинах или своих запасах. Что же, давайте посмотрим как можно сделать омеднение.
Прежде чем рассказать о самом процессе, хотелось бы сказать пару слов о прагматичности такой операции. Многие из автолюбителей не особо знакомых с химией сейчас скажут о необходимости омеднения всего чего попадется под руку, но мы вас предостерегаем от этого! Почему!? Да потому что все металлы между собой образуют гальваническую пару. Такая гальваническая пара образуется даже при попадании воды, а если средой будет еще и кислота, то процесс пойдет в разы быстрее. Суть процесса в гальванической паре сводится к следующему. Более активный металл отдает свои электроны, а менее активный принимает. Вот так и образуется самая простая «батарейка» в которой протекает электрический ток. Давайте теперь взглянем на стандартные электродные потенциалы:
- для меди Е0(Сu2+/Cu)=0,34В;
- для железа E0(Fe2+/Fe)=-0,44В.
В итоге получается не все так гладко. Ведь в такой гальванической паре У железа электродный потенциал более активным. Опять же у меди электродный потенциал более положителен, чем у железа, поэтому она будет менее активна. В итоге электроны потекут от железа к меди, что приведет к коррозии железа.
Все это мы рассказали к тому, что бездумно покрывать медью все что вам попадется под руку на машине не рекомендуется. Ведь в этом случае вы можете значительно сократить жизненный цикл многих железных деталей (крепеж, кузовные детали).
Не зря для сохранения железа применяют цинк, там ситуация с электродными потенциалами обратная.
Однако омеднение может применяться для декоративной отделки железа, если покрытие будет находиться в сухости. Также медь может применяться в случаях, где необходимо обеспечить передачу электрического тока между контактами. Опять же надо следить за их чистотой.
Медь может применяться в условиях применения пар с незначительным трением скольжения. Все это в целом вполне жизнеспособные варианты. А значит и омеднение все же имеет шанс на его реализацию. Тогда не будем более медлить, расскажем непосредственно о процессе омеднения.
Омеднение происходит в растворе. По сути этот процесс обратный гальванической паре, то есть тому, о чем мы рассказывали в абзаце выше.
Для раствора нам понадобиться кислота, можно взять электролит используемых для аккумуляторов. Воду и медный купорос.
Для раствора берется 100 мл электролита на 20 мл воды и добавляется 20 г медного купороса. В качестве донора меди можно взять медные пластинки или обычный медный провод, предварительно очищенный от изоляции. Итак, именно в этот самый раствор и помещаем медь. При этом подключаем блок питания постоянного напряжения питания к меди (+) и к железу (-). Ток на блоке питания выставляем тот, при котором мы планируем за определенный период времени нанести определенный слой меди. Это уже задача по химии школьной программы. И получается все так…
I= (плотность меди (8920 кг/м3)*площадь детали (скажем 0,1 м3)*(требуемый слой (скажем 0,0001 м, то есть 0,1 мм))/ (электрохимический эквивалент для меди это 6,6*〖10〗^(-7)
* желаемое время, скажем 3 часа – 10800 секунд). Считаем…
I=8920*0,1*0,0001/0,0000066*10800=0,0892/0,07128=1,25 А
То есть за 3 часа при токе 1,25 А у нас будет покрытие в 0,1 мм на детали площадью 0,1 м3. Вот как-то так и считаем все аналогичные вариации.
А да, время от времени не забываем помешивать раствор, чтобы процесс шел равномерно.
После того как омеднение завершено, вытаскиваем детали из раствора и отмываем хорошо с щелочью, то есть с мылом.
Если есть каике-то заусенцы и отклонения от формы, то их вполне можно пройтись наждачной бумагой и заполировать.
Собственно вы теперь не меньше знаете, как производить омеднение поверхности. Надо сказать, что по тому же принципу производится и оцинкование и хромирование… В итоге понимая принцип происходящего процесса можно перенести процесс покрытия поверхности и на другие металлы.
Когда речь идет о гальванотехнике, сразу же на ум приходят такие технологические операции, как хромирование и цинкование металлоизделий. Но если задать вопрос, а что представляет собой гальваностегия, то ответит не каждый – проверено. Хотя ничего сверхнового данный термин не подразумевает.
Проще говоря, это методика покрытия тончайшим слоем металла любого материала, будь-то сталь, алюминий, древесина или пластик. С тем, как произвести меднение какого-либо образца в домашних условиях, мы и разберемся.
 Меднение – методика отчасти более универсальная, чем то же цинкование. Для каких целей оно проводится?
Меднение – методика отчасти более универсальная, чем то же цинкование. Для каких целей оно проводится?
Вряд ли читателя заинтересуют такие нюансы, как классификация меди (рафинированная, бескислородная, общего применения), различные варианты растворов, использующихся при меднении, характеристики материалов и подобные вещи. Далее рассмотрены лишь простейшие методы нанесения Cu на любую поверхность, которые несложно организовать в домашних условиях, без каких-либо сложностей и финансовых затрат.
Такая методика подходит лишь для покрытия слоем Cu металлических деталей. По сути, технология мало чем отличается от того же цинкования в домашних условиях.
Оборудование понадобится простейшее:
Ванночка (емкость) стеклянная. Ее вместительность определяется габаритами обрабатываемой детали. Даже литровая банка или стакан – как варианты.

Медные электроды. Как правило, используются два. Это позволяет более качественно покрыть заготовку слоем со всех сторон и упрощает сам процесс. По ходу работы не придется периодически менять положение детали относительно электрода. Что именно использовать, зависит от конкретной ситуации – пластины из меди, куски толстой проволоки. Это непринципиально.
Источник тока и соединительные провода. Достаточно даже маломощного блока питания, на 6 – 8 В. Если в БП нет встроенного амперметра и не предусмотрена плавная регулировка напряжения, то придется использовать соответствующий прибор и реостат как отдельные элементы электрической цепи. Примерная схема, которую собирают для меднения деталей, показана на рисунке.
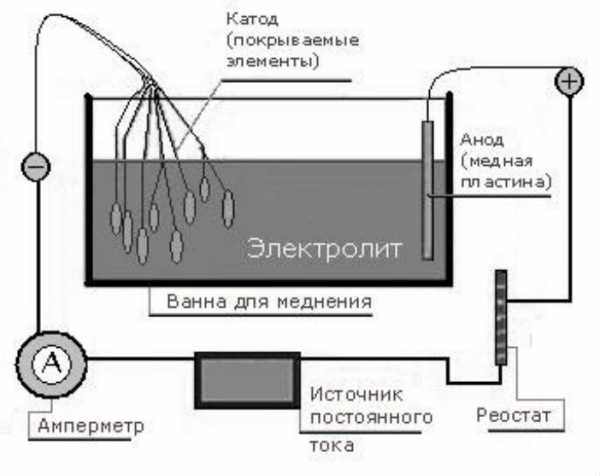
Электролит. Можно использовать покупной раствор, хотя придется и поискать. Если же его готовить самому, то на 100 мл воды дистиллированной понадобится серная кислота (3 мл) и медный купорос (20 г) – не дефицит.
После включения напряжения величина тока постепенно повышается до расчетного значения, и в таком режиме обработка осуществляется в течение ⅓ часа (время ориентировочное). Если меднение проводится впервые, то следует контролировать данный процесс. О том, что деталь можно вынимать из емкости, судят по оттенку ее поверхности и равномерности покрытия (отсутствию необработанных участков, раковин, вкраплений и так далее).
Остается лишь смыть с образца остатки электролита и просушить. Получается, что эта технология для реализации в домашних условиях никакой сложности не представляет.
Данным способом можно наносить металлическое покрытие на любые материалы. Суть заключается в «обмазке» (без прямого контакта) заготовки электролитом специальной кисточкой, щетинки которой – медные проволочки. Недостаток этой технологии в том, что добиться качественного меднения рельефных поверхностей вряд ли удастся. По крайней мере, понадобится много времени и усилий, чтобы тщательно обработать все «щели» и «выбоины».
Кисточка. В домашних условиях ее делают из многожильного медного проводника. Снять изоляцию и «распушить» один его конец – не проблема. Чтобы было удобнее работать, стоит подумать, из чего изготовить рукоятку кисточки. Ею придется водить по поверхности образца, а с учетом того, что провода гибкие, такое меднение станет испытанием для мастера. Как вариант – подвязать «рабочую часть» к карандашу, пластиковому корпусу шариковой ручки. Догадаться несложно.
Тара. Деталь перед меднением укладывается на любую подходящую посуду. Для удобства работы она не должна иметь высоких бортиков. Оптимальный вариант – тарелка. Плюс к этому – емкость, в которой будет электролит. В нее придется постоянно опускать кисточку, поэтому и здесь выбор не затруднен. Подойдет и стакан, если образец небольшой и раствора понадобится немного. Соответственно, вся тара предварительно обрабатывается – моется, чистится, кипятится, обезжиривается.
Сборка схемы. Аналогично предыдущему способу. Кисточка выполняет функцию анода, поэтому ее к «+» БП, а покрываемая деталь является катодом (к «–»).
Для обеспечения неразрывности электрической цепи в посуду наливается электролит, так, чтобы его уровень превышал высоту детали. Кисточкой, которая периодически также обмакивается в растворе (для этого он и заливается в отдельную тару), необходимо водить по-над образцом. В результате его поверхность покрывается слоем меди. По сути, производится ее напыление.

Понятно, что такой процесс в исполнении более сложный, так как проводится в «ручном» режиме. Необходимо постоянно следить, чтобы между кистью и обрабатываемой основой был небольшой зазор. Но и это не главное. Его неизменность – одно из условий равномерности покрытия.
В каких случаях целесообразно использовать такой способ меднения
Как определить требуемые параметры блока питания? Для плотности тока при меднении нормой считаются 0,5 А/дм² образца, который предстоит покрыть защитным слоем.
Медь довольно быстро окисляется. Перед началом процесса обработки изделия электроды следует хорошо зачистить.
Время выдержки детали в растворе выбирается исходя из того, какой толщины слой необходимо получить при меднении. Зависимость прямая – чем дольше идет обработка, тем толще покрытие.
При необходимости восстановления внешнего вида истершихся элементов фурнитуры (мебельной или иной) их меднение – неплохой выход из положения.
Автор не единожды сталкивался с тем, что люди, озабоченные проблемами экологии, сразу же задаются вопросом – а как в домашних условиях организовать утилизацию отработки? Ведь электролит не вечен, и использовать его всю жизнь точно не получится. Кстати, вполне резонное и более чем справедливое замечание.
Есть неплохое решение – собирать оставшуюся после меднения «бурду» в отдельной стеклянной емкости. Зачем? Пригодится. Этот раствор отлично подходит для обработки древесины. Ваш покорный слуга, читатель, сам пропитывал им лаги перед настилом полов на даче. Учитывая, что зимой она не отапливается, условия эксплуатации материала понятны. Когда спустя 12 лет потребовалось переложить половицы, выяснилось, что лаги – как новенькие. Не было даже малейшего намека на какую-то плесень, следы гнили.
Так как любому из нас приходится заниматься если не строительством, то уж ремонтом обязательно, нет смысла куда-то потихонечку, подальше от сторонних глаз, сливать использованный электролит. Не по-хозяйски это.
На самом деле, меднение в домашних условиях проводят многие умельцы в первую очередь для того, чтобы подготовить поверхность металла к последующей обработке различными защитными слоями.
Данной операции можно подвергать поверхности самых разных металлов и неметаллов, в том числе, стали, латуни, никеля и так далее.
Человечество используется в своих целях медь на протяжении многих тысячелетий и связано это, прежде всего с тем, что данный металл находится в природе в самородном состоянии, а кроме этого, обладает рядом уникальных свойств.
В настоящее время медь и самые разные сплавы на ее основе востребованы во многих промышленных сферах.
Без нее не может обойтись авиастроение, автомобилестроение, приборостроение и многие другие отрасли.
Медь и ее многочисленные сплавы достаточно распространены и в бытовой сфере.
Следует отметить и то, что добавки меди в различных сочетаниях позволяют эффективно защитить поверхности многих металлов, например, стали, латуни или никеля от различных агрессивных сред.
Один из наиболее распространенных способов покрыть тонким слоем металлическую поверхность — это выполнить нанесение меди.
В условиях дома в большинстве случае выполняется химическое меднение, причем существует несколько различных способов, каждый из которых имеет как свои плюсы, так и минусы.
Один из способов выполнить гальваническое нанесение меди в условиях дома, показан на видео ниже.
Как уже было сказано выше, в природе медь, как правило, находится в виде небольших самородков.
Это уникальное вещество представляет собой достаточно тяжелый металл, который на вид напоминает самородок яркого розово-красного оттенка.
Этот металл обладает относительной мягкостью и высокой ковкостью, кроме этого, имеет температуру плавления порядка тысячи ста градусов по Цельсию.
Он великолепно проводит не только тепло, но и электрический ток, что и объясняет повышенный спрос на данный металл в электротехнике и приборостроении.
В большинстве случаев в природе медь находится не в чистом состоянии, а с различными примесями.
Всевозможные природные добавки в зависимости от различных факторов в металле могут варьироваться и различаться приблизительно от десяти до пятидесяти раз.
Для данного металла большое значение имеет содержание в нем кислорода, и в зависимости от количества этого элемента в состав меди, разработана определенная классификация.
Так, медь может быть бескислородной и рафинированной.
Кроме этого, бывает медь с большим содержанием кислорода в своем составе, а также общего назначения, когда содержание кислорода максимальное.
Помимо данного элемента в этом металле также может находиться водород, попадающий туда за счет электролиза или отжига.
Медь имеет определенную кристаллическую решетку, и атомы водорода занимают в ней пространство в междоузлиях, а это значит, что на ее свойства они не оказывают практически никакого влияния.
Если медь в своем составе содержит в определенном количестве кислород, то водород имеет свойство определенным образом взаимодействовать, но только при достаточно высоких температурах с медной закисью, и в этом конкретном случае начинает формироваться водяной пар, который имеет достаточно высокие показатели давления.
Это оказывает негативное влияние на металл в целом и может привести в некоторых случаях к образованию вздутий, а также трещинам и разрывам.
Такое отрицательное воздействие у химиков получило название водородная болезнь.
На изменении показателей пластичности у меди в худшую сторону могут оказать влияние присутствие железа, сурьмы.
Те примеси, которые относятся к группе малорастворимых, понижают хрупкость этого металла, но только при достаточно высоких внешних температурах, а это значит, что для меди крайне нежелателен процесс обработки горячим давлением.
На видео выше показано химическое меднение данного металла.
Для выполнения меднения на поверхности стали, никеля, либо каких-то других металлов, применяется гальваника, при которой образуется тонкий медный слой.
Гальваническое нанесение меди представляет собой достаточно сложное химическое меднение, которое оказывает влияние на состав материала.
Гальваническое нанесение является предварительным, перед тем, как на поверхность никеля или другого металла будет нанесен различный защитный состав.
Гальваническое меднение свинца и других материалов, как правило, выполняется перед тем, как будет произведено хромирование, никелирование и так далее.
В данном случае медь выступает в качестве своеобразного припоя или другими словами — дополнительной добавки.
О том, как самостоятельно выполняется гальваника, показано на видео ниже.
Нанесенная таким образом медь в качестве припоя на поверхность никеля или какого-либо иного металла, способна достаточно прочно держаться, а кроме этого, способствует устранению некоторых дефектов.
На обработанную таким образом поверхность достаточно хорошо осаждаются многие другие материалы в качестве припоя.
Такие медные покрытия в качестве припоя практически не меняют состав исходного металла и характеризуются высоким сцеплением, хорошей электропроводностью, а также пластичностью.
Медь — это своеобразный блескообразователь в виде припоя, который практически не меняет исходный состав металла и выступает в качестве своеобразной добавки.
Основным методом нанесения данного металла (припоя) на поверхность никеля, стали и так далее является гальваника, и о том, как это сделать в домашних условиях, рассказывает видео ниже.
Для выполнения меднения в условиях дома не нужно обладать какими-то специфическими знаниями, достаточно только знать курс школьной химии.
За счет меднения, поверхности никеля или других материалов не меняют свой основной состав, так как оно выступает в качестве своеобразного припоя.
Для меднения в условиях дома потребуются достаточно примитивные материалы, которые можно приобрести в любом специализированном магазине.
Процедуру покрытия медью в качестве припоя можно выполнить с погружением в электролиты для меднения (раствор) и без погружения.
И в том, и в другом случае перед тем, как приступить к меднению, обрабатываемую деталь необходимо правильно подготовить.
Для этого она проходится наждачной бумагой, тщательно протирается щеткой с металлической щетиной и промывается под проточной водой.
Кроме этого, к меднению следует переходить после того, как заготовка будет обезжирена, для чего используют раствор на основе соды в подогретом состоянии.
Между данными анодами размещают подлежащую обработке деталь, которую подключают к минусу, соответственно, аноды к плюсу источника постоянного тока.
Также для меднения в цепь обязательно необходимо включить реостат.
После этого для выполнения меднения в условиях дома готовят специальный состав электролита, раствор с медным купоросом, серной кислотой и водой в определенных пропорциях.
После выполнения меднения сернокислое соединение сливают, заготовку промывают и тщательно высушивают.
На видео ниже показан процесс меднения в домашних условиях.
Меднение алюминия, меднение стали или цинка проводят способом без погружения в состав электролита.
В этом случае деталь также подготавливают к меднению путем тщательной обработки и промывки.
На проводе для удобства делают ручку и один из его концов подключают к плюсу постоянного источника тока.
После этого для выполнения меднения готовят специальный электролит — раствор с добавлением медного купороса и выливают его в емкость.
После этого раствор подключают к напряжению и при помощи кисти начинают обрабатывать деталь, нанося таким образом блескообразователь.
Процессу меднения подвергают всю заготовку (раствор) в течение нескольких минут.
По завершению меднения, раствор убирают, деталь промывают и тщательно высушивают. Процесс меднения без погружения в электролит показа на видео ниже.
Подвергнуть меднению можно практически любой металл, наложив, таким образом, на его поверхность защитное покрытие в виде слоя меди.
Видео:
Меднение – это технологический процесс, позволяющий наносить на металл, а также другие материалы слой меди толщиной от 1 до 300 мкм. Покрытие медным слоем обеспечивает хорошую адгезию покрытий и при увеличении толщины покрытий придает блеск изделиям, устраняет небольшие дефекты, позволяет создавать копии вещи. Удивительно, но все это можно делать и самим. Сегодня мы расскажем, как осуществить меднение в домашних условиях.

С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология процесса достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов:
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.

«Ингредиенты», без которых процесс не состоится, реально подготовить самим. Наши специалисты
утверждают, что прежде всего, нужны:
Стоит отметить, что химические реактивы для меднения найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах. Обязательно следует указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.

Химическое меднение является альтернативой электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды материалов подвергаются очистке по-разному:
Несмотря на возможность гальваники в домашних условиях, процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому следует неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью дома – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты нужно:
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на стальных и прочих изделиях, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
Медные покрытия:
Технологий нанесения покрытия существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.

Поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Данный способ имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшие толщины покрытий. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий:
Процесс длится до момента покрытия медным слоем изделия.
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом требуется наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным материалом для осуществления гальванопластики традиционно считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Можно сделать вывод, что меднение сегодня - это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. Компания «6 микрон» проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет под Вашу техническую задачу. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи помогут Вам определиться с подходящим курсом для обучения.
Медные покрытия, как правило, не применяются в качестве самостоятельного покрытия ни для декоративных целей, ни для защиты стальных деталей от коррозии. Это связано с тем, что медь в атмосферных условиях легко окисляется, покрываясь налетом окислов.
Однако благодаря хорошему сцеплению осажденной меди с различными металлами медное покрытие применяется в многослойных защитно-декоративных покрытиях в качестве промежуточного подслоя, а также для защиты стальных деталей от цементации. В гальванопластике медные осадки применяются для изготовления металлических копий, барельефов, волноводов и матриц.
Электролиты меднения подразделяют на кислые и щелочные. Из кислых электролитов используют сернокислые и борфтористоводородные. Наибольшее применение нашли сернокислые электролиты, отличающиеся простотой состава, устойчивостью и высоким выходом по току (до 100%). Недостатком этих электролитов является невозможность непосредственного покрытия стальных и цинковых деталей вследствие контактного выделения меди, имеющей плохое сцепление с основным металлом. Поэтому перед меднением стальных детален в кислых электролитах их предварительно меднят в цианистых электролитах или осаждают тонкий подслой никеля. К недостаткам сернокислых электролитов относятся также их незначительная рассеивающая способность и более грубая: структура осадков по сравнению с другими электролитами.
К щелочным электролитам меднения относятся цианистые, пирофосфатные и другие электролиты. Цианистые медные электролиты обладают высокой рассеивающей способностью, мелкокристаллической структурой осадков, возможностью непосредственного меднения стольных деталей. К недостаткам относятся низкая плотность тока и неустойчивость состава вследствие карбонизации свободного цианида под действием двуокиси углерода воздуха. Кроме того, цианистые электролиты характеризуются пониженным выходом по току (не более 60-70%).
Будьте внимательны! Компания «ЛВ-Инжиниринг» не предоставляет услуги по нанесению гальванических покрытий! Наша организация осуществляет проектирование гальванических производств, изготовление гальванических ванн и линий из полипропилена, монтаж и пусконаладочные работы по данному направлению.
Кислые электролиты меднения
Медь сернокислая - 150-250 г/л
Никель хлористый - 50-70 г/л
Температура = 18-25°С
Плотность тока = 1-4 А/дм 2
При перемешивании электролита сжатым воздухом можно довести катодную плотность тока до 6-8 А/дм 2 .
Для приготовления сернокислого электролита меднения растворяют медный купорос, фильтруют его в рабочую панну и при непрерывном помешивании добавляют серную кислоту.
При нанесении медных покрытий из сернокислого электролита медные аноды растворяются в основном с образованием двухвалентных ионов, которые, разряжаясь на катоде, осаждаются в виде металлической меди. Однако наряду с этими процессами происходят п другие, нарушающие нормальное течение электролиза. Возможно также анодное растворение с образованием одновалентных ионов, хотя и в меньшей степени.
В электролите, омывающем металлическую медь, идет также химический обратимый процесс: Cu + Cu 2+ = 2Cu + .
Накопление в растворе ионов одновалентной меди в больших количествах приводит к сдвигу реакции влево, в результате чего выпадает металлическая губчатая медь.
В растворе, кроме того, происходит окисление сернокислой одновалентной меди за счет кислорода воздуха н серной кислоты, особенно при воздушном перемешивании: Cu 2 SO 4 + 1/2O 2 + H 2 SO 4 = 2CuSO 4 + H 2 O. На катоде процесс заключается в разряде двухвалентных и одновалентных ионов меди, но в связи с тем, что концентрация ионов одновалентной меди приблизительно в 1000 раз меньше концентрации ионов двухвалентной меди, катодный процесс выглядит так: Cu 2+ + 2е - = Cu. Выход по току составляет 100%.
Для получения плотного гладкого осадка в электролите необходимо присутствие сорной кислоты. Серная кислота выполняет ряд функций: значительно повышает электропроводность электролита; понижает активность ионов меди, что способствует образованию мелкозернистых осадков; предотвращает гидролиз сернокислой закисной меди, который сопровождается образованием рыхлого осадка закиси меди.
Дефекты при эксплуатации сернокислого электролита меднения и способы их устранения
| Дефект | Причина дефекта | Способ устранения |
| Грубая крупнокристаллическая структура осадков | Недостаток кислоты | Добавить кислоту |
| Высокая плотность тока | Снизить плотность тока | |
| Шероховатые осадки | Загрязнение электролита механическими примесями | Отфильтровать электролит |
| Черные и коричневые полосы на покрытии | Присутствие в электролите примесей тяжелых металлов, мышьяка, сурьмы | Проработать электролит, при большом содержании примесей электролит заменить |
| Пористые, рыхлые осадки | Наличие в электролите солей железа | |
| Светлые блестящие полосы на покрытии, осадки хрупкие | Присутствие в электролите органических примесей | Отфильтровать электролит, проработать его током |
Борфтористоводородный электролит обладает несколько более высокой рассеивающей способностью, чем сернокислый. Кроме того, в борфтористоводородных электролитах можно применять высокие плотности тока. Состав электролита (г/л) и режим меднения:
Медь борфтористоводородная - 35-40 г/л
Кислота борная - 15-20 г/л
Кислота борфтористоводородная - 15-20 г/л
Никель хлористый - 50-70 г/л
Температура = 18-25°С
Плотность тока = до 10 А/дм 2
Электролит перемешивают сжатым воздухом или механической мешалкой.
Для приготовления борфтористоводородного электролита в борфтористоводородную кислоту небольшими порциями вводят свежеосажденную углекислую медь. Раствор углекислой меди готовят подливанием подогретого концентрированного раствора соды к раствору сернокислой меди при перемешивании. Полученный осадок декантируют, промывают и растворяют в борфтористоводородной кислоте. В приготовленный раствор добавляют свободную борфтористоводородную и борную кислоту до требуемого значения рН (1-1,5). В ванну с полученным электролитом доливают воду до рабочего уровня.
Современная техника выдвигает жесткие требования к характеристикам конструктивных элементов, во многих случаях эти задачи решает химическое меднение. Использование специальных покрытий поверхностей деталей выгодно экономически, так как гальваническое меднение позволяет понизить металлоемкость изделий из дорогостоящих металлов.
Плотность меди 8,96 г/см 3 , атомная масса 693,54, удельное электрическое сопротивление 1,68×10 -8 Ом×м, температура плавления +1083°С. На открытом воздухе в присутствии агрессивных химических соединении медь окисляется, при контакте с сернистыми соединениями покрывается пленкой сульфида меди темно-коричневого или серого оттенков. Под влиянием углекислоты и влаги пленка приобретает зеленый цвет, верхний слой состоит из гидрокарбонатов. Медь легко растворяется в растворе азотной кислоты, разбавленная серная кислота на химическое меднение негативного влияния почти не оказывает. Но наличие кислорода увеличивает скорость протекания химических реакций. При наличии открытых пор в покрытии образуется гальванопара, что нужно учитывать при меднении. Железо в этом случае является анодом, коррозионные процессы протекают очень интенсивно.
В связи с такими особенностями, процесс меднения в большинстве случаев должен завершаться дополнительной обработкой поверхностей. Покрытия шлифуются или полируются до зеркального блеска. Медь имеет высокую адгезию с различными металлами: алюминий, серебро, цинк, никель, свинец, хром и т. д. В связи с этими особенностями химическое меднение часто используется для создания подслоя при серебрении, никелировании, хромировании поверхностей деталей. Меднение получило широкое распространение в качестве метода эффективной защиты отдельных участков деталей от появления эффекта науглероживании при процессе цементации. В зависимости от назначения деталей или изделий гальваническое нанесение меди может иметь следующую толщину:
В процессе меднения используется большое количество специальных технологических растворов, разделяемых на две большие группы:
Процесс осаждения в кислых электролитах происходит при высокой плотности по току, они устойчивы, просты по химическому составу. Главными составляющими являются соответствующие кислоты и соли, осадки меди из них достаточно плотны и имеют крупнокристаллическую структуру. Недостатки – непосредственное меднение стали, цинковых сплавов и иных металлов происходит с более низким отрицательным потенциалом, чем медь.
Обработка деталей в комплексных электролитах выполняется за счет комплексных ионов, для них требуется высокая катодная поляризация. Выход по току меньше, что способствует более равномерному осаждению, структура мелкокристаллическая. Используются пирофосфатные, цианидные, аммонийные, триполифосфатные, цитратные и другие растворы.
Простые кислые составы
При перемешивании увеличивается концентрация медных ионов на катодном слое. При повышении температуры возрастает растворимость сульфата меди, электролит повышает кислотность, что приводит к получению мелкокристаллических осадков.
Для улучшения катодной поляризации в электролит добавляются поверхностно активные вещества. Дополнительно они уменьшают образование наростов на острых краях.
Для образования блестящего покрытия используются аноды АМФ, не допускающие образование шлама, или аноды из особо чистой рафинированной меди.
Электролит фторборатный.
Для недопущения попадания шлама аноды помещаются в чехлы, изготовленные из кислотоустойчивого материала, дополнительно раствор постоянно фильтруется.
При непрерывном перемешивании допускается повышать плотность тока. Контроль технологически параметров меднения осуществляется измерением кислотности раствора. Для повышения качества меднения используется карбонат натрия, для понижения медный купорос.
Режимы и состав нитратных электролитов
Комплексные электролиты
Режим и состав цианидных электролитов для меднения
Режим и состав пирофосфатных электролитов
Режим и состав этилендиаминовых электролитов
Без специальной обработки поверхностей медные осадки имеют недостаточную адгезию, причина – пассивирование стали раствором аммиака. Улучшение параметров покрытия достигается введением в раствор нитрата меди.
Устройство ванны меднения Линейные параметры и конструктивные особенности должны отвечать требованиям ГОСТ 23738-85. изготавливается из модифицированных особо устойчивых пластиков, конкретные марки подбираются с учетом параметров технологических процессов.
Ванна без кармана
Ванна с карманом
Конкретный выбор ванны меднения осуществляется в зависимости от особенностей предприятия, характеристик подлежащих меднению деталей и общих производственных мощностей.
Во время проектирования рассчитываются максимальные нагрузки с учетом объема раствора, длина, высота и ширина может изменяться по желанию заказчиков. При необходимости на ванны меднения устанавливается дополнительное оборудование и водопроводная арматура. За счет специальных механизмов улучшается качество процесса меднения. Используемые пластики адаптируются к химическому составу электролита и температурным режимам меднения.
Перед меднением с поверхности должна удаляться окалина, заусеницы и раковины. Качество обработки регламентируется положениями действующего ГОСТа 9.301-86. Конкретные параметры шероховатости устанавливаются в зависимости от назначения покрытия. После механической обработки деталей с поверхности должны быть удалены все дефекты, оказывающие негативное влияние на качество меднения. В обязательном порядке удаляется техническая смазка и эмульсия, металлическая стружка, продукты коррозионных процессов и пыль.
Подготовка к меднению производится при следующих технологических операциях:
От качества предварительной подготовки поверхностей во многом зависит процесс меднения и физические показатели осадков.
Для того чтобы подготовить металлический предмет к дальнейшей обработке, его нужно покрыть медью — такой процесс называют гальваностегией. Принцип его действия заключается в осаждении на поверхность обрабатываемой детали из другого металла, который растворен подходящим средством. Из данной статьи вы узнаете, как покрыть медью металл в домашних условиях, чтобы реализовать все последующие свои задумки с заготовкой.
Технология гальваностегии включает в себя создание раствора и образование различных электродов. Во время этого процесса медные ионы, которые растворены в электролите, притягиваются минусовым полюсом обрабатываемой детали на свою поверхностную точку.
Гальваностегия металлических деталей в промышленности применяется не только как завершающий обрабатывающий процесс. Она может применяться для того, чтобы подготовить детали к последующей операции (к примеру, хромированию, никелированию, серебрению каких-либо предметов).
В домашних условиях чаще всего проводится химическое меднение деталей. Также стоит заметить, что есть множество способов проведения такой процедуры, каждый из которых имеет свои преимущества и недостатки.
Покрывать медью металл в домашних условиях в последнее время стало очень полезно. Чаще всего к такой процедуре подходят в следующих целях:
Таким способом можно покрыть медью сталь в домашних условиях, а также другие детали за исключением алюминия и цинка.
Для дальнейшей процедуры необходимо подготовить следующие материалы:
Важно! Последний компонент можно приобрести в специальном магазине, а можно и изготовить самостоятельно. Для этого нужно сделать раствор серной кислоты и дистиллированной воды при соотношении 2/100 мл. Нужный раствор получится, когда вы добавите к составу не больше 20 г медного купороса.

Суть работы заключается в следующем:
Важно! Проследите за тем, чтобы пластины из меди были полность погружены в электролит.
В конечном итоге вы заметите, что смогли покрыть медью металл в домашних условиях, ведь он полностью покроется тонкой блестящей пленкой.
Важно! Толщина медного слоя будет зависеть от того, как долго была выдержана деталь в электролите.
Данный способ отлично подойдет для металлов-исключений, что были названы ранее — цинка и алюминия.
Алгоритм работы:
Важно! Напряжение должно быть не более, чем 6 В.
Важно! Деталь должна быть предварительно очищена и обезжирена.
Важно! Следите за тем, чтобы между концом растеребленной проволоки и металла был маленький слой электролитного раствора (и катод, и анод обязательно должны быть смочены этим раствором).
В статье представлен вариант экономичного и простого решения по замешиванию собственного раствора для гальванизации различных поверхностей с возможностью дальнейшей пайки. Как обычно, автор приводит множество фотографий и сопутствующее описание, а в конце дает сам рецепт.
3D принтеры отлично подходят для изготовления всевозможных корпусов, но сам по себе пластик, являясь диэлектриком, не обеспечивает нужного экранирования.
Когда мне понадобился корпус для нового зарядочувствительного усилителя (ЗЧУ) и трубок с гелием-3 He3, я спроектировал такой вариант:
Спустя 6 часов я уже держал его в руках:
Самая интересная часть заключалась в омеднении этого корпуса изнутри. В линейке
Tifooесть аэрозольная краска «Медь», на которую после высыхания можно наносить гальваническое покрытие. Требуется это только для гальванизации не проводящих ток деталей.
После предварительной грунтовки эта краска отлично держится на PLA-пластике, для чего вполне хватает двойного нанесения.
Сразу скажу, что это недешевый вариант покрытия, и tifoo просят еще 30 баксов за электролит. Я же подумал, что сложного тут ничего нет и решил изготовить его сам.
Сначала я попробовал просто сульфат меди — безуспешно. Тогда я решил добавить к нему серную кислоту, что уже дало хоть какой-то положительный результат. По крайней мере теперь медь начала оседать. Однако кристаллы получались слишком большими и совершенно неоднородными. Из-за обширной площади покрытия они быстро окислялись и т.д.
Здесь и был задействован магический компонент – сахарин (орто-сульфобензимид). С ним кристаллы получились уже более мелкие и однородные. Самое же главное, что теперь осадок не зависел от геометрии электрода.
Этот раствор хорош тем, что им можно гальванизировать практически все (кроме цинка, хрома, алюминия, титана, олова и железа). К тому же его можно паять!
А вот готовый корпус для моего ЗЧУ, покрытый электролитом:
А теперь самая долгожданная часть.
Использовать нужно только дистиллированную воду температурой 25°C, так как раствор очень чувствителен к загрязнениям.
Внимание: изопропиловый спирт все портит. Даже минимального осадка на поверхности после чистки будет достаточно, чтобы загубить весь электролит.
Вот и все!
Покрываемая деталь должна быть катодом, и вам понадобится (чистый!) медный анод, при этом плотность тока должна составлять 20-30 мА на см2. Убедитесь, что анод расположен близко к детали, и его площадь не менее площади омедняемой детали.
На покрытие уходит от 10 минут до 1.5 часов, в зависимости от требуемой толщины. Но после определенного момента ее наращивание останавливается. Не знаю почему, в химии я не силен.
Химическое меднение - это процесс покрытия металла медью без использования внешнего источника питания. Это текущее меднение без электричества. Этот процесс использует преимущество вытеснения «более благородных» (менее электроотрицательных) металлов из раствора «менее благородными» (более электроотрицательными) металлами. В случае меднения предметов из железа или стали, погруженных в раствор соли меди, напримерсульфат меди, происходит осаждение медного покрытия (металл, который менее электроотрицателен, более благородный) на поверхности железа из стали (металл менее благородный, более электроотрицательный). В результате химического меднения образуются очень толстые покрытия порядка 0,02–0,2 мкм. Качество покрытий во многом зависит от состава раствора, интенсивности перемешивания раствора, времени выдержки и опыта оператора. Химическое меднение подходит только для нанесения декоративных покрытий, поэтому в технологических процессах оно не используется повсеместно.
Самым простым решением химического меднения является рабочая жидкость следующего состава:
- Вода дистиллированная 1 л
- Сульфат (пентагидрат) меди (II) 50 г / л
- Серная кислота (VI) (d = 1,84) 5-10 мл / л
Время воздействия этого раствора должно быть ограничено несколькими или несколькими десятками секунд. Слишком длинное покрытие вызовет травление объекта и отслоение покрытия. Процесс следует проводить при температуре в пределах 15-20 градусов Цельсия при сильном перемешивании.
Для процесса меднения заготовка должна быть тщательно подготовлена - обезжирена, протравлена и активирована. После меднения всю заготовку нужно как можно быстрее нейтрализовать в растворе гидроксида натрия или карбоната натрия. Затем промыть дистиллированной водой и высушить.
Другой метод декоративного меднения, позволяющий наносить глянцевые покрытия, - это галтовка немолистных опилок, пропитанных медным раствором, содержащим комплексные соли меди.
Например с составом:
- Вода дистиллированная 1 л
- Сульфат (пентагидрат) меди (II) 37,5 г / л
- Аммиак (25% водный раствор) 50 мл
- Винная кислота 50-100 мл
Мы пропитываем опилки несмолистых деревьев такой рабочей жидкостью, затем помещаем их в деревянный барабан и обрабатываем около 30 минут, используя медленные вращательные движения.По истечении этого времени отделите опилки от медных элементов, нейтрализуйте их в растворе гидроксида натрия или карбоната натрия и промойте дистиллированной водой. Покрытые медью предметы блестят, потому что при такой обработке покрытие наносится и полируется одновременно.
Сульфат меди, деионизированная вода и нейтрализующие вещества (каустическая сода и карбонат натрия) доступны на сайте distripark.com
* Эта статья предназначена только для ознакомления.Представленное описание, в частности использование продуктов, является примерным и представляет собой необязательную информацию о характеристиках и возможностях их использования / применения. В любом случае перед использованием продукта посоветуйтесь со специалистом, безопасно и оправдано ли конкретное использование. Мы не несем ответственности за использование предложенных решений даже в очень похожих ситуациях.
. Меднение путем гальваники - это покрытие другого материала медью с использованием явления электролиза. Подвешенный в ванне анод, который является источником меди, и катод, который является местом осаждения меди, подключенный к электрическому току, заставляют движение ионов меди Cu 2+, которые мигрируют с анода, растворенных в виде результат процесса - через электролитическую ванну к катоду, на который укладывается медь. Электролитическое меднение можно проводить в ваннах различного типа.Наиболее эффективными и долговечными считаются так называемые кислотные ванны. Покрытия, получаемые за единицу времени, намного толще, чем, например, при использовании цианидных ванн. Однако кислотные ванны имеют свои ограничения, например, стальные или железные предметы нельзя покрывать медью непосредственно в них. Поскольку меднение является отличной защитой, например, от науглероживания или азотирования, оно часто используется косвенно. То есть стальные предметы сначала покрывают медью в ванне с цианидом.После получения начального слоя меди, а затем и фактического меднения, происходит гораздо более эффективный процесс с использованием кислотной ванны.
Наиболее часто используемая кислотная ванна - это ванна, приготовленная на основе сульфата меди и серной кислоты со следующим составом:
- 1 литр дистиллированной воды, нагретой до 18-20 градусов Цельсия.
- 200 г пентагидрата кристаллического сульфата меди.
- 25 мл концентрированной серной кислоты.
Медный анод и прикрепленные к катоду предметы, которые должны быть покрыты медью, могут быть вставлены в подготовленную таким образом ванну.
Меднение в кислотной ванне требует стабильной температуры ванны в диапазоне 18-20 градусов Цельсия и постоянного, но не интенсивного перемешивания ванны. Перед началом процесса аноды следует очистить и предварительно активировать, например, протравив в течение нескольких секунд в 8% -ной азотной кислоте. В процессе мы используем ток плотностью 1-2 А / дм2 и напряжением 2-3 В. В результате часового процесса мы получаем среднюю толщину покрытия 30 мкм, т.е. 0,03 мм. . Для получения более толстых покрытий продолжительность процесса пропорционально увеличивается.Во время меднения состояние покрытия нужно проверять каждые 20 минут - разумеется, без отключения электричества. В случае обнаружения дефектов, особенно на углах и острых краях, а также пятен и обесцвечивания лицевых поверхностей и образования так называемых крупнокристаллических капель, силу тока следует немедленно уменьшить, а качество нанесенное покрытие должно сразу улучшиться. После завершения меднения как можно скорее удалите остатки электролитической ванны.Лучше всего это сделать, тщательно ополоснув под проточной водой из-под крана. Деактивированный таким образом элемент может быть высушен, например, в опилках, и пассивирован, например, путем покрытия слоем масла, или непосредственно передан для дальнейшей электролитической обработки. Медь часто является не целевым покрытием, а промежуточным покрытием, предназначенным для обеспечения хорошей адгезии основы для следующего слоя серебра, серебра и золота, никеля, никеля и хрома, олова.
Кристаллический пентагидрат сульфата меди, доступный в distripark.com.
<< Предыдущий Вернуться в блог Следующий >>
* Эта статья предназначена только для ознакомления. Представленное описание, в частности использование продуктов, является примерным и представляет собой необязательную информацию о характеристиках и возможностях их использования / применения. В любом случае перед использованием продукта посоветуйтесь со специалистом, безопасно и оправдано ли конкретное использование.Мы не несем ответственности за использование предложенных решений даже в очень похожих ситуациях.
* Эта статья предназначена только для ознакомления. Представленное описание, в частности использование продуктов, является примерным и представляет собой необязательную информацию о характеристиках и возможностях их использования / применения. В любом случае перед использованием продукта посоветуйтесь со специалистом, безопасно и оправдано ли конкретное использование.Мы не несем ответственности за использование предложенных решений даже в очень похожих ситуациях.
., можно получить блестящие медные покрытия, превосходящие по качеству покрытия, полученные в сульфатной ванне.
Указанную ванну готовят растворением сульфата меди в воде с последующим добавлением аммиака для образования медно-аминного комплекса и, наконец, винной кислоты для получения слегка кислого pH раствора.
Как и в случае меднения в сульфатной ванне, предметы не должны находиться в указанной ванне долгое время, а когда медное покрытие покрывает их полностью, их следует немедленно вынуть и промыть.
Рассматриваемая ванна также может использоваться для небольших серийных изделий.Для этого чистые (не содержащие смол) опилки пропитываются этим раствором и обрабатываются вместе со стальными предметами в деревянном барабане. Процесс длится 30 минут при медленном вращении барабана. Затем вставленные предметы отделяются от опилок на сите, промываются и сушатся. Покрытые медью предметы блестят, потому что при такой обработке покрытие наносится и полируется одновременно.
************************************************ *****
Немного более толстые медные покрытия можно получить в ванне эдетата со следующим составом:
сульфат меди 37,5 г / дм3,
эдетат натрия2 87,5 г / дм3.
Обезжиренные, протравленные и активированные стальные предметы погружают в эту ванну на 1-10 минут при интенсивном перемешивании. Температуру ванны можно держать в широких пределах, от 20 до 50 ° C.
Процесс омеднения в ваннах данного состава можно проводить также протиранием поверхности предметов тампоном, смоченным в ванне.
Процессы описаны в Руководстве по гальванике.
В промышленных условиях сталь обычно покрывают медью в ваннах с щелочным цианидом.
Полученные таким образом слои меди можно покрыть покрытием даже толщиной в несколько миллиметров в кислотных ваннах.
Основная задача собственного меднения или другого меднения - подготовка поверхности металла к дальнейшей обработке. Данной операции могут быть подвергнуты различные металлы, но не металлы, среди которых следует отметить:
Благодаря своим многочисленным достоинствам этот металл получил широкое распространение.Сегодня медь и многие ее сплавы широко используются в промышленности. Металл находит применение в авиастроении, автомобилестроении, приборостроении и других отраслях промышленности. Не меньшей популярностью в быту пользуются металл и изделия из него. Само по себе меднение - один из лучших методов нанесения покрытия на тонкий металл. В домашних условиях меднение можно осуществить несколькими способами.
Для этого вам понадобится:
Гальваническая медь собственного производства

Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора в соляную кислоту.После того, как раствор медного купороса будет приготовлен, его нужно тщательно перемешать, чтобы не осталось частиц. Затем в этот раствор нужно добавить тонкой струйкой соляную кислоту. Не забывайте соблюдать меры предосторожности и пользоваться перчатками и очками. После добавления в раствор соляной кислоты тщательно перемешайте.
Итак, раствор готов и можно начинать медить дома. Для этого нужно взять металлическую деталь, на которую вы будете наносить слой меди и подготовить ее к работе.Подготовка включает шлифование. Эта процедура позволяет не только очистить металлическую поверхность, но и обезжирить ее. Та же процедура применяется к деталям из латуни или свинца. Затем покрытие следует тщательно промыть раствором кальцинированной соды. Это позволит более тщательно обезжирить материал.

Сода кальцинированная для обезжиривания материала
Затем поверхность погружают в раствор сульфата меди и соляной кислоты. Следует отметить, что первый слой меди очень тонкий и непрочный, поэтому желательно удалить его металлической щеткой.После этой операции стальную или свинцовую поверхность следует снова промыть раствором кальцинированной соды и снова погрузить в раствор для меднения. Эти манипуляции приведут к тому, что слой меди в доме на поверхности будет намного толще и прочнее, так как снять его с объекта можно будет только наждачной бумагой, а не металлической щеткой, как в прошлый раз.
Этот метод позволяет получить очень качественное медное покрытие, которое можно удалить только наждачной бумагой.Чтобы улучшить медное покрытие в домашних условиях, деталь необходимо повторно погрузить в раствор. Этот метод отличается простотой и высокой эффективностью, в том числе и для свинцовых продуктов.
Меднение обычно называют процедурой меднения, толщина медного слоя в таких случаях может составлять от 300 мкм и более. Меднение стали - один из важнейших процессов гальваники, так как он используется как дополнительный процесс перед нанесением других металлов для хромирования, никелирования, серебряного покрытия.
Медный слой отлично прилегает к стали и способен сглаживать различные дефекты поверхности.
 Медные покрытия характеризуются высокой адгезией к другим поверхностям, изделиям из свинца, особенно к металлу, а также высокой электропроводностью и пластичностью. Последний нанесенный финиш - ярко-розовый матовый или глянцевый цвет. Под воздействием атмосферных воздействий медные покрытия могут окисляться и покрываться оксидами с различными радужными пятнами.
Медные покрытия характеризуются высокой адгезией к другим поверхностям, изделиям из свинца, особенно к металлу, а также высокой электропроводностью и пластичностью. Последний нанесенный финиш - ярко-розовый матовый или глянцевый цвет. Под воздействием атмосферных воздействий медные покрытия могут окисляться и покрываться оксидами с различными радужными пятнами.
 Обычно можно использовать гальваническое меднение:
Обычно можно использовать гальваническое меднение:
Меднение происходит вместе с другим гальваническим покрытием
Первый способ предполагает обработку металлического изделия наждачной бумагой, щеткой и ополаскивание водой. Затем обезжиривание в горячем содовом растворе с многократным ополаскиванием. Затем две медные пластины-анода опускаются в стеклянную емкость по медным проводам. Деталь подвешивают между пластинами на проводе, после чего включают ток.
Второй метод - для изделий из стали, алюминия и цинка.
Эта процедура применима в различных случаях, так как медное покрытие можно наносить на алюминиевые столовые приборы, сувениры, подсвечники и т. Д.Неповторимый эффект дают изделия не из металла со слоем меди. Это могут быть стебли растений, листья и т. Д. Из-за отсутствия проводящего слоя на покрываемых объектах вместо него используется специальный электропроводящий лак, который наносится на поверхность.
Лак содержит ряд органических растворителей, пенообразователей и мелкодисперсный порошок графита, благодаря которому создается электропроводность. Лак наносится тонким слоем на сухую поверхность, а после высыхания через час можно приступать к омеднению.При желании медь можно придать другим оттенкам цвета с помощью специальных приемов. Высокое качество и уникальность таких изделий заслуженно приравнивают к настоящим украшениям.
Меднение - это процесс гальванического покрытия медью различных поверхностей. Слой меди имеет прочную адгезию к металлам, сглаживает полости на покрытой поверхности, обладает высокой электропроводностью и пригоден для дальнейшей обработки. Меднение может использоваться как самостоятельный процесс или как часть более сложных (серебряное покрытие, никелирование, хромирование).Наряду с промышленным способом в домашних условиях практикуется меднение, что позволяет решить многие бытовые проблемы. Помимо высоких технических параметров, это покрытие отлично выглядит, что обуславливает его использование в различных дизайнерских решениях.
В промышленных условиях меднение происходит в мощных гальванических ваннах, оборудованных автоматикой и другими специальными устройствами. Однако этот процесс также доступен внутри компании, что устраняет необходимость в сложном химическом оборудовании.
Последовательность технологических операций следующая:
1. С поверхности металла снимается оксидная пленка. Использованная наждачная бумага, кисть, полировальная паста;
2. Окрашенный предмет обезжирить содовым раствором и тщательно промыть водой;
3. Две медные пластины (аноды) погружены в стеклянный сосуд на медной проволоке, между ними подвешена деталь;

4. Аноды подключаются к «плюсу» источника постоянного тока, а медная часть - к «минусу»;
5.Токорегулирующий реостат и амперметр включены последовательно в электрическую цепь. В качестве источника постоянного тока можно использовать автомобильный аккумулятор или адаптер питания;
6. Электролит наливается в емкость так, чтобы полностью покрыть поверхность анодов. Эту операцию необходимо выполнять с особой осторожностью, избегая попадания агрессивных жидкостей на открытые участки тела!
7. Плотность тока устанавливали 2А на дм2 обрабатываемой поверхности, температура электролита: 20-26 градусов, время обработки: 20-25 минут;

8.Медная часть вынимается из емкости, и процесс завершается. Толщина медного слоя может быть увеличена за счет более длительного пребывания деталей в гальванической ванне.

Состав электролитов несложный: серная кислота - 40 г, медный купорос - 190 г, вода - 980 г.
Несколько советов по омеднению:

Иногда бывает необходимо заменить сломанную медную мебельную фурнитуру, и в продаже есть только никелированные изделия.При этом легко монтируется установка для осаждения меди. Необходимое оборудование и материалы: блок питания 12 В / 3 А, серная кислота и медный купорос.
Сначала необходимо удалить никелирование. Для этого деталь держится с помощью пинцета, который подводится «вниз» от источника питания. С прикрепленной тканью
Положительный электрод, смоченный 5% -ной серной кислотой, вытирает поверхность изделия.
При снятии никелирования образуются ядовитые пары, от которых следует защищать органы дыхания.Желательно использовать специальные очки и респиратор с угольным фильтром. Очищенная поверхность полируется.
Следующим шагом будет установка простейшей гальванической установки. В банку помещается медный электрод, подключаемый к «плюсу» блока питания, а заготовка - к «минусу».
Заливается электролит, состоящий из сульфата меди, воды и 5% серной кислоты в соотношении 1/5/3, и подается электричество. Готовые изделия полируются до приятного блеска.

Есть много различных применений для внутреннего меднения. Медь можно использовать для изготовления алюминиевых столовых приборов, давая им вторую жизнь, для рыболовных приманок, подсвечников и многого другого. Особенно эффективны работы, в которых декоративное покрытие наносится на неметаллические предметы: стебли растений, листья, желуди и даже засушенных насекомых. Естественная фактура исходного материала в сочетании с красотой гальванического покрытия создает неповторимый художественный эффект.
Технология изготовления таких изделий немного сложнее, но в домашних условиях вполне реальна. В материале с покрытием нет токопроводящего слоя, поэтому на поверхность наносится специальный токопроводящий лак. В состав лака входят органические растворители, пленкообразующие вещества и мелкодисперсный порошок графита, обеспечивающий электропроводность.
Лак наносится тонким слоем на сухое растение, он подсыхает, и через час все готово к омеднению.После гальваники внешний вид продукта может быть улучшен. Есть несколько способов добавить различные оттенки цвета к гальванической меди, включая патинирование, химическое окрашивание и окисление.
Качество графики, полученной с использованием этих технологий, находится на уровне настоящих ювелирных украшений.
Уважаемые читатели, комментируйте статью, задавайте вопросы, подписывайтесь на новые публикации - нам интересно ваше мнение :)
Медь - один из древних металлов: люди начали использовать ее для изготовления инструментов еще в 4 тысячелетии до нашей эры.C.E. Такое широкое распространение меди объясняется тем, что это вещество встречается в естественном металлическом состоянии. И сегодня медь используется повсеместно - в металлургии, автомобилестроении, электротехнике и строительстве.
Металлическая медь - тяжелый розово-красный металл, ковкий и мягкий, плавится при температуре выше 1080 градусов по Цельсию, очень хорошо проводит тепло и электричество: электропроводность меди в 1,7 раза больше, чем у алюминия, и в 6 раз больше. железа и лишь немного уступает по электропроводности серебра.
Конкретные свойства меди определяются содержанием в металле определенных примесей, количество которых может варьироваться от 10 до 50 раз. По содержанию кислорода принято использовать следующую классификацию меди:
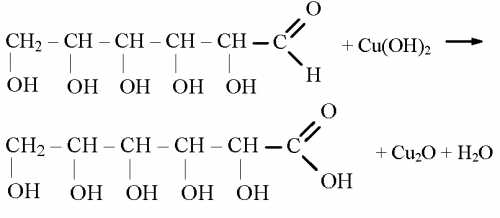
Помимо кислорода, медь может содержать водород, который переносится на металл во время электролиза или отжига в атмосфере, содержащей водяной пар. При высоких температурах водяной пар разлагается с образованием водорода, который легко диффундирует в медь.
Атомы водорода в бескислородной меди расположены в промежутках решетки и не оказывают особого влияния на свойства металла. В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с оксидом меди, в то время как в объеме меди образуется водяной пар, который присущ высокому давлению, что приводит к набуханию, растрескиванию и растрескиванию.Это явление называется «водородная болезнь».
Железо, висмут, сурьма и свинец ухудшают пластичность меди. Плохо растворимые в меди примеси (свинец, кислород, сера, висмут) вызывают хрупкость при высоких температурах, что затрудняет процесс горячей обработки.
Основное свойство меди, определяемое ее использованием, - это высокая электропроводность или низкое удельное электрическое сопротивление. Примеси, такие как железо, фосфор, мышьяк, олово и сурьма, значительно ухудшают его электропроводность.Механическое состояние меди имеет большое влияние на значение электропроводности.
Еще одним важным свойством меди является ее высокая теплопроводность. Добавки и свойства сплава снижают теплопроводность меди, поэтому медные сплавы на основе самой меди значительно уступают этому показателю.
Медь устойчива к коррозии при нормальных температурах в таких средах, как пресная вода, сухой воздух, морская вода с низкой скоростью потока, неокисляющие кислоты и солевые растворы без доступа кислорода, сухие галогеновые газы, щелочные растворы, кроме аммиака и солей аммония, кислоты органические , фенольные смолы и спирты.

Медь нестабильна в аммиаке, хлориде аммония, окисляющих минеральных кислотах и растворах кислотных солей. Его коррозионные свойства также значительно ухудшаются в некоторых средах по мере увеличения количества загрязняющих веществ. Медь может контактировать со своими сплавами, оловом и свинцом во влажной атмосфере, а также в морской и пресной воде. При этом контакт меди с цинком и алюминием недопустим из-за их быстрого износа.
Медь, ее сплавы и соединения широко используются в различных отраслях промышленности. Медь в электротехнике используется в чистом виде для производства контактных и неизолированных шин, кабельной продукции, генераторов, телефонного и радиооборудования. Вакуумные аппараты, теплообменники и трубопроводы изготовлены из меди.
Сплавы меди с различными металлами используются в автомобильной промышленности и в производстве химического оборудования.Проволока из красной меди для создания всевозможных линий и гибки самых сложных элементов. Высокие свойства меди делают ее незаменимой при производстве деликатных деталей.
Меднение - это процесс меднения с толщиной слоя от 1 до 300 микрон или более. Меднение стали - один из важнейших процессов гальваники, который используется как предварительный процесс при подготовке поверхности металла к покрытию другими металлами - хромом, никелем и серебром, а также как полностью независимый процесс.
Использование меднения в качестве подготовительной операции связано с тем, что этот металл может очень плотно прилегать к стали, устраняя дефекты поверхности. Другие материалы хорошо ложатся на медь, но не очень хорошо на чистую сталь.
90 230
Медные покрытия характеризуются высокой адгезией к различным металлам, высокой электропроводностью и пластичностью. Обычно они используются на стальных, цинковых и алюминиевых деталях.
Свеженанесенное медное покрытие имеет светло-розовый матовый или глянцевый цвет в зависимости от технологии нанесения.Атмосферные медные покрытия легко окисляются и покрываются слоем оксидов, создавая пятна различных оттенков и переливающиеся пятна.
В большинстве случаев применяется гальваническое меднение:

Меднение используется вместе с другими гальваническими покрытиями:
Процедура меднения своими руками доступна даже новичкам. Для этого достаточно знать его основные тонкости. В домашних условиях существует два метода меднения: с погружением в электролит и без погружения.
Металлическое изделие обрабатывают наждачной бумагой для удаления оксидного слоя, протирают щеткой, тщательно промывают водой, обезжиривают в горячем содовом растворе и снова промывают.Затем принято опускать две медные пластины, являющиеся анодами, в стакан или банку на медных проводах.
Деталь, подвешенная между пластинами на проволоке. Провода, выходящие из медных пластин, соединены друг с другом и подключены к плюсу источника питания, а некоторые - к минусу. Затем в схеме есть реостат, регулирующий ток и миллиамперметр. Требуется источник постоянного тока с напряжением не более 6 В.

Для домашнего меднения приготовьте следующий раствор электролита.Возьмите 20 граммов медного купороса и 2-3 миллилитра серной кислоты на 100 миллилитров воды и вылейте в миску. Убедитесь, что этот раствор полностью покрывает электроды.
При использовании реостата установите ток в диапазоне 10–15 мА на каждый квадратный сантиметр площади детали. Примерно через 20 минут выключите электричество и снимите изделие, которое уже было покрыто тонким слоем меди. Чем дольше длится процесс, тем толще будет слой меди.
Эта процедура выполняется для стали, алюминия и цинка.С одного конца скрученного провода снимается изоляция, а затем тонкие медные провода нужно разорвать, чтобы получить медную щетку. Для удобства работы его необходимо привязать к медной щетке или деревянной палке, а другой конец кабеля подключить к плюсу источника питания.
Затем нужно приготовить электролит - раствор медного купороса, желательно слегка подкисленного, и перелить его в широкую бутыль, в которую будет удобно окунуть кисть. Подготовьте кусок металла или другой небольшой плоский предмет.Его следует натереть мелкой наждачной бумагой и обезжирить кипячением в растворе стиральной соды.

Затем поместите пластину в кювету или ванну и подключите проводом к минусу источника питания. После того, как схема собрана, достаточно залить электролит. Окуните «кисть» в раствор медного купороса, который следует провести по длине пластины, не касаясь поверхности.
Рекомендуется работать так, чтобы между щеткой и пластиной всегда был слой электролита.Электропроводку в рабочем состоянии необходимо пропитать раствором. Пластина на глазах будет покрыта слоем красной металлической меди. На обработку небольшой детали уйдет несколько минут.
После нанесения покрытия просушите деталь на воздухе и протрите тусклый медный слой до блеска тканью или шерстяной тканью. Процесс меднения алюминия, при котором продукт не погружают в ванну с электролитом, а обрабатывают снаружи на небольших поверхностях с добавлением электролита, используется в случаях, когда продукт настолько велик, что найти подходящую ванну невозможно.
Меднение не отличается от обычных ванн для гальваники. Электролиты для меднения довольно легко получить, если у вас под рукой есть подходящие ингредиенты. Есть два типа медных растворов: щелочные и кислые.
В кислых растворах невозможно получить хорошо прилегающие медные покрытия на изделиях из цинка и стали, потому что в этом случае цинк и железо растворяются вместе с медью, и адгезия к защитному покрытию нарушается.
Чтобы устранить эту особенность, рекомендуется первый тонкий слой меди (2-3 мкм) сделать в растворе щелочного меднения, а в дальнейшем наращивать покрытие до определенной толщины в кислотном электролите, что больше экономичный. Цинковые изделия сложной формы лучше всего смешивать в щелочных электролитах.

Наиболее распространенными кислотными электролитами являются фтороводород и сульфат. Наибольшее распространение получили сернокислые электролиты, которые отличаются простым составом, высоким выходом по току и значительной стабильностью.
Перед медированием стальных деталей в кислотных электролитах рекомендуется сначала медить их в цианидном электролите или нанести тонкий подслой никеля. У этих электролитов есть несколько недостатков.
Одна из них - невозможность прямого покрытия цинковых и стальных деталей из-за контактного высвобождения меди, которая имеет плохую адгезию к основному металлу. Кроме того, электролиты имеют низкую рассеивающую способность и более толстую структуру отложений по сравнению с другими электролитами.
Среди электролитов для щелочного меднения известны пирофосфатные и цианидные электролиты.
Цианидные электролиты из меди характеризуются высокими диспергирующими свойствами, возможностью меднения столярных изделий и мелкокристаллической структурой отложений.
К недостаткам щелочных электролитов относятся низкая плотность тока и нестабильность раствора из-за карбонизации свободного цианида диоксидом углерода. Кроме того, цианидные электролиты отличаются пониженным выходом по току - не более 60-70%.
Таким образом, медь - это металл, который используется повсеместно: в автомобилестроении, электротехнике и строительстве. А в гальванике известна технология покрытия медью для подготовки металлических поверхностей к покрытию другими металлами или как самостоятельный процесс.
Их изготавливают многие мастера в первую очередь для подготовки металлической поверхности к последующей обработке различными защитными слоями.
Эта операция может применяться к поверхности самых разных металлов и неметаллов, включая сталь, латунь, никель и так далее.
Человечество использует медь в своих целях на протяжении многих тысячелетий, и это в основном связано с тем, что этот металл находится в естественном состоянии в природе и обладает рядом уникальных свойств.
Сегодня медь и различные сплавы на ее основе востребованы во многих отраслях промышленности.
Авиация, автомобилестроение, приборостроение и многие другие отрасли не могут обойтись без него.
Медь и многие ее сплавы широко используются в быту.
Следует также отметить, что различные комбинации добавок меди могут эффективно защищать поверхности многих металлов, таких как сталь, латунь или никель, от различных агрессивных сред.
Один из наиболее распространенных методов утонения металлической поверхности - нанесение меди.
Химическое меднение в основном выполняется в домашних условиях, и существует несколько различных методов, каждый из которых имеет свои преимущества и недостатки.
Один из способов прокладки меди в домашних условиях показан на видео ниже.
Как упоминалось выше, медь обычно встречается в природе в виде небольших самородков.
Это уникальное вещество представляет собой довольно тяжелый металл, похожий на самородок со светлым розово-красным оттенком.
Этот металл обладает относительной мягкостью и высокой пластичностью, кроме того, он имеет температуру плавления порядка тысячи сотен градусов по Цельсию.
Прекрасно проводит не только тепло, но и электрический ток, чем объясняется повышенная потребность в этом металле в электротехнике и приборостроении.
В большинстве случаев в природе медь бывает не в чистом виде, а с различными примесями.
Все типы натуральных добавок, в зависимости от различных факторов в металле, могут различаться и варьироваться от десяти до пятидесяти раз.
Для этого металла большое значение имеет содержание кислорода, и в зависимости от количества этого элемента в составе меди была разработана определенная классификация.
Таким образом, медь может быть бескислородной и рафинированной.
Кроме того, в его состав входит медь с высоким содержанием кислорода, а также медь общего назначения при максимальном содержании кислорода.
Помимо этого элемента, металл может также содержать водород, который туда попадает путем электролиза или отжига.
Медь имеет особую решетку, и атомы водорода занимают свое место в трещинах, а это значит, что они практически не влияют на ее свойства.
Если медь в своем составе содержит в определенном количестве кислород, то водород имеет тенденцию взаимодействовать определенным образом, но только при достаточно высоких температурах с оксидом меди, и в этом конкретном случае начинает образовываться водяной пар, который имеет достаточно высокую индикаторы давления.
Обычно это отрицательно влияет на металл и в некоторых случаях может привести к образованию пузырей, а также к трещинам и разрывам.
Этот отрицательный эффект в химии называется водородной болезнью.
Присутствие железа и сурьмы может повлиять на ухудшение показателей пластичности меди.
Примеси, относящиеся к группе малорастворимых, снижают хрупкость этого металла, но только при достаточно высоких внешних температурах, что делает процесс горячей обработки под давлением крайне нежелательным для меди.
На видео выше показано химическое меднение этого металла.
Для нанесения меднения на поверхность стали, никеля или некоторых других металлов применяется гальваника, при которой образуется тонкий слой меди.
Гальваника меди - это довольно сложное химическое покрытие меди, которое влияет на состав материала.
Гальваника - это предварительный процесс перед нанесением другого защитного состава на никель или другую металлическую поверхность.
Гальваника свинца и других материалов обычно выполняется перед хромированием, никелированием и т. Д.
В этом случае медь действует как припой или, другими словами, дополнительная добавка.
Как самостоятельно выполнить гальванику показано на видео ниже.
Медь, нанесенная таким образом в виде припоя на поверхность никеля или другого металла, способна удерживаться достаточно плотно, а также помогает устранить некоторые дефекты.
Многие другие материалы неплохо откладываются, как припой, на поверхности, обработанной таким образом.
Такие медные покрытия, как припой, практически не изменяют состав основного металла и отличаются высокой адгезией, хорошей электропроводностью и пластичностью.
Медь - это разновидность осветлителя припоя, которая практически не изменяет исходный состав металла и действует как своего рода добавка.
Основной способ нанесения этого металла (припоя) на поверхность никеля, стали и т. Д.гальваника, и в следующем видео рассказывается, как это сделать в домашних условиях.
Для выполнения меднения в домашних условиях не требуется специальных знаний, достаточно знать курс школьной химии.
Посредством меднения поверхности никеля или других материалов не изменяют свой основной состав, поскольку он действует как своего рода припой.
Медь в бытовых условиях потребует довольно примитивных материалов, которые можно купить в любом специализированном магазине.
Процедура меднения может выполняться с погружением в медный электролит (раствор) или без него.
В обоих случаях перед началом меднения заготовка должна быть должным образом подготовлена.
Для этого его протирают наждачной бумагой, тщательно протирают щеткой с металлической щетиной и ополаскивают под проточной водой.
Дополнительно после обезжиривания объекта приступают к меднению, для чего используется горячий раствор на основе соды.
Между этими анодами помещается обрабатываемая деталь, которая соединяется с минусом, соответственно, анод с плюсом источника постоянного тока.
Кроме того, в случае меднения в цепи должен быть реостат.
Затем для проведения меднения в домашних условиях готовится специальный состав электролита - раствор с сульфатом меди, серной кислотой и водой в определенных пропорциях.
После меднения сульфатное соединение отфильтровывают, заготовку тщательно промывают и сушат.
На следующем видео показан процесс меднения в домашних условиях.
Меднение алюминия, меднение стали или цинка производится методом без погружения в состав электролита.
В этом случае деталь также подготавливается для меднения путем тщательной обработки и ополаскивания.
Для удобства ручка сделана на проводе, и один из ее концов подключен к плюсу источника постоянного тока.
Затем для меднения готовится специальный электролит - раствор с добавлением медного купороса и переливается в емкость.
Затем раствор подключают к источнику питания и с помощью кисти начинают обрабатывать детали, нанося отбеливатель.
Вся заготовка (раствор) подвергается процессу меднения в течение нескольких минут.
После завершения меднения раствор удаляют, деталь тщательно промывают и сушат. На следующем видео показан процесс нанесения покрытия медью без погружения в электролит.
Практически любой металл можно подвергнуть омеднению, если нанести на его поверхность защитное покрытие в виде слоя меди.
Видео:
Гальваника - это раздел электрохимии, изучающий нанесение электролитов на поверхность металлических изделий. Метод гальваники - это процесс, при котором на продукт наносится металлическое покрытие, чтобы защитить его от коррозии или других внешних воздействий. Однако в последнее время большую популярность приобрела декоративная гальваника. И несмотря на довольно сложный технологический процесс, гальваника проводится в домашних условиях.
Этот процесс требует не только некоторых знаний химии и физики, но и некоторого оборудования, которое вы можете изготовить самостоятельно.
Для этого требуется:
 Характеристика и сложность Хромирование, меднение, серебряное покрытие или другое покрытие - это многоступенчатый процесс. На начальном этапе необходимо подготовить среду из вышеуказанных материалов и подготовить электролит. Для его приготовления вам потребуются химические реактивы, измеренные в определенных пропорциях с точностью до грамма. Конечно, для достижения такой высокой точности нужны специальные (желательно электронные) весы.
Характеристика и сложность Хромирование, меднение, серебряное покрытие или другое покрытие - это многоступенчатый процесс. На начальном этапе необходимо подготовить среду из вышеуказанных материалов и подготовить электролит. Для его приготовления вам потребуются химические реактивы, измеренные в определенных пропорциях с точностью до грамма. Конечно, для достижения такой высокой точности нужны специальные (желательно электронные) весы.
Далее можно переходить к следующему этапу: в емкость сливают подготовленный электролит, в нее опускаются аноды и подключаются к «+», а между ними помещается изделие, которое подключается к «-», так что цепь замкнута и высвободившийся металл в электролите откладывает на поверхности продуктов.
 Перед нанесением покрытия на изделие необходимо тщательно очистить поверхность изделия ... Это очень важно, так как от этого этапа будет зависеть качество и долговечность покрытия. Для этого изделие проходит несколько этапов очистки: от обезжиривания до шлифовки и пескоструйной обработки. Для обезжиривания продукта можно использовать любое органическое вещество, например ацетон, растворитель, бензин или спирт. Однако решение может отличаться в зависимости от материала изделия.
Перед нанесением покрытия на изделие необходимо тщательно очистить поверхность изделия ... Это очень важно, так как от этого этапа будет зависеть качество и долговечность покрытия. Для этого изделие проходит несколько этапов очистки: от обезжиривания до шлифовки и пескоструйной обработки. Для обезжиривания продукта можно использовать любое органическое вещество, например ацетон, растворитель, бензин или спирт. Однако решение может отличаться в зависимости от материала изделия.
В последнее время получили распространение гальванические ванны, для получения декоративного эффекта ванны из чугуна и стали начали покрывать медью и никелем.Поэтому для обезжиривания изделий из таких материалов используются специальные горячие растворы каустической соды, жидкого стекла, окисленного фосфорной кислотой натрия или кальцинированной содой. Или, если изделие выполнено из цветного металла, используйте для стирки мыльный раствор. Благодаря этому изделия обезжириваются, полируются и шлифуются ... Затем их погружают в емкость с электролитом и анодами, где на поверхность наносится покрытие.
Прежде всего, помните, что гальваника - очень опасный процесс, потому что вещества, используемые для приготовления электролита, очень токсичны, и особенно при нагревании, что необходимо, неправильное обращение с химическими веществами может вызвать серьезные ожоги или респираторные заболевания. Поэтому специалисты рекомендуют не пренебрегать правилами безопасности:
90 478Меднение - это процесс нанесения проводящего слоя меди на поверхность изделия. Для чего нужно меднение в домашних условиях? Как уже говорилось выше, гальваника проводится в защитно-декоративных целях ... Меднение можно просто отнести к другому. Изделия из черных металлов после меднения выглядят очень оригинально, к тому же, что немаловажно, защищают их от коррозии.Однако, по мнению специалистов, меднение изделий из чугуна может привести к летальному исходу, поэтому перед процессом изделия покрывают слоем никеля, а затем - медью.
Для меднения используется электролит с медным купоросом и раствор серной кислоты и воды, нагретый до комнатной температуры (18-20 градусов). Перед нанесением медного или никелированного покрытия каждое изделие проходит тщательную очистку, методы которой выбираются в зависимости от металла, из которого изготовлено изделие. Например, изделия из алюминия необходимо предварительно очистить от оксидного слоя, этот процесс еще называют травлением, а затем их промывают в специальном растворе оксидов воды и серной кислоты.
Хромирование сделано для увеличения прочности и защиты от внешних воздействий, но не забывайте, что хромированные изделия смотрятся эффектно. Особенно, если это диски из крутых элитных авто или деталей мотоцикла. Таким образом, с точки зрения самого процесса, медное или никелированное покрытие выполняется до хромирования как более нейтральный и универсальный метод. Или изделие сначала покрывается никелем, потом медью и только потом начинается хром.
В качестве электролита используются такие вещества, как свинец, олово и сурьма, в пропорции: 85 × 11 × 4%. В отличие от медного или никелевого покрытия, в процессе хромирования оттенок покрытия и цвет можно регулировать, они зависят от температуры и состава электролита. Например, для получения блестящего оттенка необходимо нагреть электролит до температуры 35-55 градусов, молочного оттенка - температура должна быть выше 55 градусов, матового оттенка - ниже 35 градусов.
А цвет может варьироваться от темно-синего, агатового, синего до черного.После покрытия изделие промывают в содовом растворе и полируют специальными пастами.
Изделие перед серебрением, как и в первых двух случаях, сначала покрывается никелем. Электролит состоит из хлорида серебра, кальцинированной соды, цианида железа-калия и дистиллированной воды. Температура электролита не должна превышать комнатной, а в качестве анода используются графитовые пластины.
.90 000 электролитического металлического меднения, доступного в домашних условиях. На главную Гальваника медиМеднение - это процесс гальваники поверхности медного слоя.
Медный слой придает изделию визуальную привлекательность, что позволяет использовать технологию гальваники меди в строительных проектах. Он также придает металлу высокую электропроводность, что позволяет продукту подвергаться дальнейшей обработке поверхности.
Меднение может использоваться как основной процесс для создания поверхностного слоя, а также как промежуточная операция для последующего нанесения другого металлического слоя.Этот метод включает, например, процесс серебрения, хромирования и никелирования.
Меднение можно сделать в домашних условиях. Это дает возможность решать многие бытовые проблемы.
Чтобы сделать медное покрытие самостоятельно, необходимо приобрести оборудование и материалы, необходимые для этого процесса.

Прежде всего, необходимо подготовить источник электроэнергии. Различные домашние мастера рекомендуют использовать силу тока, которая распространяется в широком диапазоне.Работы следует проводить на постоянном токе.
В качестве источника питания можно взять аккумулятор КБС-Л напряжением 4,5 вольта или новый аккумулятор марки «Крона» рабочим напряжением 9 вольт. Как вариант, можно использовать маломощное зарядное устройство с напряжением не более 12 вольт или автомобильный аккумулятор.
Необходимо использовать реостат для регулирования напряжения и плавного выхода из процесса.
Подготовьте нейтральную емкость для раствора электролита, например, сделанную из стекла, а также широкие пластиковые емкости, достаточно большие, чтобы вместить его часть.Емкости должны выдерживать температуру не менее 80 ° C.
Вам также понадобятся аноды, чтобы покрыть всю поверхность детали. Они предназначены для подачи тока в раствор электролита и распределения его по всей поверхности детали.
Для выполнения гальваники в домашних условиях вам также потребуются химические реактивы для приготовления раствора:
Когда у вас есть все необходимое, можно приступать к работе.
Медно-сульфатная сталь является одним из основных процессов в области гальваники, так как она используется для предварительного покрытия медью. Он имеет отличную адгезию к стали, в отличие от других металлов, которые плохо сцепляются со сталью. Медный слой, в зависимости от технологии, отлично сцепляется со стальными изделиями.
Существует две технологии нанесения покрытия: с погружением изделия в раствор электролита и метод бесконтактного покрытия поверхности медью без помещения ее в раствор жидкого электролита.
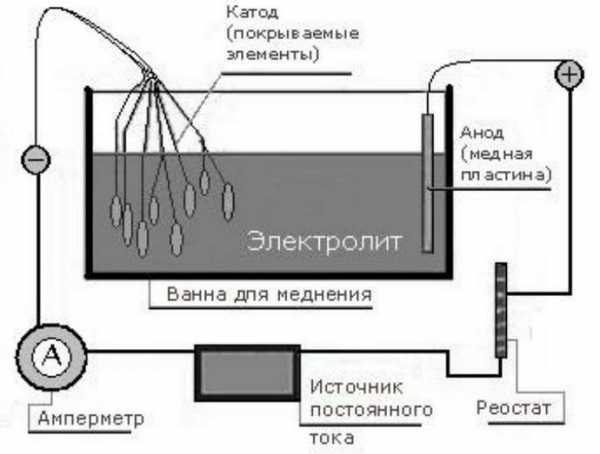
Процесс состоит из следующих шагов:
Этот метод применяется не только к стальным изделиям, но также к изделиям из алюминия и цинка. Процесс выглядит следующим образом:
Между поверхностью детали и импровизированной медной щеткой всегда должен быть слой раствора электролита, поэтому щетку необходимо постоянно погружать в электролит.
Меднение - отличный способ обновить алюминиевые столовые приборы и другие изделия из алюминия, используемые в доме.
Покрытие медным купоросом можно выполнить самостоятельно. Упрощенный вариант демонстрации процесса - меднение алюминиевой пластины простой формы.

Вы можете попрактиковаться в этом примере. Процесс такой:
1. Поверхность пластины сначала очистить, а затем обезжирить.
2. Затем на него нужно нанести немного концентрированного раствора медного купороса (медного купороса).
3. Следующим шагом является подключение отрицательного вывода к алюминиевой пластине.Подключить провод к плате можно обычным зажимом.
4. Положительный заряд прикладывают к устройству, состоящему из неизолированного медного провода диаметром от 1 до 1,5 мм, конец которого распределен между щетинками зубной щетки.
Во время работы этот конец провода не должен касаться поверхности алюминиевой пластины.
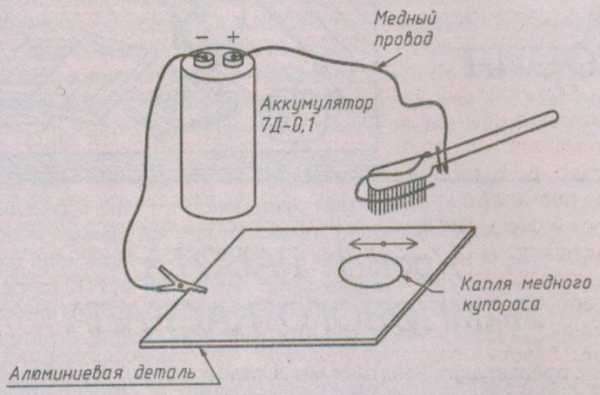
5. Окунув щетинки в раствор медного купороса, они начинают чистить щеткой участок, подготовленный для покрытия медью.В этом случае нет необходимости замыкать цепь, касаясь поверхности алюминиевой пластины концом медного провода.
6. Меднение поверхности сразу становится заметным визуально. Чтобы слой был качественным, совсем не обязательно торопиться с окончанием процесса.
7. По окончании работы слой меди следует зачистить дополнительной очисткой, удалив остатки медного купороса и протерев поверхность спиртом.
Гальваника - это процесс электрохимического воздействия на продукт с целью придания ему необходимой формы с помощью металла, нанесенного на поверхность.

Обычно эта технология применяется для нанесения металлических покрытий на неметаллические изделия. Он широко используется в дизайне ювелирных украшений и товаров для дома.
Покрытие заготовки должно быть электропроводным. При отсутствии такого слоя объект сначала покрывают графитом или бронзой.
Основными металлами, используемыми для гальваники, являются медь, никель, серебро и хром. Применяется также металлизация поверхности стальными сплавами.
Гальваника в домашних условиях пользуется особой популярностью у мастеров. Для получения желаемой формы с копий делается слепок. Для этого используется легкоплавкий металл, графит и гипс.
После изготовления формы изделие металлизируется электролитом.
Процесс извлечения металла из раствора и нанесения его на поверхность металлического изделия называется гальваникой. Медь - Нанесение меди на поверхность металлических изделий.
Процесс меднения широко распространен в промышленности и используется не только как отдельный процесс, но и как подготовительный процесс перед хромированием, никелированием и серебрением. Использование меднения в качестве подготовительной операции связано с тем, что медь очень плотно прилегает к стали, выравнивает поверхностные дефекты, а другие металлы очень хорошо осаждаются на меди, а чистая сталь является непрочной.
Меднение металлов в домашних условиях не такая уж и сложная операция, есть два способа: с погружением в электролит и без него.
Отшлифуйте металлический предмет, как обычно, наждачной бумагой, чтобы удалить оксидный слой, протереть кистью, тщательно промыть водой, обезжирить в горячем содовом растворе и снова сполоснуть. В банке или стакане две нижние медные пластины - аноды на проводах (желательно медных). Деталь между ними подвесьте на проволоке. Соедините провода, идущие от медных пластин, вместе и подключите к положительному полюсу источника питания, а часть - к отрицательному; включить в цепь реостат для регулирования тока и миллиамперметр (тестер).Источник питания постоянного тока с напряжением не более 6 В. 9000 3
Раствор электролита для меднения: 20 г сульфата меди и 2–3 мл серной кислоты на 100 мл воды - влить в емкость, раствор должен полностью покрыть электроды. С помощью реостата установите ток от 10 до 15 мА на каждый квадратный сантиметр площади детали. Минут через двадцать выключите электричество и снимите деталь - она покрыта тонким слоем меди. Чем дольше длится процесс, тем толще слой меди.
Этот процесс подходит не только для стали, но также для цинка и алюминия. Снимите изоляцию с одного конца мягкой проволоки и растяните тонкие медные проволоки, чтобы образовалась медная щетка. Для удобства привяжите его к деревянной палочке или карандашу, а другой конец шнура подсоедините к положительному полюсу источника питания.
Приготовьте электролит - концентрированный раствор медного купороса, желательно слегка подкисленного - и перелейте его в широкую бутыль, в которой будет удобно окунуть «кисточку».
Приготовьте кусок металла или другой небольшой предмет, желательно с плоской поверхностью. Протереть мелкой наждачной бумагой и обезжирить кипячением в растворе стиральной соды. Поместите пластину в лоток или кювету и подключите ее к отрицательной клемме источника питания с помощью кабеля. Схема собрана, остается только ввод электролита.
Окуните «кисть» в раствор медного купороса и проведите им по пластине, стараясь не касаться поверхности; работайте так, чтобы между пластиной и щеткой всегда был слой электролита.Электропроводка всегда должна быть погружена в раствор. На наших глазах пластина будет покрыта красным слоем металлической меди. На обработку небольшой детали уйдет несколько минут. После нанесения покрытия просушите деталь на воздухе и протрите матовый медный слой до блеска шерстяной или льняной тканью.
Такой процесс, при котором деталь не погружается в ванну с электролитом, а обрабатывается снаружи на небольших участках при постоянном добавлении электролита, используется в случаях, когда деталь настолько велика, что для нее не может быть найдена подходящая ванна. ...
В этом уроке я покажу вам, как заделать металлическую шайбу медью за несколько простых шагов. У вас будет широкое поле для экспериментов: вы сможете изменять время, напряжение и кислотный состав. Я рассмотрю только основные этапы электролитического меднения, объясняя, «как это сделать», но не вдаваясь в детали «почему».
Вкратце о собственном эксперименте: его цена колеблется в пределах 50–150 рублей, продолжительность эксперимента составляет 1–3 часа, а его сложность, в зависимости от ваших навыков гальваники меди, колеблется от легкой до средней.
Внимание! Проведите эксперимент с медью в хорошо проветриваемой комнате, а если вы молоды, попросите помощи у взрослого.
Что вам понадобится:
Я записал видео для этого урока.В нем я прошел все этапы меднения, которые описаны ниже.
Я не уверен, что «растворение» - правильное слово, но оно точно объясняет, что мы собираемся делать на этом этапе. Начните с того, что схватите медный предмет с помощью крокодилов. Затем поместите предмет в контейнер. Убедитесь, что крокодилы не касаются друг друга. Добавьте уксус в емкость, пока большая часть медного предмета не будет покрыта, но не позволяйте крокодилам контактировать с уксусом (см. Фотографии).
А теперь пора подключить крокодиловые провода к источнику питания. Пока не подключайте адаптер питания к сети. При подключении обоих зажимов типа «крокодил» к источнику питания установите напряжение 12 В. Затем вы можете подключить устройство к сети.
(На видео видно, что штекер адаптера питания отрезан для удобства подключения крокодилов.)
Вы заметите, что одна часть медного провода пузырчатая. Запомните эту часть, она отрицательная.
Я позволил всей конструкции поработать около 30 минут, но вы можете попробовать поиграть с напряжением и временем.Из соображений безопасности я рекомендую оставаться в диапазоне 0–12 В, так как с этими настройками все работает очень хорошо.
Через 30 минут я отключил питание и отключил отрицательный крокодил (со стороны пузырящейся меди). Затем я прикрепил к этому крокодилу металлический предмет (в моем случае - шайбу). Установите напряжение питания на самое низкое (первое). Минимум моего блока 3В. Подключите устройство снова и посмотрите, как металлический предмет покрыт медью.Я оставил стиральную машину в растворе примерно на 30 минут.
Считается, что продукт следует сушить 1-2 дня после обработки. Не знаю, правда это или нет, но я не заметил никакой разницы при удалении лишнего материала из стиральной машины, оставался ли он на 2 дня или 30 минут.
Для того, чтобы изделие блестело, достаточно его отполировать (используя соответствующие инструменты и материалы), но не переусердствуйте, потому что на покрываемом объекте есть только тонкий слой меди.
Обязательно поэкспериментируйте со временем выдержки и напряжениями для получения разных результатов и постарайтесь получить как можно более однородное медное покрытие.
Медный сплав более распространен в современном мире. Его наносят на поверхность, чтобы добавить визуальной привлекательности различным продуктам. В домашних условиях часто делают меднение, чтобы значительно повысить электропроводность. В некоторых случаях рассматриваемый процесс является промежуточной операцией, позволяющей нанести на поверхность другое вещество.
В последнее время в домашних условиях покрывают медью различные предметы.В большинстве случаев технология используется для достижения следующих целей:

Медь в домашних условиях встречается крайне редко, поскольку такой материал не выдерживает воздействия высоких температур. Кроме того, пластичность основания приводит к появлению трещин конструкции.
Металлическое меднение - это особая технология нанесения слоя меди толщиной от 1 300 мкм и более. Специфика применяемых технологий определяет, что медное покрытие прочно прилипнет к металлической поверхности. Среди особенностей, которые приобретает заготовка, отметим следующие моменты:
Копирование дома можно сделать с помощью специального решения.Учтите, что процесс требует использования специальных реагентов. Поэтому необходимо обеспечить наличие эффективной приточной вентиляции, а также средств индивидуальной защиты. Замедление пластика немного другое, связано это с применением особой технологии.
Рассматриваемая процедура доступна даже новичкам в области металлургии. Чтобы получить качественную поверхность, нужно знать все особенности процесса. Отечественное меднение свинца и других металлов может производиться по двум различным технологиям:
В обоих случаях обеспечивается электропитание, от которого вещество активируется.
В зависимости от того, какого результата вы хотите достичь, выбирается наиболее подходящий метод обработки. Назовем пример:
Обе технологии обработки имеют определенные характеристики, которые следует учитывать.
Меднение в домашних условиях иммерсионным методом очень распространено. Эта технология позволяет получить однородное покрытие. К особенностям этого способа обработки можно отнести следующие моменты:

При использовании этой технологии сила тока устанавливается на 15 мА на квадратный сантиметр. Покрытие всей поверхности специальным сплавом обычно занимает не менее 20 минут. С увеличением длины периода покрытие становится толще.
Аналогичный метод используется для покрытия стали, цинка или алюминия.В этом случае покрытие изделия медью в домашних условиях проводится проволокой, с которой заранее снимается изоляция для получения своеобразной щетки. Другой конец шнура подключается к положительному источнику питания. Химическое меднение в домашних условиях также предполагает использование специального раствора, повышающего эффективность процесса.
Среди особенностей создания раствора, требующего решения, можно отметить следующие моменты:
Вещество наносится на поверхность и металлическая поверхность подготавливается. Его очищают от примесей, а затем обезжиривают. Затем заранее подготовленную пластину помещают в ванну и подводят к ней минус от источника питания.

Этот процесс требует, чтобы между собранными проводами и пластиной всегда был слой электролита. Это обеспечивает высокую степень проводимости. Достаточно нескольких секунд, чтобы покрыть изделие небольшого размера.
После нанесения покрытия продукт сушат на воздухе. Избегайте попадания различных загрязнений. Следующим шагом нужно протереть медный слой шерстяной тканью или другой тканью. В большинстве случаев рассматриваемая технология применяется, когда изделие имеет большие размеры и его нельзя погружать в ванную комнату.
Меднение можно провести в домашних условиях даже на самом обычном оборудовании. Монтаж ванной комнаты для проведения рассматриваемой процедуры осуществляется примерно так же, как и с обшивкой. Обратите внимание, что есть два типа активных растворов: кислотные и щелочные.
Во время работы можно использовать:
Медить алюминий и другие сплавы в домашних условиях не займет много времени. Для очистки получившейся поверхности можно использовать различные ткани.
Обработка поверхностей различных предметов проводится с целью получения декоративного эффекта или в качестве промежуточной обработки перед дальнейшими операциями. Многие процессы доступны для выполнения и не требуют большого количества оборудования. Один из самых популярных методов обработки - это меднение, которое также можно провести в домашних условиях.
Меднение - это процесс нанесения тонкого слоя меди на поверхность объекта. Это делается гальваническим методом, то есть переносом ионов меди от положительно заряженного источника на отрицательно заряженную поверхность, подлежащую обработке. Чаще всего процесс меднения является подготовительным этапом перед нанесением никелирования и хромирования, но часто меднение становится отдельным типом отделки. Гальваника широко используется и требует меднения.
90 350
Есть два варианта собственной меди:
С погружением детали в электролит. У вас должен быть достаточный объем резервуара с электролитом для выполнения процедуры. После предварительной подготовки, заключающейся в очистке поверхности наждачной бумагой и ополаскивании в горячем содовом растворе, объект подключается к отрицательному электроду и на некоторое время погружается в электролит.
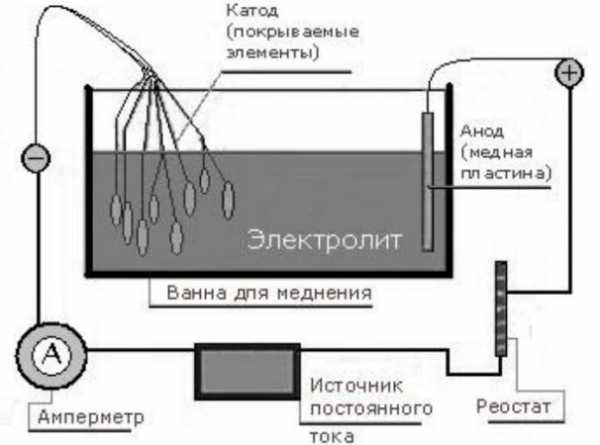
Не погружается в воду. Сталь, алюминий, свинец, цинк можно обрабатывать. Обработка проводится без погружения в емкость, обычно этот вариант применяется для крупных деталей.
Оба варианта вполне доступны для домашней самореализации.

Чтобы получить медную сталь или другие металлы, вам понадобятся определенные материалы и оборудование.Вам понадобится:







Электролит должен состоять из воды, сульфата меди и соляной кислоты.Сначала в воду добавляют сульфат меди до получения насыщенного раствора. Его необходимо тщательно перемешать, чтобы не осталось твердых частиц. Затем в раствор тонкой струйкой добавляют соляную кислоту (а не наоборот!). Всего для покрытия вам понадобится:
Теперь все готово, можно приступать к омеднению дома.



Внимание! Следует помнить, что соляная кислота является химически активным реагентом, поэтому при себе необходимо иметь средства защиты - перчатки, очки и как лучше подготовить рабочее место.
Процедура нанесения покрытия:
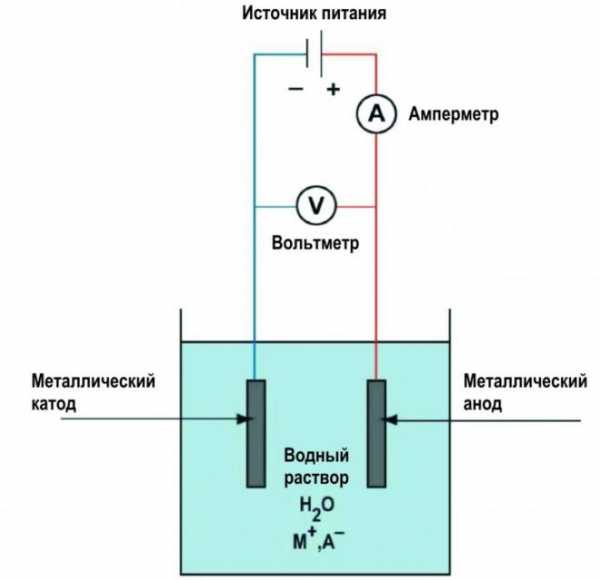
Часто бывает необходимо удалить слой покрытия с хромированных деталей. Для этого на деталь наносится отрицательный заряд, а на положительный электрод наматывается ткань, смоченная в растворе серной кислоты (5%).Протирает поверхность детали, снимается слой хрома. Во время процедуры следует защищать кожу, глаза и органы дыхания от паров кислоты.
Гальваника может производиться без погружения деталей в емкость с электролитом. Для этого нужно подключить к нему отрицательный электрод. Положительный контакт представляет собой медный провод, конец которого отодвигают на 1-2 см от изоляции и разминают таким образом, чтобы получилось нечто вроде щетки.
Для нанесения слоя медного покрытия «кисть» погружается в электролит, а затем конец кисти проводится по поверхности детали, не касаясь ее, но сохраняя между собой промежуточный слой. Постоянно погружая анод в электролит, покройте всю поверхность слоем меди. Процедура требует навыков и времени, но результат того стоит.
Медить можно не только на металлические предметы. Гальваника широко распространена, когда меднение наносится на различные засушенные растения, насекомых и другие неметаллические предметы.
Технология нанесения покрытия мало чем отличается от обычной, только в начале процесса следует наносить на поверхность электропроводящий лак. После высыхания краски предпринимаются обычные шаги по нанесению слоя меди. Полученные изделия имеют высокую декоративную или художественную ценность и высоко ценятся получателями.
.После презентации техники перегородчатой эмали, подготовленной Самией Анной Бетли, сегодня мы представляем вам еще одну интересную технику, с помощью которой вы можете создавать эффектные украшения. Сегодняшний урок был подготовлен специально для Royal-Stone Агой Орловской - художницей, известной своими работами в серебре с использованием филиграни, но также использующей другие техники в своей работе. Сегодня Aga познакомит вас с техникой гальванопластики, т.е.Способом удивительно воспроизвести форму и текстуру натуральных медных листьев, а также получить интересные формы и текстуры меди.
Приглашаем вас прочитать, посетить профиль Художника на Facebook и заглянуть в ювелирный магазин , созданный Агой Орловской .
Примечание: В представленной методике используются опасные для здоровья и жизни препараты и химические вещества. Приступая к работе, будьте особенно осторожны, запаситесь и используйте соответствующие меры безопасности (проветриваемое помещение, защитную одежду), а также строго следуйте указаниям и рекомендациям производителей используемых препаратов.
Электроформование меди - одна из самых интересных техник, которые мы можем использовать в своей работе с ювелирными изделиями. Истоки гальванопластики восходят к 1840-м годам, так что это относительно молодая ювелирная техника, почему? Потому что для гальванопластики нужно электричество. О чем это все? Объект, который мы хотим покрыть медью, погружается в специальный раствор, медный электрод также погружается в этот раствор, прикладывается напряжение (к электроду и объекту) и ... объект покрывается медью в таинственном способ.То есть не в секрете, потому что это простая и понятная физика. В этом посте я дам вам возможность с радостью насладиться лепкой из меди, создавая осенние украшения, например, из желудей. и уходит.
Что на картинке?
Медь от электрода, подключенного к «+» - аноду - растворяется, отдает электроду два электрона и в виде положительно заряженных ионов (катионов) переходит в раствор к отрицательному электроду - катоду - который притягивает Это. Там ионы меди «берут» два электрона и спокойно садятся на предмет, покрытый медью (наш катод). Чтобы сделать возможным «захват» электронов медью, если мы хотим покрыть медью изолятор (камень, лист, семена), мы должны позволить заряду каким-то образом течь по этому изолятору, отсюда, например,красим токопроводящей краской (об этом в пункте II).
Может возникнуть вопрос, для чего это решение, если медь идет с анода, воды, например, недостаточно? Раствор играет вспомогательную роль, это как магистраль, по которой катионы текут.
Рекомендуется, чтобы ток, протекающий через раствор, находился в диапазоне 2-10 А / дм2.
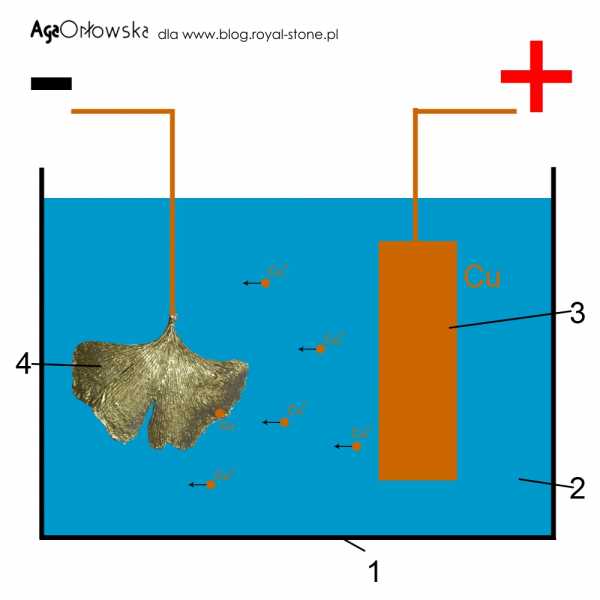
Чтобы начать играть с гальванопластикой, рекомендую пойти двумя путями. Лучше всего во время прогулок собрать запас интересных листьев, желудей, семян, гальки и т. Д.Просушите листья в книжке и подсушите семена, орехи и желуди. Идите по магазинам одновременно.
Список покупок:
1) лабораторный источник питания - работающий в диапазоне 0-3А, 0-30В, с возможностью работы в режиме CC ( Constant Current - стабилизация выходного тока)
2) медный обмоточный провод диаметром примерно 1,5 - 1,6 мм - этот провод покрыт изоляционным слоем
3) запас медных проводов разного диаметра, рекомендую комплект 0,9 мм, 1,2 мм, 2 мм, 3 мм - покупаем медные кабели и снимаем изоляцию.
4) дистиллированная вода - желательно сразу 5 л.
5) серная кислота 96% в год
6) медный купорос на год
7) материал для медных электродов, для газовых инсталляций рекомендую медные трубы - можно купить в строительных магазинах кусками длиной 2,5 м, можно конечно купить много медной проволоки диаметром 4 мм,
7) запас перчаток лабораторных
8) очки защитные
9) контейнер, в котором мы будем гальванопластик, я использую прозрачный прямоугольный пластиковый контейнер вместимостью ок.2 л, некоторые предпочитают бочки.
10) сода пищевая
11) супер клей (большая упаковка)
12) графитовый порошок
13) большой тюбик водной акриловой краски - рекомендую темную
14) стаканчики для мочи лабораторные
15) щетки из бронзы и стали (колпачки для микрополировок)
16) оксид меди
17) Дополнительный воск для обработки поверхности
18) опционально - бригтенер
19) емкости для хранения раствора меди, напримерпосле минеральной воды
20) пластиковые ложки 9000 3
Начнем с приготовления раствора для гальванопластики. Пропорции на 1 литр дистиллированной воды.
Состав:
- 1 литр дистиллированной воды
- 240 г сульфата меди CuSO4
- 32 мл серной кислоты
- необязательно несколько капель осветлителя (но я не использую его, потому что люблю темные вещи)
Осторожно! Все работы с кислотой проводятся в защитном фартуке, очках и перчатках, также мы помним принцип, что кислоту всегда наливаем в воду, работаем в проветриваемом помещении.Емкости, в которых смешивается раствор, должны быть из стекла или химически стойкого пластика.
Налейте воду в большой сосуд, затем аккуратно влейте кислоту, помешивая. Температура раствора может повыситься или он может начать «дымиться», затем при перемешивании добавляют сульфат меди. Дожидаемся, пока все растворится и переливаем в емкость, в которой будем формировать медь. Вылейте остаток (если есть) в бутылку, подпишите бутылку и храните в темном прохладном месте.
Время для электродов. Электродом, который «отдает» медь в раствор, является анод. Подключаем его к "+" на блоке питания. Ионы меди положительны, поэтому, когда электрод подключен к «+», они уходят в раствор. Следовательно, этот электрод должен быть твердым, потому что со временем он начнет исчезать. Вот почему я использую медные газовые трубы, которые нарезаю по размеру, просверливаю и подключаю к обмоточному проводу без изоляции на концах. Благодаря этому у меня переваривается электрод, а не соединение электродов. Катод сделан из более толстой медной проволоки, на которую вешаем медные «крючки», подключаем обмоточный провод, а катод подключаем к «-» на блоке питания.

Следующим шагом будет изготовление токопроводящей краски. Вот чем нам пригодятся емкости с мочой ;-). Насыпьте в емкость пару столовых ложек порошкообразного графита (графит является проводником и обеспечит проводимость краски) и добавьте такое же количество акриловой краски. Тщательно перемешиваем. Добавьте столовую ложку дистиллированной воды и перемешайте, пока все не смешается. У нас должна получиться масса плотностью сметаны. Мы рисуем, погружая кисть в дистиллированную воду, и таким образом контролируем толщину краски: она должна быть тоньше для листьев, желудей, семян и более плотной для камней.Рекомендую работать в перчатках, акриловую краску после высыхания сложно смыть, а графит очень грязный.

Покроем медью: сушеный лист гинкго, два желудя, горный хрусталь. Первым делом приклеиваем медные держатели. У горного хрусталя появятся глазки из медной плетеной проволоки, на желуди - медные кольца, а на листе - петля.

Закрепите хрусталь и желуди, например,в тисках. Сверху нанести небольшое количество клея, наклеить на него медные кружочки и подождать, пока он слипнется. Следующим шагом будет укрепление стыка (желуди) и изготовление медной основы на кристалле. Для этого покроем клей пищевой содой. Наносим новый слой клея на стык медь-желуди и сразу же сбрызгиваем пищевой содой. Затем образуется очень твердая и прочная масса. В случае с кристаллом покрываем сверху приклеенную петельку клеем и сразу же сбрызгиваем, затем покрываем боковые фрагменты.

Очень аккуратно приклеиваем петлю к листу гинкго (желательно слегка расплющить молотком), хвостом по стеблю листа, когда клей высохнет, нанести новый слой, разложить и сбрызнуть пищевой содой. Стык должен затвердеть, поэтому у нас перерыв 2-3 часа.

Теперь мы можем покрыть все электропроводящей краской. Мы будем использовать более плотный кристалл для кристалла и более тонкий лист и желудь для листа. В случае с кристаллом красим только слой клей-натрий + медь, в случае желудей и листьев - целиком, потому что покрываем весь объект.Раскрасьте лист на листе бумаги сначала с одной стороны, дождитесь высыхания, затем - с другой. После покраски лучше всего оставить вещи на 12 часов, чтобы краска высохла.

Рекомендую гальванопластику и отдельно камни. Дело в том, что в случае листьев и т. Д. Ток должен быть ниже, чтобы ионы меди могли оседать на листьях, воссоздавая их структуру, в случае камней мы можем позволить себе более высокий ток, тогда медь растет более хаотично, создавая интересные формы.

Поместите лист и желуди в емкость для гальванопластики. Если сосуд уже заполнен раствором, то, конечно, листья и желуди всплывут наверх и не будут погружены в раствор. Способ сделать это прост - вы должны погрузить их так глубоко, чтобы даже после того, как они всплыли, они оставались под поверхностью. Включаем ток - обычно выставляю 0,2 А и жду. Через час у нас должны быть те же эффекты, что и на фото. Я обычно оставляю листья и т. Д. В растворе примерно на 24 часа при небольшом течении.

Конечно, может и будет так, что листья / желуди не будут очень точно покрыты медью. Не беспокойтесь об этом, просто выньте его из раствора, промойте в дистиллированной воде, тщательно просушите, покройте токопроводящей краской, дайте краске высохнуть и снова поместите ее в раствор и сформируйте медь с низким током.
Пока листья и желуди сохнут после второго слоя, можно начинать добычу кристалла. Вешаем на крючок и опускаем в раствор.Мы начинаем с малого тока, то есть 0,2 А, когда крышки из содового клея покрыты медью, мы можем увеличить ток и вырастить удивительные медные структуры.

Когда мы успешно покрыли все медью и медь вырастет, как нужно, пришло время для окончательной обработки. Полировка стальными / бронзовыми щетками - на ваше усмотрение .. И снова из соображений безопасности рекомендую работать в очках или, как я, специальной полировальной станцией (деревянный ящик с прозрачными стенками: сверху и спереди и отверстиями для рук. боковые стенки - дизайн и исполнение - муж).

После полировки можно окислить, покрыть патиной или оставить медь… медного цвета. Я обычно окисляю, ополаскиваю, тщательно сушу, немного полирую, а затем покрываю небольшим количеством защитного воска.

И это, наверное, почти все. Что дальше? Желаю вам много веселья. И внимание к одежде - мои футболки и рабочие брюки стали ажурными, потому что я забыла о защитной одежде.


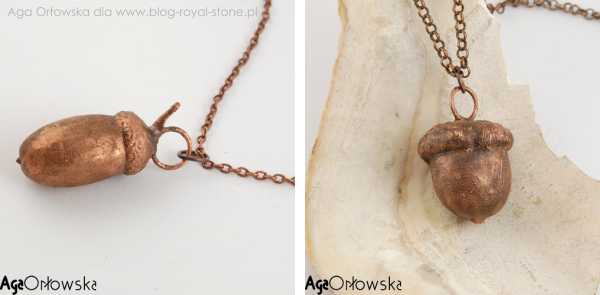
Может ли стальной гвоздь быть медным?
Металлические предметы можно покрыть тонким слоем другого металла. Этот процесс называется гальваникой. Гальваника использует электрохимические явления, сопровождающие прохождение тока между электродами, помещенными в гальваническую ванну.
Примером гальваники является химическое меднение, процесс покрытия металла медью без использования внешнего источника питания.
Это текущее меднение без электричества. В этом процессе используется явление вытеснения «более благородных» металлов «менее благородными» металлами.
В случае меднения предметов из железа или стали, погруженных в раствор соли меди, например сульфата меди, на поверхность чугуна или стали наносится медное покрытие. В результате химического меднения образуются очень тонкие покрытия.Химическое меднение подходит только для нанесения декоративных покрытий, поэтому в технологических процессах оно не используется повсеместно.
Это меднение можно сделать в домашних условиях. Попробуйте провести такой эксперимент.
Вам понадобится:

Налейте в банку полстакана воды и добавьте 1 пакетик лимонной кислоты (20 г), сделайте раствор, т.е. тщательно перемешайте.В готовый раствор опустить медные элементы и оставить примерно на 1 час.

За это время подготовьте ноготь: тщательно очистите его наждачной бумагой, тщательно вымойте с мылом и ополосните, чтобы удалить загрязнения (этот процесс называется обезжириванием).
Удалите медные предметы из раствора лимонной кислоты.
Обратите внимание, что изделия из меди теперь идеально чистые и блестящие! Теперь поместите подготовленный ноготь в тот же раствор.

Оставляем ноготь в растворе на несколько часов, и за это время наблюдаем, что происходит с нашим ногтем.

Через полчаса видно, что ноготь меняет цвет.
Во время эксперимента частицы меди переходили в раствор лимонной кислоты и становились электрически заряженными, затем оседали на поверхности железа и прочно связывались с ней.В результате получается тонкий слой коричневого налета, состоящий из чистой меди, хотя он немного похож на ржавчину.

Способность тонировать один металл поверх другого также была полезна в старые времена, особенно преступникам и фальшивомонетчикам.
Такое тонкое покрытие может быть выполнено из различных металлов, например хрома, цинка, золота, серебра.
В настоящее время украшения, скульптуры и чашки позолочены, а хромированный смеситель не только не ржавеет, но и сияет, как зеркало.
Удачных экспериментов!
Драгоценность Виолетты
.