Водород – самый распространенный элемент во Вселенной. Человечеству он был известен достаточно давно, но активное применение и разработка технологий с использованием этого газа начались лишь несколько десятилетий назад. Газ водород активно используется в самых разных областях промышленности, а в перспективе еще и в энергетике.
Поскольку как химический элемент водород был известен достаточно давно, то однозначного первооткрывателя установить невозможно. В истории сохранилось не так много записей и документов, которые могли бы дать ответ. Алхимики еще в 14-15 веках наблюдали в ходе определенных химических реакций выделение загадочного «горючего» газа, но еще не выделяли водород как отдельную составляющую.
Первые упоминания в научных работах датируются 1766 годом. Британский химик и физик Генри Кавендиш сумел выделить из кислот водород, после чего собрал газ в отдельной камере и поджег. В ходе этого эксперимента была получена вода. Также Кавендиш попытался определить массу водорода, что ему удалось сделать лишь с небольшой погрешностью.
Окончательное открытие признают за французом Антуаном Лавуазье, который с 1774 года также занимался исследованиями «горючего воздуха». В ходе своих опытов ему удалось определить, что в ходе синтеза водорода и кислорода получается именно вода, молекулярное соединение. Считается, что именно Лавуазье дал название элементу «hydrogene», от греческого «рождающий воду».
А вот русское название химическому элементу выдал Михаил Соловьёв в 1824 по аналогии с «кислород».
Что такое водород — это самый легкий элемент в химической таблице, поэтому занимает почетное первое место. Его ядро включает всего один протон и один нейтрон. Несмотря на повсеместное распространение во вселенной, в земной коре содержится всего около 1%.

Встречается элемент на Земле чаще всего в виде соединений с другими элементами. Реже в виде двухатомного газа h3, состоящего из пары атомов. В обычных условиях – это бесцветный, нетоксичный газ без какого-либо цвета и вкуса. В смесях с воздухом, кислородом, хлором или фтором при определенной концентрации может быть взрывоопасен.
Температура кипения составляет -252,87°С, а при -259,14°С происходит плавление. Наиболее распространенные соединения с водородом – это вода (Н2О), аммиак (Nh4), сероводород (Н2S), метан (Ch5), гидриды металлов и некоторые органические соединения.
Уникальные свойства этого газа быстро нашли применение в нескольких сферах, в частности, в военной. В 18 веке воздушная техника сводилась к шарам и дирижаблям. Наполняли емкости горячим воздухом, благодаря которому вся конструкция могла взлетать. Проблемой было то, что воздух требовалось поддерживать горячим, иначе он терял свою подъемную способность.
Газ водород в этом плане был намного выгоднее – он всегда оставался легче воздуха, но наоборот требовал повышенной защиты от огня. Почему не использовали гелий? На тот момент производство этого газа было непомерно дорогим, поэтому о наполнении таких больших объемов как в дирижаблях речи не шло. Сегодня же гелий куда более доступный и активно используется в самых разных сферах.

История дирижаблей на водороде ассоциируется с именем Фердинанда фон Цеппелина, который создал модели LZ-1, LZ-2 и LZ-3. Последнюю заметили военные, после чего эти воздушные суда начали активно использоваться в военных действиях в ходе Первой мировой войны, а также в пассажирских перевозках. Дирижабли без особых проблем могли совершать длительные полеты, в том числе через Атлантический океан.
Водород не только подарил новую жизнь воздушным судам, но и стал причинной их гибели. Газ легко воспламенялся, из-за чего каждый дирижабль фактически становился потенциальной бомбой. Конец эры этих монстров датируется 1937 годом, когда в США загорелся и рухнул дирижабль «Гинденбург».
В космосе над всеми элементами преобладает водород, однако на Земле встретить его в свободном виде практически невозможно. В связи с этим существует несколько разнообразных технологий получения этого газа, каждая из которых имеет свои особенности.

В лабораторных условиях нередко пользуются древним способом – получая газ из кислот. Пример, взаимодействие серной кислоты и цинка, в ходе которого выделяется h3. В качестве металлов могут подойти и другие, например, алюминий. Однако полученный газ требуется еще дополнительно очистить.
В промышленных масштабах часто используется метод паровой конверсии с метаном или природным газом. В ходе сложных контролируемых химических реакций удается получить относительно чистый газ водород. После с помощью угольных фильтров достигается концентрация в 99,9%. Такой подход требует наличия крупных установок, но считается одним из самых эффективных.
В местах с дешевым электричеством может использоваться электролиз – разложение воды на водород и кислород. В воду добавляется небольшое количество солей, чтобы жидкость смогла проводить электричество. Технология позволяет получить не только водород, но и кислород, который также имеет большое значение в промышленном производстве. Единственный недостаток – большие затраты электроэнергии.

Среди других методов стоит отметить газификацию угля. Методика из-за доступности сырья успешно конкурирует с другими способами, но вызывает вопросы с точки зрения экологичности. Газификация сопровождается ощутимыми выбросами углекислого газа, из-за чего производства могут попадать под санкции.
Нередко можно встретить разработки по получению водорода в ходе разложения органических или неорганических веществ. Например, компания Ways2H предлагает специальную технологию утилизации бытовых отходов, в ходе которой без сгорания можно получить водород. По заявлениям представителей фирмы, с одной тонны сухих отходов вырабатывается от 30 до 150 килограмм водорода. Однако все подобные проекты пока находятся либо на стадии экспериментов, любо работают только на небольших тестовых площадках.
С развитием технологий и возможностью получать газ в больших масштабах началось широкое применение водорода в самых разных областях:
Есть и более бытовое применение, знакомое каждому – перекись водорода. Этот состав также используют при отбеливании.
Водород активно применяется в качестве защитного газа при сварке. Процесс сварки неотъемлемо связан с целым списком технических газов, в чем вы можете убедиться лично в статьях соответствующего раздела.
Как известно, кислород оказывает неблагоприятный эффект на сварной шов, понижая его прочность. Решением этой проблемы стали защитные газы, которые не допускают попадания воздуха в зону горения дуги. В число активных защитных газов как раз и входит водород. Применение этого газа в качестве защитного имеет несколько плюсов: равномерное проплавление ванны, возможность создания аккуратного шва, высокая защита от большинства окислительных процессов.
Однако при водородной сварке предъявляются высокие требования к напряжению источника тока. Также применение водорода в качестве защитного газа может стать причиной появления пор в металле и холодных трещин. В плазменной сварке уже необходимо применение аргоно-водородной смеси с концентрацией последнего до 20%.
Баллоны с водородом изготавливают из углеродистой стали по ГОСТу 949 и окрашивают в зеленый цвет с красными надписями. Подробнее про металлические баллоны вы можете узнать здесь.
При работе с водородом необходимо особое внимание уделять герметичности оборудования. Как говорилось ранее, газ при контакте с воздухом образует взрывоопасную смесь. Пределы взрываемости колеблются от 4 до 75%. При высокой концентрации газ также способен вызвать удушье, поэтому перед началом работы необходимо ознакомиться с соответствующими правилами.
Проблемы экологии вынуждают исследователей искать альтернативные источники энергии. Один из самых животрепещущих вопросов последних лет – водород в качестве автомобильного топлива. Главный плюс – отсутствие выброса вредных газов в атмосферу. В цилиндр двигателя поступает водород и кислород, которые в ходе реакции создают небольшой взрыв и двигают поршни. Побочный продукт в ходе этой реакции – обычная вода. Также выпускаются машины на электротяге, но с водородными ячейками, внутри которых формируется электрическая энергия при взаимодействии h3 и О2.

Крупные автопроизводители постепенно осваивают технологию на прототипах или тестовых машинах. Например, уже были выпущены и протестированы такие модели, как BMW Hydrogen 7, Mazda RX-8 Hydrogen RE, а также автобусы Ford E-450 для аэропортов. Самым популярным и известным автомобилем на водороде можно назвать Toyota Mirai, которая активно продается на территории США, Канады и Японии. Во многом популярность этой модели обоснована дотациями со стороны государства. Например, в США при покупке Mirai вы получали дополнительно 15 тысяч долларов на заправку водородом в течение трех лет.
Видео о водородной энергетике
Схожие предложения есть и от других компаний — Honda Clarity, Hyundai Nexo, Mercedes—Benz GLC F-Cell, BMW X5i Hydrogen Next.
Несмотря на все достоинства водородной технологии, есть несколько важных «но». Во-первых, имеется масса вопросов относительно безопасности водорода в автомобильном транспорте. В отличие от бензина, водород легко может взорваться при контакте с воздухом, поэтому даже незначительные ДТП на дороге представляют опасность. Это вынуждает автопроизводителей устанавливать дополнительные датчики и делать баки более ударопрочными.
Во-вторых, в мире образовалась проблема «яйца и курицы». Машины на водороде не появляются из-за отсутствия инфраструктуры, а ее не хотят возводить из-за небольшого количества машин. Разорвать этот замкнутый круг становится сложнее, учитывая конкуренцию со стороны электромобилей. По данным за 2020 год в мире насчитывается около 500 водородных заправок, в то время как станций для зарядки авто – больше 11 миллионов!
Несмотря на эти ограничения, многие уверены, что водород станет неотъемлемой частью энергетики будущего, так же, как он используется сейчас в пищевой и химической промышленности.
А больше информации о нашей компании вы найдете на сайте https://idealgaz.ru/.
МОСКВА, 29 апр — ПРАЙМ. Страны Европы ждет холодная и темная зима, но есть способы исправить ситуацию, пишет обозреватель FT.
По его мнению, "самый дешевый и быстрый" способ пережить зиму — перестать пользоваться газом, поставляемым Россией. Однако, для этого жителям Европы придется пойти на некоторые жертвы.
Европейские политики должны сделать экономию энергии национальным приоритетом и поставить во главу угла.
"Решение Владимира Путина прекратить поставки газа в Польшу и Болгарию стало предупредительным сигналом для стран Запада. Европу ждет холодная и темная зима, если все те, кто заодно с Украиной, не начнут экономить газ. Это даст европейским странам возможность освободиться от российской энергетической удавки", — переводит текст статьи ИноСМИ.
Не отменяя важность разработки планов по закупке газа у других поставщиков, по наращиванию сырьевых запасов в летний период, а также ускорение проектов ветровой и солнечной энергетики и по термоизоляции домов, самый быстрый и самый дешевый способ снизить зависимость от российских поставок — это просто меньше его расходовать.
Именно это является беспроигрышным способом решения наших сегодняшних энергетических проблем. "Если зимой понизить температуру в наших помещениях, это приведет к снижению рыночных цен, лишит Россию твердой валюты, увеличит запасы доступного для Европы газа в дружественных странах и немного поможет с решением проблем климатических изменений", считает автор.
Снижение температуры в домах по всей Европе с 20 до 18 градусов приведет к сокращению потребления на 20-25%, пишет он со ссылкой на подсчеты консалтинговой фирмы Cambridge Energy.
"Добиться такой экономии за счет повышения эффективности определенно возможно. Например, за 40 лет с 1971 по 2011 год средняя температура в британских домах в зимнее время поднялась на пять градусов. Но ведь мы можем надеть теплую одежду, воспользоваться одеялами и купить куртки с подогревом от аккумуляторов. Мерзнуть не придется", — призывает издание.
Полный текст статьи читайте на сайте ИноСМИ >>
В таблице приведена плотность газов и паров при нормальных условиях – температуре 0°С и нормальном атмосферном давлении (760 мм. рт. ст.). Для некоторых газов, например газа стибина, плотность дана при температуре 15°С и давлении 754 мм. рт. ст.
Значение плотности газов в таблице указано в размерности кг/м3 для следующих газов и паров: азот N2, аммиак NH3, аргон Ar, ацетилен C2H2, бор фтористый BF3, бутан C4H10, водород: бромистый HBr, йодистый HI, мышьяковистый H3As, селенистый H2Se, сернистый H2S, теллуристый H2Te, фосфористый H3P, хлористый HCl, воздух, гелий He, германия тетрагидрид GeH4, диметиламин (CH3)2NH, дифтордихлорметан CF2Cl2, дициан C2N2, закись азота N2O, кислород O2, кремний фтористый SiF4, гексагидрид Si2H6, тетрагидрид SiH4, криптон Kr, ксенон Xe, метан CH4, метиленхлорид CH3Cl, метиламин CH5N, метиловый эфир C2H6O, метилфторид CH3F, метилхлорид CH3Cl, мышьяк фтористый AsF5, неон Ne, нитрозил фтористый NOF и хлористый NOCl, озон O3, окись азота NO, пропан C3H8, пропилен C3H6, радон Rn, двуокись серы SO2 и гексафторид серы SF2, силан диметил SiH2(CH3)2, метил SiH3CH3, хлористый SIH3Cl, трифтористый SiHF3, стибин SbH3, сульфурил фтористый SO2F2, триметиламин (CH3)3N, триметилбор (CH3)3B, двуокись углерода CO2, окись углерода CO, сероокись COS, фосфор фтористый PF2, оксифторид POF3, пентафторид PF5, фтор F2, фторокись азота NO2, двуокись хлора ClO2, окись хлора Cl2O, хлорокись азота NO2Cl, этан C2H6, этилен C2H4, окись азота NO.
Плотность газов вычисляется, как отношение молярной массы газа к его молярному объему, который при 0°С и давлении 1 атм. равен 22,4 л/моль.
Следует отметить, что самым легким газом является водород — плотность этого газа при нормальных условиях равна 0,0899 кг/м3. Для удобства восприятия плотность газов приводят именно к плотности водорода, используя при этом относительную плотность по водороду. Например, относительная плотность газа азота N2 по водороду равна 13,9.
Наибольшую плотность имеет газ радон. Этот радиоактивный газ имеет плотность при нормальных условиях 9,73 кг/м3, а его относительная плотность по водороду составляет величину 108,2.
Необходимо отметить, что при увеличении давления газов и паров, их плотность увеличивается пропорционально.
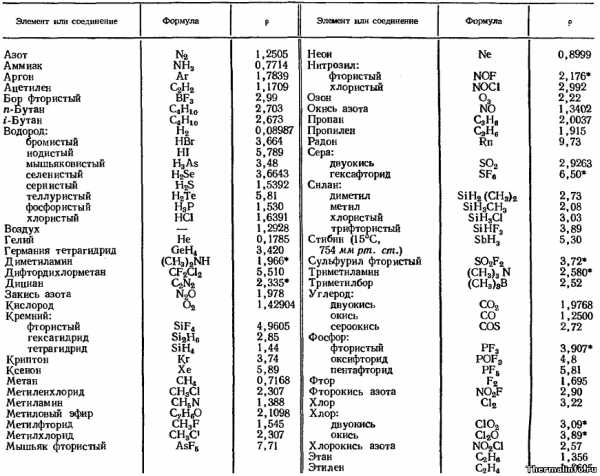
Примечание: Для газов и паров, рядом со значением плотности которых, присутствует символ *, ее величина в таблице приведена при температуре 20°С.
Из анализа данных, представленных в таблице, видно, что плотность рассмотренных газов находится в диапазоне от 0,089 до 9,73 кг/м3.
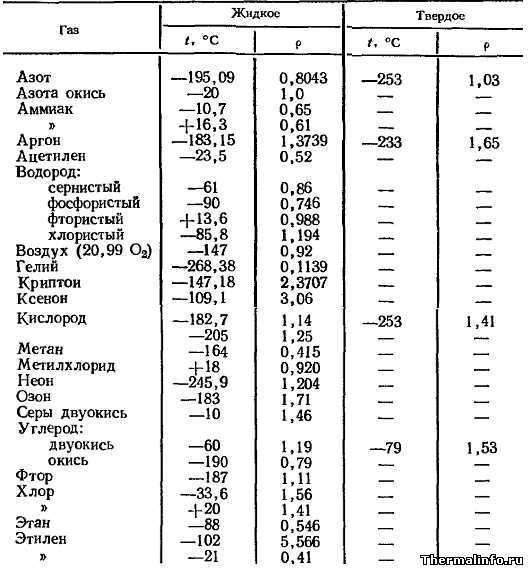
Значения плотности газов и паров в жидком и твердом состояниях приведены в таблице в зависимости от температуры при нормальном атмосферном давлении. Величина плотности газов указана в основном при низких температурах (в интервале от -268 до 20°С), при которых они находятся в жидком, или твердом состояниях.
При низких температурах плотность некоторых газов сравнима с плотностью металлов. К плотным (тяжелым) газам в жидком состоянии можно отнести такие газы, как этилен, криптон (плотность 2371 кг/м3) и ксенон (плотность 3060 кг/м3). Например, плотность газа этилена при температуре -102°С имеет значение 5566 кг/м3, что почти в полтора раза больше плотности алюминия. При этом этилен находится в жидком состоянии.
Газы в твердом состоянии имеют плотность немногим больше, чем в жидком. Твердое состояние газа достигается при более низкой температуре.
Например, углекислый газ находится в виде жидкости при температуре -60°С (при атмосферном давлении), но уже при -79°С становиться твердым и имеет плотность 1530 кг/м3.
Плотность газов в таблице дана в т/м3и приведена для следующих газов: азот N2, окись азота NO, аммиак NH3, аргон Ar, ацетилен C2H2, водород: сернистый H2S, фосфористый H3P, фтористый HF, хлористый HCl, воздух, гелий He, криптон Kr, ксенон Xe, кислород O2, метан CH4, метилхлорид CH3Cl, неон Ne, озон O3, сера двуокись SO2, углерод: двуокись CO2, окись CO, фтор F2, хлор Cl2, этан C2H6, этилен C2H4.
 Источник:
Источник:
Таблицы физических величин. Справочник. Под ред. акад. И.К. Кикоина. М.: Атомиздат, 1976. — 1008 с.
| Водород | |
|---|---|
| Атомный номер | 1 |
| Внешний вид простого вещества | газ без цвета, вкуса и запаха |
| Свойства атома | |
|
Атомная масса (молярная масса) |
1,00794 а.е.м. (г/моль) |
| Радиус атома | 79 пм |
|
Энергия ионизации (первый электрон) |
1311,3 кДж/моль (эВ) |
| Электронная конфигурация | 1s1 |
| Химические свойства | |
| Ковалентный радиус | 32 пм |
| Радиус иона | 54 (−1 e) пм |
|
Электроотрицательность (по Полингу) |
2,20 |
| Электродный потенциал | |
| Степени окисления | 1, −1 |
| Термодинамические свойства простого вещества | |
|
Плотность вещества |
0,0000899 (при 273K (0 °C)) г/см³ |
| Молярная теплоёмкость | 14,235 Дж/(K·моль) |
| Теплопроводность | 0,1815 Вт/(м·K) |
| Температура плавления | 14,01K |
| Теплота плавления | 0,117 кДж/моль |
| Температура кипения | 20,28K |
| Теплота испарения | 0,904 кДж/моль |
| Молярный объём | 14,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | гексагональная |
| Параметры решётки | a=3,780 c=6,167 Å |
| Отношение c/a | 1,631 |
| Температура Дебая | 110 K |
| H | 1 |
| 1,00794 | |
| 1s1 | |
| Водород | |
Водород является первым элементом периодической системы элементов. Широко распространён в природе. Катион (и ядро) самого распространённого изотопа водорода 1H— протон. Свойства ядра 1H позволяют широко использовать ЯМР-спектроскопию в анализе органических веществ.
Трое из пяти изотопов водорода имеют собственные названия: 1H— протий (Н), 2H— дейтерий (D) и 3H— тритий (радиоактивен) (T).
Простое вещество водород— H2— лёгкий бесцветный газ. В смеси с воздухом или кислородом горюч и взрывоопасен. Нетоксичен. Растворим в этаноле и ряде металлов: железе, никеле, палладии, платине.
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре становления химии как науки. Прямо указывал на выделение его и М. В. Ломоносов, но уже определённо сознавая, что это не флогистон. Английский физик и химик Г. Кавендиш в 1766 году исследовал этот газ и назвал его «горючим воздухом». При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона помешала ему сделать правильные выводы. Французский химик А. Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, в 1783г. осуществил синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Таким образом он установил, что «горючий воздух» входит в состав воды и может быть из неё получен.
Лавуазье дал водороду название hydrogène (отὕδωρ— «вода» и γενναω— «рождаю»)— «рождающий воду». Русское наименование «водород» предложил химик М.Ф.Соловьев в 1824 году— по аналогии с ломоносовским «кислородом».
Водород — самый распространённый элемент во Вселенной. На его долю приходится около 92% всех атомов (8% составляют атомы гелия, доля всех остальных вместе взятых элементов — менее 0,1%). Таким образом, водород — основная составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца ~6000 °C) водород существует в виде плазмы, в межзвёздном пространстве этот элемент существует в виде отдельных молекул, атомов и ионов и может образовывать молекулярные облака, значительно различающиеся по размерам, плотности и температуре.
Массовая доля водорода в земной коре составляет 1%— это десятый по распространённости элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет 17% (второе место после кислорода, доля атомов которого равна ~52%). Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода. В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в атмосфере (0,00005% по объёму).
Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках. В живых клетках по числу атомов на водород приходится почти 50%.
Промышленные способы получения простых веществ зависят от того, в каком виде соответствующий элемент находится в природе, то есть что может быть сырьём для его получения. Так, кислород, имеющийся в свободном состоянии, получают физическим способом— выделением из жидкого воздуха. Водород же практически весь находится в виде соединений, поэтому для его получения применяют химические методы. В частности, могут быть использованы реакции разложения. Одним из способов получения водорода служит реакция разложения воды электрическим током.
Основной промышленный способ получения водорода— реакция с водой метана, который входит в состав природного газа. Она проводится при высокой температуре (легко убедиться, что при пропускании метана даже через кипящую воду никакой реакции не происходит):
СН4 +2Н2O =CO2↑ +4Н2 −165 кДж
В лаборатории для получения простых веществ используют не обязательно природное сырьё, а выбирают те исходные вещества, из которых легче выделить необходимое вещество. Например, в лаборатории кислород не получают из воздуха. Это же относится и к получению водорода. Один из лабораторных способов получения водорода, который иногда применяется и в промышленности,— разложение воды электротоком.
Обычно в лаборатории водород получают взаимодействием цинка с соляной кислотой.
1.Электролиз водных растворов солей:
2NaCl +2H2O → H2↑ +2NaOH +Cl2
2.Пропускание паров воды над раскаленным коксом при температуре около 1000°C:
H2O +C ⇄ H2↑ +CO↑
3.Из природного газа.
Конверсия с водяным паром:
CH4 +H2O ⇄ CO↑ +3H2↑ (1000°C)
Каталитическое окисление кислородом:
2CH4 +O2 ⇄ 2CO↑ +4H2↑
4. Крекинг и риформинг углеводородов в процессе переработки нефти.
1.Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную соляную кислоту:
Zn +2HCl → ZnCl2 +H2↑
2.Взаимодействие кальция с водой:|
Ca +2H2O → Ca(OH)2 +H2↑
3.Гидролиз гидридов:
NaH +H2O → NaOH +H2↑
4.Действие щелочей на цинк или алюминий:
2Al +2NaOH +6H2O → 2Na[Al(OH)4] +3H2↑
Zn +2KOH +2H2O → K2[Zn(OH)4] +H2↑
5.С помощью электролиза. При электролизе водных растворов щелочей или кислот на катоде происходит выделение водорода, например:
2H3O+ +2e- → H2↑ +2H2O
Биореактор для производства водорода
Спектр излучения водорода
Эмиссионный спектр водорода
Равновесная мольная концентрация пара-водорода
Разделить модификации водорода можно адсорбцией на активном угле при температуре жидкого азота. При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону последнего. При 80 К соотношение форм приблизительно 1:1. Десорбированный параводород при нагревании превращается в ортоводород вплоть до образования равновесной при комнатной температуре смеси (орто-пара: 75:25). Без катализатора превращение происходит медленно (в условиях межзвездной среды— с характерными временами вплоть до космологических), что даёт возможность изучить свойства отдельных модификаций.
Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н2. При нормальных условиях — это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н.у.), температура кипения −252,76 °C, удельная теплота сгорания 120.9·106 Дж/кг, малорастворим в воде — 18,8 мл/л. Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов на 1объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
Фазовая диаграмма водорода
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая (плотность при −253 °C 0,0708 г/см3) и текучая (вязкость при −253 °C 13,8 спуаз). Критические параметры водорода очень низкие: температура −240,2 °C и давление 12,8 атм. Этим объясняются трудности при ожижении водорода. В жидком состоянии равновесный водород состоит из 99,79% пара-Н2, 0,21% орто-Н2.
Твердый водород, температура плавления −259,2 °C, плотность 0,0807 г/см3 (при −262 °C) — снегоподобная масса, кристаллы гексогональной сингонии, пространственная группа P6/mmc, параметры ячейки a=3,75 c=6,12. При высоком давлении водород переходит в металлическое состояние.
Давление пара для различных изотопов водорода
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1H— протий (Н), 2Н— дейтерий (D), 3Н— тритий (радиоактивный) (T).
Протий и дейтерий являются стабильными изотопами с массовыми числами 1и 2. Содержание их в природе соответственно составляет 99,9885±0,0070% и 0,0115 ± 0,0070%. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода.
Изотоп водорода 3Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет. Тритий содержится в природе в очень малых количествах.
В литературе также приводятся данные об изотопах водорода с массовыми числами 4— 7и периодами полураспада 10−22— 10−23 с.
Природный водород состоит из молекул H2 и HD (дейтероводород) в соотношении 3200:1. Содержание чистого дейтерийного водорода D2 ещё меньше. Отношение концентраций HD и D2, примерно, 6400:1.
Из всех изотопов химических элементов физические и химические свойства изотопов водорода отличаются друг от друга наиболее сильно. Это связано с наибольшим относительным изменением масс атомов.
|
Температура плавления, K |
Температура кипения, K |
Тройная точка, K /kPa |
Критическая точка, K /kPa |
Плотность жидкий /газ, кг/м³ |
|
|---|---|---|---|---|---|
| H2 | 13.95 | 20,39 | 13,96 /7,3 | 32,98 /1,31 | 70,811 /1,316 |
| HD | 16,60 | 22,13 | 16,60 /12,8 | 35,91 /1,48 | 114,80 /1,802 |
| HT | 22,92 | 17,63 /17,7 | 37,13 /1,57 | 158,62 /2,310 | |
| D2 | 18,62 | 23,67 | 18,73 /17,1 | 38,35 /1,67 | 162,50 /2,230 |
| DT | 24.38 | 19,71 /19,4 | 39,42 /1,77 | 211,54 /2,694 | |
| T2 | 25,04 | 20,62 /21,6 | 40,44 /1,85 | 260,17 /3,136 |
Дейтерий и тритий также имеют орто- и пара- модификации: p-D2, o-D2, p-T2, o-T2. Гетероизотопный водород (HD, HT, DT) не имеют орто- и пара- модификаций.
Доля диссоциировавших молекул водорода
Молекулы водорода Н2 довольно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция:
и с единственным неметаллом— фтором, образуя фтороводород:
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении:
Он может «отнимать» кислород от некоторых оксидов, например:
Записанное уравнение отражает восстановительные свойства водорода.
С галогенами образует галогеноводороды:
С сажей взаимодействует при сильном нагревании:
При взаимодействии с активными металлами водород образует гидриды:
Гидриды— солеобразные, твёрдые вещества, легко гидролизуются:
Оксиды восстанавливаются до металлов:
Молекулярный водород широко применяется в органическом синтезе для восстановления органических соединений. Эти процессы навзывают реакциями гидрирования. Эти реакции проводят в присутствии катализатора при повышенных давлении и температуре. Катализатор может быть как гомогенным (напр. Катализатор Уилкинсона), так и гетерогенным (напр. никель Ренея, палладий на угле).
Так, в частности, при каталитическом гидрировании ненасыщенных соединений, таких как алкены и алкины, образуются насыщенные соединения — алканы.
На Земле содержание водорода понижено по сравнению с Солнцем, гигантскими планетами и первичными метеоритами, из чего следует, что во время образования Земля была значительно дегазирована и водород вместе с другими летучими элементами покинул планету во время аккреции или вскоре после неё.
Свободный водород H2 относительно редко встречается в земных газах, но в виде воды он принимает исключительно важное участие в геохимических процессах.
В состав минералов водород может входить в виде иона аммония, гидроксил-иона и кристаллической воды.
В атмосфере водород непрерывно образуется в результате разложения воды солнечным излучением. Имея малую массу, молекулы водорода обладают высокой скоростью диффузионного движения (она близка ко второй космической скорости) и, попадая в верхние слои атмосферы, могут улететь в космическое пространство.
|
Водород при смеси с воздухом образует взрывоопасную смесь— так называемый гремучий газ. Наибольшую взрывоопасность этот газ имеет при объёмном отношении водорода и кислорода 2:1, или водорода и воздуха приближённо 2:5, так как в воздухе кислорода содержится примерно 21%. Также водород пожароопасен. Жидкий водород при попадании на кожу может вызвать сильное обморожение. Взрывоопасные концентрации водорода с кислородом возникают от 4% до 96% объёмных. При смеси с воздухом от 4% до 75(74)% объёмных. |
Атомарный водород используется для атомно-водородной сварки.
При производстве аммиака, метанола, мыла и пластмасс
При производстве маргарина из жидких растительных масел.
Зарегистрирован в качестве пищевой добавки E949 (упаковочный газ)
Водород очень лёгок и в воздухе всегда поднимается вверх. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XXв. произошло несколько катастроф, когда дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием.
Водород используют в качестве ракетного топлива. Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей. Водородные двигатели не загрязняют окружающей среды и выделяют только водяной пар.
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.
Водород, Hydrogenium, Н (1)
Как горючий (воспламеняемый) воздух водород известен довольно давно. Его получали действием кислот на металлы, наблюдали горение и взрывы гремучего газа Парацельс, Бойль, Лемери и другие ученые XVI— XVIII вв. С распространением теории флогистона некоторые химики пытались получить водород в качестве «свободного флогистона». В диссертации Ломоносова «О металлическом блеске» описано получение водорода действием «кислотных спиртов» (например, «соляного спирта», т. е. соляной кислоты) на железо и другие металлы; русский ученый первым (1745) выдвинул гипотезу, о том что водород («горючий пар»— vapor inflammabilis) представляет собой флогистон. Кавендиш, подробно исследовавший свойства водорода, выдвинул подобную же гипотезу в 1766 г. Он называл водород «воспламеняемым воздухом», полученным из «металлов» (Inflammable air from metals), и полагал, как и все флогистики, что при растворении в кислотах металл теряет свой флогистон. Лавуазье, занимавшийся в 1779 г. исследованием состава воды путем ее синтеза и разложения, назвал водород Hydrogine (гидроген), или Hydrogene (гидрожен), от греч. гидор— вода и гайноме— произвожу, рождаю.
Номенклатурная комиссия 1787 г. приняла словопроизводство Hydrogene от геннао, рождаю. В «Таблице простых тел» Лавуазье водород (Hydrogene) упомянут в числе пяти (свет, теплота, кислород, азот, водород) «простых тел, относящихся ко всем трем царствам природы и которые следует рассматривать как элементы тел»; в качестве старых синонимов названия Hydrogene Лавуазье называет горючий газ (Gaz inflammable), основание горючего газа. В русской химической литературе конца XVIII и начала XIX в. встречаются два рода названий водорода: флогистические (горючий газ, горючий воздух, воспламенительный воздух, загораемый воздух) и антифлогистические (водотвор, водотворное существо, водотворный гас, водородный гас, водород). Обе группы слов представляют собой переводы французских названий водорода.
Изотопы водорода были открыты в 30-x годах текущего столетия и быстро приобрели большое значение в науке и технике. В конце 1931 г. Юри, Брекуэдд и Мэрфи исследовали остаток после длительного выпаривания жидкого водорода и обнаружили в нем тяжелый водород с атомным весом 2. Этот изотоп назвали дейтерием (Deuterium, D) от греч.— другой, второй. Спустя четыре года в воде, подвергнутой длительному электролизу, был обнаружен еще более тяжелый изотоп водорода 3Н, который назвали тритием (Tritium, Т), от греч.— третий.
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА № 225
РЕФЕРАТ ПО ХИМИИ
Водород - самый легкий газ
Иванова А.А.
Проверил: учитель химии
Воронаев.И.Г
Оценка:
Санкт-Петербург 2018г.
1) Титульный лист.
2) Оглавление с нумерацией страниц.
3) Задачи.
4-5) Основная часть.
6) Заключение.
7) Список используемой литературы.
Задачи
В этой работе мы попытаемся узнать “Почему водород самый легкий газ?”. Мы узнаем историю открытия водорода, водород как химический элемент, водород как простое вещество, физические свойства водорода, и интересные факты.
Атом водорода самый легкий, самый простой по строению и один из самых маленьких по размерам. Относительная атомная масса водорода равна:
Атомы водорода соединяются с атомами других химических элементов, образуя сложные вещества. Как химический элемент водород входит в состав воды, кислот, природного газа, нефти, глюкозы и многих других веществ. В растительных и животных организмах, включая и человеческий, химический элемент водород содержится в составе воды и самых разнообразных органических веществ.
Молекулы водорода образованы двумя атомами химического элемента водорода. В виде простого вещества водород встречается на Земле лишь в небольшом количестве в вулканических и некоторых других природных газах. Молекулы водорода Н2 обнаружены в верхних слоях земной атмосферы. В Солнечной системе простое вещество водород входит в состав атмосферы планет — Юпитера, Сатурна, Урана.
 .
.
Еще в XVI в. Парацельсом было замечено, что при действии кислот на железо и другие металлы выделяется газ. Первоначально его назвали «горючим воздухом». Спустя примерно 100 лет горение водорода на воздухе описал Р. Бойль и этот газ научились собирать. Во второй половине XVIII в. английский ученый Г. Кавендиш подробно исследовал свойства «горючего воздуха». Он установил, что этот газ при сгорании на воздухе образует воду. 
Физические свойства водорода и интересные факты
-Водород при нормальных условиях находится в газообразном состоянии. Это бесцветный газ, у которого нет запаха и вкуса.
-У водорода самые низкие после благородного газа гелия температуры кипения (−252,8 °С) и плавления (−259,2 °С).
-Молекула водорода самая легкая из молекул всех веществ. Поэтому газообразный водород по плотности значительно уступает воздуху и кислороду.
-Водород реагирует с оксидами малоактивных металлов, причем он способен восстанавливать только металлы, стоящие в ряду активности правее цинка.
-Водород-наиболее распространенный элемент во Вселенной
-Водород не имеет цвета, запаха и вкуса
-Водород мало растворяется в воде и его можно собирать методом вытеснения воды и воздуха
-Смесь водорода и воздуха опасна
Вывод
-Водород получали многие ученые, но первооткрывателем считают Генри Кавендиша.
-Название водорода гидрогениум (от греческого “рождают воду”)
-Молекула водорода состоит из двух атомов
Я узнала, что водород легкий газ, но его нельзя использовать для наполнения шаров потому, что водород легковоспламеняемый газ, который может взорваться и сжечь в любую минуту.
И ранее водород использовался в воздухоплавании, но в виду высокой взрывоопасности смеси водорода с кислородом и нескольких крупных аварий от широкого использования водорода отказались.
Список используемой литературы
http://ru.solverbook.com/spravochnik/svojstva-po-ximii/fizicheskie-i-ximicheskie-svojstva-vodoroda/
https://himi4ka.ru/arhiv-urokov/urok-21-vodorod-samyj-ljogkij-gaz.html
декабря 14, 2010
Первый элемент
Самый легкий газ - это водород, самый распространённый элемент во Вселенной. Почти 92% всех существующих атомов приходится на водород. Это первый элемент в периодической таблице Д. И. Менделеева. Его атомный № - 1, атомная масса равна 1,0079. Водород открыт в 1766 г английским химиком Г. Кавендишем. Масса 1000 миллилитров Водорода в газообразном состоянии набирает всего 0,08988 граммов. Сам воздух, в состав которого входит водород, 14,5 раз тяжелее.
Молекулы водорода, как самые легкие, движутся быстрее молекул всякого иного газа, и обладают высочайшей теплопроводностью среди всех газообразных материй. Его теплоотдача приблизительно в семь раз превышает теплопроводности воздуха. Водород быстрее, полнее и с меньшими потерями, передает теплоту от одного вещества к другому. Он находится в составе всех органических веществ и есть во всех живых клетках, при этом, на его долю приходится почти 50%.
В жидком состоянии водород - самая лёгкая жидкость в мире.
Подробне о водороде
Водород имеет только один электрон, который, проявляет свойство галогенов - образуя гидриды, и свойства щелочных металлов - образуя галоген водороды.
Рассказывая о Водороде нельзя не упомянуть о гелии. Ведь Солнце – «светящийся шар» ,представляющий с собой смесь Водорода и Гелия в пропорции 4:1. И, если Водород представляет с собой ядерное топливо Солнца, то гелий есть его ядерный «пепел». Ежесекундная потеря Солнцем определенной массы - это потеря массы в результате превращения Водорода в Гелий. То есть, каждую секунду определенное количество Водорода превращается в гелий.
Кстати, самый тяжёлый газ - это радон.
Владимир Мтварелишвили, Samogo.Net
Последние опубликованные
Самая большая свинья в мире: где она живет? Рейтинг детских смесей: самые популярные производителиВ НИУ ВШЭ 27 октября 2020 года прошёл онлайн-семинар «Перспективы водородной энергетики — ожидания и вызовы». Его участники, среди которых был академик Сергей Алдошин, обсудили перспективы реализации «Энергетической стратегии Российской Федерации на период до 2035 года». В этом недавно утверждённом документе ставится сверхамбициозная цель: переход России от «нефтяной» к «водородной» трубе, то есть превращение в одного из крупных мировых экспортеров водорода, с которым в западном мире сегодня многие связывают безуглеродное будущее. Большинство участников семинара посчитали цели стратегии своевременными, хотя и отметили массу сложностей на этом пути. Главный вопрос: будет ли вообще существовать рынок водорода или речь идёт о временном увлечении без большого будущего?
Весь мир считает абсолютно необходимым остановить глобальное потепление. Для этого необходимо найти какую-то замену газу метану. Как известно, 40% всех выбросов диоксида углерода в мире генерируются при получении тепла, а отнюдь не электричества! Однако использовать для его выработки электроэнергию от солнечных и ветровых электростанций практически невозможно. Проблема в том, что зимние пики потребления тепла в странах с умеренным климатом вчетверо выше, чем зимние же пики потребления электроэнергии. Это значит, что покрыть их за счёт ВЭС и СЭС можно будет только если их мощности будут в разы выше уровня летнего потребления. Соответственно, в тёплые сезоны инфраструктура для генерации возобновляемой энергии обречена на простои, а, следовательно, и на чрезмерную дороговизну получаемого с её помощью киловатт-часа.
В таких условиях многие считают выходом использование в качестве накопителя энергии, а также топлива для самолётов, автомобилей и даже обогрева домов — водород — самый легкий из существующих газов. Тогда летом избыточные мощности ветряков и фотоэлементов можно отправлять на получение водорода электролизом воды. А затем закачивать его в подземные газохранилища, как метан сейчас, и зимой сжигать полученные запасы для покрытия пиковых потребностей в тепле, типичных для холодного времени года. Такая схема кажется логичным и экономически обоснованным путём к полной декарбонизации крупных экономик.
Подобная позиция стала модной и на уровне лиц, принимающих решения в государственных аппаратах ряда европейских стран. Например, в 2020 году Германия приняла «Национальную водородную стратегию», а чуть позже Еврокомиссия представила «Водородную стратегию для климатически нейтральной Европы». Очевидно, что на водородную энергетику возлагают большие надежды: считается, что её развитие поможет снизить зависимость от ископаемых энергоносителей и выполнить амбициозные цели по сокращению эмиссии парниковых газов.

Сергей Соловьёв,
научный руководитель АО «ВНИИАЭС»
Росатома
Сергей Соловьёв, научный руководитель АО «ВНИИАЭС» Росатома, выразил настрой значительной части участников семинара: сочетание высоких оценок перспектив и настороженности по поводу технических проблем «водородной эры». Он отметил: «Я целиком поддерживаю развитие водородной энергетики, но, тем не менее… выступаю против неоправданных темпов её развития. Недавно вышедшее Распоряжение Правительства дополнительно укрепило мои сомнения».
Сергей Соловьёв обратил внимание на то, что согласно этому документу, ключевая задача развития водородной энергетики в нашей стране — ответ на вызов выпадения углеводородов из мирового энергетического баланса из-за предпринимаемых западными странами усилий по декарбонизации их экономик. «И тут сразу встает вопрос: а ждут ли наш [российский] водород за рубежом?» — продолжает эксперт.
Стратегическая цель европейцев — в том числе Германии — состоит в переходе исключительно на «зелёный» водород. Это значит, что он должен быть получен электролизом, посредством электроэнергии от СЭС, ВЭС и сжигания биомассы. Очевидно, что для России эти варианты не подходят: объёмы такой генерации у нас невелики.
Другая большая проблема, озвученная Соловьёвым — тот факт, что водород в принципе сложнее перемещать на большие расстояния, нежели метан. При сгорании одного кубометра водорода (он весит всего лишь 90 грамм) выделяется ~10,8 мегаджоулей или три «тепловых» киловатт-часа. А вот при горении кубометра метана — порядка 35 мегаджоулей, или почти десять «тепловых» киловатт-часов. Выходит, чтобы «доставить» одно и тоже количество энергии через трубу, водорода по ней придётся прокачать втрое больше, а значит и затраты на транспорт будут выше. Кроме того, атомы водорода легко проникают в кристаллическую решетку металлов, делая их более хрупкими. От этого его транспортировка по металлическим трубам, в отличие от метана, может быть небезопасной.
В теории можно транспортировать сжиженный водород, но это потребует его охлаждения до -253 градусов. Это само по себе недёшево, и вдобавок трубопроводам понадобится крайне продвинутая система теплоизоляции. Альтернативой может стать перевозка жидкого водорода в газовозах.
С точки зрения Соловьёва, для атомной энергетики и конкретно «Росатома» развитие водородной энергетики весьма перспективно. Энергия атомных реакторов часто бывает невостребована, и тогда логично использовать её для наработки водорода. Однако не стандартным путем электролиза (у него низкий КПД и потому высокая стоимость), а, в идеале, за счёт использования специальных атомных реакторов, способных нагревать воду до +800 градусов. При таких условиях вода распадается на водород и кислород без затрат электричества. КПД этого процесса выше, чем при электролизе, использующем непосредственно электроэнергию от АЭС.
Предположительно, к 2050 году за счёт такого технологического процесса Россия могла бы получать до 50 миллионов тонн водорода, при том что в мире сегодня его получают 78 миллионов тонн. Однако это потребовало был строительства АЭС общей мощностью 200-250 гигаватт. По мощности это превосходит всю современную энергетику нашей страны.
Реализовать нечто подобное технически вполне возможно. Вопрос только в одном: есть ли надёжные данные, экономические прогнозы, что этот газ будет востребован в таком объёме?

Юрий Стеценко,
профессор НИУ ВШЭ,
руководитель представительства Российского экспортного центра
в Германии
С другой позиции на ситуацию взглянул Юрий Стеценко, доктор технических наук, профессор НИУ ВШЭ и руководитель представительства Российского экспортного центра в Германии. Он акцентировал внимание на том, что для Германии этот вопрос «уже решён». Немецкая сторона, как и ЕС в целом, совершенно однозначно нацелилась на подобные решения и уже начала вкладываться в проекты, которые могут дать нужный ей «зелёный» водород. Например, европейцы уже подписали документы о вложении примерно двух миллиардов долларов в наработку водорода посредством электролиза в Марокко. Источником электроэнергии здесь будут солнечные батареи, условия для работы которых в Северной Африке близки к идеальным.
Стеценко отмечает, что вне зависимости от российской позиции переход на водород в Европе произойдёт. И вопрос состоит не в том, будет ли Россия в этом участвовать, а в том, получит ли она от этого заметные преимущества или нет. Чем раньше мы «войдем» в этот процесс, тем выше наши шансы получить от него экономическую отдачу.

Юрий Мельников,
старший аналитик по электроэнергетике
Энергетического центра бизнес-школы «Сколково»
Юрий Мельников, старший аналитик по электроэнергетике Энергетического центра бизнес-школы «Сколково», обоснованно отметил, что для того, чтобы уверенно экспортировать тот или иной энергоноситель, страна прежде всего должна освоить его сама. По его словам, важно понять, не выйдет ли водород «золотым» для европейских покупателей — если производство этого газа в России будет ориентировано исключительно на экспорт. Он цитирует позицию немецких правительственных источников: «Время водорода пришло». Там его видят ключевым элементом для декарбонизации сталелитейной и автомобильной промышленности.
Однако пока, напоминает он, «Энергетическая стратегия» мало что сообщает о намерении использовать водород внутри страны. Речь идёт только об экспорте. Это выглядит её слабым местом, и такой подход нуждается в пересмотре.
В ходе дискуссии эксперты предположили, что наиболее вероятным приложением водорода в российских условиях может быть его использование в рамках северного завоза. Здесь его можно применять вместо солярки, которая имеет существенный углеродный след и выделяет много вредных веществ при сгорании.
Сергей Алдошин,
академик, научный руководитель
Института проблем химической физики РАН
Достаточно оптимистично на место России в будущей водородной энергетике взглянул академик Сергей Алдошин, долгие годы близкий к разработкам водородных топливных элементов. Он отметил, что в России в последние годы наладили, наконец, производство собственных мембран, что позволяет локализовать производство всех основных компонентов топливных элементов внутри страны. Более того, по его словам, ряд контактов с зарубежными партнерами (из Австрии) показал их интерес к импорту установок на топливных элементах из России.
Чтобы дать читателю более точное представление о глубине проблем, стоящих на пути водородной энергетики, следует напомнить некоторые базовые факты о методах его получения и физических свойствах.
Сегодня 95% всего водорода в мире получают не «зелёным» способом, а, как его обозначает Сергей Соловьёв, «турецким» (в английском языке его ещё называют «коричневым», brown). Это процесс, в ходе которого метан обдают перегретым водяным паром. В результате образуется смесь угарного газа и водорода, последний сепарируют и затем используют. Средняя стоимость такого водорода — 1,3 долларов за килограмм и выше.
Получение водорода электролизом сегодня крайне непопулярно из-за его высокой стоимости. По чисто физическим и химическими причинам кубометр водорода из воды можно получить, затратив никак не менее 3,6 киловатт-часов электроэнергии. При этом сам он отдает при сжигании всего 3 киловатт-часа («тепловых»). Более того, на практике идеальных установок электролиза не существует, и реально на кубометр водорода уходит не менее 4,5 киловатт-часов. При этом стоимость электричества в мире — не ниже 6 центов за киловатт-час, поэтому в среднем «зелёный» водород не может стоить дешевле 27 центов за кубометр. Даже в условиях сверхдешёвой электроэнергии от крупных ГЭС эта стоимость не упадёт ниже 18 центов. Таким образом один «тепловой» киловатт-час при сжигании «зелёного» водорода стоит 6-9 центов.
Цена же кубометра природного газа колеблется от 0,1 доллара (в США и России) до 0,2 долларов (в Европе), но при сгорании дает ~10 киловатт-часов. Стоимость «теплового» киловатт-часа от него — от 1 до 2 центов. Говоря иначе, энергия от «коричневого» (турецкого) водорода в 2-3 раза дороже, чем от метана. В случае же «зелёного» водорода разница достигает четырёх раз. Сегодня в мире потребляют 3,5 триллиона кубометров природного газа в год. Замена его на «коричневый» водород при нынешних ценах означает рост затрат на энергию более чем на три триллиона долларов в год. А на «зелёный» — более чем на шесть триллионов долларов в год. Источники финансирования подобного перехода пока неясны.
Кроме того, в случае если его предпримет только ЕС, а страны третьего мира воздержатся, конкурентоспособность сталелитейной и ряда других энергоёмких отраслей европейских экономик снизится до нуля. Само их существование станет возможно только при жесткой протекционистской защите местного рынка. Но его закрытие может спровоцировать серию торговых войн с туманным исходом. Впрочем, каким бы он ни был, ясно одно: сами эти войны нанесут крупный ущерб мировой экономике.
Опасной стороной проблемы является то, что здесь нет потенциала резкого падения цены. С ВЭС и СЭС технологии могут снижать стоимость генерации со временем, но водород — это не готовый природный источник энергии (как ископаемый метан), а её носитель, создаваемый человеком. Это значит, что никакое совершенствование технологий не позволит снизить его стоимость настолько, чтобы описанный выше разрыв мог серьёзно сократиться.
Другая проблема водородной энергетики — низкая плотность водорода, во много раз уступающая метану. Поэтому его прокачка по трубам на большие расстояния требует слишком больших затрат энергии. Водород, как указано выше, можно сжижать (хотя это также потребует больших затрат энергии), но в жидком виде он весит 70 килограмм на кубометр — в шесть раз меньше, чем сжиженный метан. Иными словами, одинаковый по объёму бак с жидким метаном будет в 2,5 раза более энергоёмким, чем аналогичный с жидким водородом.
В такой ситуации попытки создания самолётов на водороде автоматически означают резкое сокращение дальности полётов таких машин (в разы). Попутно, в силу того, что даже «коричневый» водород минимум втрое дороже метана и даже дороже керосина, «водородизация» авиации должна привести к заметному росту цен на авиабилеты. В 2,5 раза большая нужда в посадках для дозаправки также повысит стоимость и, кроме того, увеличит время в полете. Насколько мировая авиаиндустрия, особенно с учётом глубокого кризиса из-за пандемии COVID-19, готова на такой технический шаг назад. И намерены ли пассажиры оплатить его?
В области автомобилестроения водородные автомобили на сегодня — явные аутсайдеры. Стоимость машин с топливными батареями выше (даже лучших, типа Mirai), чем у электромобилей Tesla тех же размеров, а динамика заметно хуже. Кроме того, стоимость жидководородной заправки начинается от пары миллионов долларов, а электро — от 50 000 долларов.
Всё это — ключевые причины, по которым число авто на водороде в современном мире измеряется считанными тысячами, а электромобилей — миллионами.
Чисто теоретически, чуть лучше выглядит ситуация с водородным топливом на рынке обогрева домов. Если получать «зелёный» водород в Европе и перекачивать его на малые расстояния, то для этого вполне годятся газовые пластиковые трубы низкого давления, используемые сегодня в ЕС для природного газа.
Однако и здесь возможны заметные сложности — в первую очередь, в плане готовности потребителей. По данным британской прессы, в Соединённом Королевстве и сегодня бывают зимы, когда число жителей этой страны, умерших от последствий плохого отопления, достигает 15 тысяч в год (это явление называют fuel poverty). Повышение стоимости газового отопления, а именно оно сегодня доминирует в Англии, в три и более раза может увеличить эту цифру. Насколько европейское общество психологически готово заплатить за декарбонизацию подобным образом — пока остается большим вопросом.
Таким образом, переход к водородной энергетике может состояться только в том случае, если западные государства готовы к нему буквально любой ценой.
В чём нельзя не согласиться с участниками онлайн-семинара, так это с тем, что в теории позиции России в случае мирового перехода к «водородной экономике» выглядят не так плохо. Росатом сегодня доминирует на мировом рынке строительства реакторов, и, судя по некоторым его экзотическим проектам (БН-800 на уран-плутониевом топливе), способен создать реакторы с нестандартными параметрами, чтобы получать «зелёный» водород по умеренным ценам.
Как сообщил в ходе онлайн-семинара Сергей Соловьёв, цена водорода при таком пути получения может быть 1,15-1,2 доллара за килограмм. Технически это на уровне лучших образцов «коричневого» водорода, и намного меньше, чем у «зелёного». Вместе с готовностью страны производить топливные элементы, это внушает оптимизм. Если водородный рынок в мире состоится, к «нефтяной» и «газовой» игле вполне может добавиться ещё и «водородная».
Однако и здесь не всё так просто. Даже если предположить, что западный мир в самом деле готов заплатить за водородную декарбонизацию — несмотря на то, что водород всегда будет минимум втрое дороже природного газа — далеко не факт, что ЕС психологически готов платить за это российским экспортёрам. Как отметили участники онлайн-семинара, чтобы добиться возможности такого экспорта, придётся провести комплексное исследование, сравнивающее, какое количество углекислого газа на килограмм полученного водорода выбрасывается в российской атомной отрасли и в проектах, использующих ветровые и солнечные электростанции. Только если «атомный» водород в самом деле окажется не менее зеленым, чем «ветровой» и «солнечный», может идти речь о выходе России на такой рынок.
IQ
Автор текста: Александр Березин
29 октября, 2020 г.
Технические газы - процессы резки и сварки - горючие газы - атмосферные газы - гелий - двуокись углерода
От ацетилена до ксенона… Messer предлагает вам гораздо больше, чем просто газы. Наше ноу-хау в области прикладных технологий является как обширным, так и специализированным. Таким образом, это ключ к оптимизации производственных процессов с точки зрения качества, экономичности и инноваций.
Наши клиенты получают добавленную стоимость независимо от того, представляют ли они автомобильную, пищевую, химическую, нефтехимическую, металлургическую, электронную, экологическую, медицинскую или сварочную отрасли.
Сварочные защитные газы доступны под торговыми марками: Aluline, Inoxline и Ferroline, унифицированными во всех компаниях группы Messer, что облегчает нашим клиентам выбор подходящих продуктов для данной технологии.
Ацетилен – это высокоэффективный горючий газ с широким спектром применения – настоящий газово-кислородный омнибус. Для сварки, резки, зачистки, напыления, правки пламенем и газовой строжки - ацетилен всегда является правильным выбором.
Традиционно ацетилен получают путем химической реакции карбида с водой. Однако Messer также поставляет ацетилен из нефтехимических производств в Европе.Также другие горючие газы являются продуктами процессов в нефтехимическом секторе.
Водород — самый легкий из всех газов. Важнейшими процессами получения водорода являются процессы каталитического риформинга (паровой риформинг) и электролиз растворов хлорида калия. Более двух третей мирового производства водорода приходится на химический сектор, где большая его часть используется для синтеза аммиака и метанола. Водород используется во многих отраслях промышленности из-за его типичных физических и химических свойств - в качестве горючего газа для специальных применений, в качестве защитного газа при термообработке, в технологии пищевых продуктов и в электронной промышленности.В последнее время водород также рассматривается как альтернативный энергоноситель. Но водород также используется в определенных целях в металлургической промышленности и лабораториях. Благодаря своей высокой теплопроводности водород также используется в качестве охлаждающего газа, например, для генераторов электроэнергии.
Доля азота в воздухе, которым мы дышим, составляет 78% по объему. При температуре окружающей среды азот представляет собой бесцветный газ без запаха и нейтрального вкуса.Он нетоксичен и при низких температурах химически инертен, то есть чрезвычайно пассивен в химических реакциях. Азот негорюч и может подавлять процессы горения. Кроме того, при высоких концентрациях он оказывает удушающее действие, поскольку вытесняет кислород, необходимый для дыхания. При атмосферном давлении азот становится чистым при минус 196°С.
С другой стороны, кислород составляет 21% состава атмосферного воздуха. При минус 183 °С кислород становится жидким, а при минус 218,9 °С — твердым.Жидкий кислород при атмосферном давлении занимает в газообразном виде всего 854 части своего объема. Поэтому большое количество кислорода транспортируется и хранится в жидком виде при низких температурах.Важнейшим свойством кислорода является его реакционная способность. Есть только несколько элементов, с которыми кислород не связан атомарно. В обогащенной кислородом атмосфере процессы окисления и горения протекают значительно быстрее, чем на воздухе. Благодаря этому свойству кислород необходим для большого количества промышленных применений.Кислород необходим для метаболизма многих организмов и хорошо растворим в воде. Поэтому он используется во многих приложениях для очистки воды и защиты окружающей среды.
Аргон — благородный газ без цвета и запаха, тяжелее воздуха. Важнейшим свойством аргона является его химическая инертность. Это свойство делает аргон идеальным защитным газом даже при температурах, встречающихся в металлургии и дуговой сварке. Аргон демонстрирует поведение, фактически отклоняющееся от закона идеального газа при высоких давлениях.Это приводит, среди прочего, к тому, что газовый баллон при давлении 200 бар содержит примерно на 7% больше аргона, чем можно было бы ожидать, взяв за основу закон идеального газа. Аргон не токсичен, но, как и азот, может вытеснять кислород, необходимый для дыхания. Более того, поскольку аргон тяжелее воздуха, он может скапливаться у земли, особенно в углублениях.
Гелий, наряду с водородом, является наиболее распространенным элементом во Вселенной.Однако гелий почти полностью отсутствует в атмосфере Земли. Поэтому весь спрос в настоящее время обеспечивается за счет источников природного газа, содержащих гелий. Мировой спрос удовлетворяется за счет богатых месторождений в США, Северной Африке, России и на Ближнем Востоке.
Двуокись углерода присутствует в нашей атмосфере в ограниченном количестве (0,03%). Это химическая молекула, образованная атомом углерода и двумя атомами кислорода, широко известная как: CO 2 .Углекислый газ (CO 2 ) представляет собой бесцветный, негорючий, слабокислый газ без запаха. Углекислый газ в соединении с водой образует угольную кислоту (H 2 CO 3 ). Особые свойства углекислого газа, такие как его реакционная способность и растворимость в воде, делают CO 2 идеальным помощником во многих сферах нашей повседневной жизни и защиты окружающей среды.
Одним из них являются газообразные агрегатные состояния веществ. В таком виде они чаще всего существуют во Вселенной, образуя туманности, звезды и межзвездное вещество. Земля не без газа. К ним относится состав воздуха, присутствующего в живых организмах. А какой самый легкий газ? Какие функции у него есть? Давай выясним.
Химический элемент, молекулы которого составляют самый легкий газ, — водород.В периодической таблице он обозначается символом Н и стоит первым. Он уникален в природе тем, что может быть опасен, но в то же время крайне необходим любому живому существу.
Водород является самым легким газом, когда два его атома соединяются вместе, образуя молекулу, образующую h3. По легкости он в 14,5 раз быстрее воздуха. Может взорваться при смешивании с кислородом или воздухом. Но если мы соединим два атома с атомом кислорода, то получим нужную нам обычную воду.На это указывает его латинское название Hydrogenium, которое можно перевести как «производящий воду».

Если соединить два атома водорода и два атома кислорода, получится другое вещество. Они образуют перекись водорода — бесцветную жидкость, которую используют для обеззараживания ран, осветления волос, а также в качестве ракетного топлива.
Самый легкий химический газ при нормальных условиях не имеет цвета, вкуса и запаха.Его плотность на кубический сантиметр составляет всего 0,0000899 грамма. Его температура кипения составляет 252,6°С. В свободном состоянии он присутствует в виде газа h3.
Водород прекрасно растворяется во многих металлах (палладий, титан, ниобий, платина, никель) и диффундирует с ними. Он также растворим в этаноле, но не смешивается с серебром.
Обладает высокой теплопроводностью, в семь раз выше, чем у воздуха. Жидкий водород также легкий и бесцветный.При разжижении его объем уменьшается и вещество приобретает криогенные свойства. В таком виде он опасен для человека — может вызвать обморожение кожи, а его пары — отек легких.
В твердом состоянии вещество выглядит как белоснежная масса. Плавится при -259,2°С и имеет едва ли не самую низкую плотность среди простых твердых веществ - 0,08667 г/см³. При давлении 300 ГПа переходит в металлическое состояние. Предполагается, что металлический водород находится в ядре некоторых планет, таких как Сатурн и Юпитер.

Самый легкий газ сам по себе неактивен. Однако при нагревании он может реагировать с различными веществами, такими как азот, кислород, сера и др. Горение водорода сопровождается выделением воды, что было открыто в 18 веке химиком Лавуазье, давшим ему название.
При смешивании с кислородом окисляется. Но при обычной температуре реакция медленная и незаметная со стороны. Тем не менее смесь назвали «взрывчатой», поскольку при нагревании она взрывается, сопровождаясь громким хлопком.Даже одной искры достаточно, чтобы активировать смесь.

Реагирует со светом и теплом со многими металлами и неметаллами. В случае с хлором образует хлороводород — устойчивый газ с отчетливым запахом. Растворяется в воде и горит во влажном воздухе. Аммиак образует азот с серой, сероводород имеет сильный запах серы, похожий на серу.
При нормальной температуре самый легкий газ реагирует только с фтором и очень активными щелочными металлами, такими как кальций.С фтором он очень взрывоопасен и вступает в реакцию даже при температуре замерзания и в темноте.
Оксиды поглощают кислород и действуют как восстановитель. Так, из CuO на выходе образуются медь и вода, а из WO 3 - вольфрам и 3H 2 O.
Водород - самый распространенный элемент во Вселенной, но на Земле он уступали превосходству кислорода. В космосе самый яркий газ, присутствующий в межзвездном материале, образует туманности, звезды и ядра планет.
На солнце и других звездах температура слишком высока, поэтому водород становится плазмой. Наряду с этим в нем протекают термоядерные реакции, которые сопровождаются выделением огромного количества энергии. Именно горение водорода и его превращения позволяют звездам сиять и выделять тепло.
На Земле водород в основном связан. В свободном состоянии только 0,00005% этого газа находится в сухом воздухе. Он присутствует практически во всех живых клетках. Таким образом, около 64% атомов в организме составляют водород.Он входит в состав белков, жиров, гормонов и других соединений.
Когда-то самый легкий газ использовался для подъема в воздух воздушных шаров и дирижаблей. Однако это было небезопасно. Если он каким-то образом получал кислород, установка загоралась. Из-за возгорания самого большого дирижабля «Гинденбург» в 1937 году погибло 35 человек. Затем опасный газ заменили гелием.

Хлористый водород теперь состоит из водорода и соляной кислоты, а также аммиака, необходимого для производства удобрений.С помощью мыла, пластика. Объединив его с CO 2 , получите синтез-газ для производства энергии. Проходя через него жидкие растительные жиры, получают твердые, из которых делают маргарин.
Восстановительные свойства водорода помогают в получении чистых оксидов металлов (медь, вольфрам, молибден и т.п.). При его горении создаются очень высокие температуры (3000-4000 градусов), с их помощью варятся тугоплавкие металлы.
Водород имеет высокую теплотворную способность и не вреден для окружающей среды, при его сгорании в атмосферу выделяются кислород и вода.Он с легкостью заменит дорогую нефть и газ, каменный уголь, а также остановит выделение вредного углекислого газа, неизбежного при их переработке.
Над этим вопросом сейчас ломают голову ученые. Повестка дня в области водородной энергетики уже была выражена Исландией, США, Японией, Южной Африкой, Индией и Южной Кореей. В Италии Enel уже запустила электростанцию на этом газе, Япония объявила, что откроет свою станцию в 2018 году. Автомобильные компании уже давно представили свои водородные модели.

Этот вид топлива может решить некоторые ваши проблемы. Однако он может генерировать новые. Пока неизвестно, как эффективно производить водород, затратив минимум денег и не нарушив природный баланс. Соответственно, все идеи по использованию легчайшего газа находятся в стадии разработки.
.С тех пор, как лавинный рюкзак увидел свет, он вызвал массу эмоций. Это давало надежду перехитрить природу и избежать последствий лавинных аварий. В настоящее время лавинные рюкзаки выпускаются многими компаниями и помимо оценки принципа работы стоит посмотреть на конкретные решения.
Однако, прежде чем мы перейдем к выбору рюкзака, стоит узнать, как он устроен.И это, вопреки видимости, очень просто. Описывая лавину в движении, можно сказать, что она ведет себя как густая жидкость. А можно прибегнуть к иллюстрациям из повседневной жизни и изображению емкости для мюслей. Когда мы его встряхиваем, на поверхности образуются большие легкие хлопья, а на дне оседают изюм и орехи. Каждое из этих описаний обосновывает вывод о том, что по отношению к объекту в движущейся лавине можно говорить о его смещении. Очень важно, что речь идет о лавине в движении – когда снег прекратится, все кардинально изменится.
Таким образом, лавинный рюкзак увеличивает плавучесть (проще говоря: увеличивает свой объем, сохраняя при этом ту же массу) человека, попавшего в лавину, и тем самым заставляет его оставаться наверху в движущейся массе снега. И, возможно, это спасет вам жизнь. Еще несколько лет назад лавинные рюкзаки - в основном из-за значительной стоимости - встречались редко. Тем не менее, осведомленность горных пользователей растет, и сегодня лавинный рюкзак является основным снаряжением каждого скитуриста. А если у кого-то еще нет рюкзака или я хочу заменить тот, который должен хорошо подумать, какой лавинный рюкзак выбрать?
 (фото.Черный алмаз)
(фото.Черный алмаз) Первый патент на конкретное решение в этой области был подан в 1980 году. Его работа заключается в следующем. При срабатывании системы сжатый газ из баллона поступает в баллон, вшитый в лавинный рюкзак, через устройство, называемое соплом Вентури. Конструкция засасывает большое количество дополнительного воздуха извне, и полученная смесь заполняет вшитые в рюкзак мешки. Владельцем первого патента был Питер Ашауэр, основатель компании ABS, пионера мировой индустрии.ABS показала первую модель рюкзака, готовую к продаже на ISPO в 1985 году. Это была модель с одной подушкой, которая с сегодняшней точки зрения была далека от идеала. Потом, правда, произвел большое впечатление и надеялся, что лавинные аварии будут уносить меньше жизней. Это было первое устройство для предотвращения лавинного затопления. Рюкзаки ABS постепенно модифицировались, и, наконец, в 1998 году система приобрела вид, близкий к тому, что мы имеем сегодня.
Большим шагом в эволюции лавинных рюкзаков стало использование мобильной системы, которая не вшивается в рюкзак постоянно.Благодаря этому его можно разместить между адаптированными к этому рюкзаками разного размера. Прорывом стало также внедрение все более легких баллонов — сначала алюминиевых, а затем и карбоновых. По истечении срока патентной защиты на рынке появились другие игроки: Ortovox, Mammut, Pieps, Deuter, BCA, Black Diamond. Наконец, произошла революция и в самих характеристиках рюкзака: выпущена модель JetForce . Это система, в которой от баллона со сжатым газом отказались в пользу батареи и вентилятора, надувающего баллон рюкзака.Итак, какой лавинный рюкзак выбрать? Тема более сложная, чем может показаться.
 Лавинный рюкзак может спасти нас от угнетения и спасти нам жизнь (фото: Pieps)
Лавинный рюкзак может спасти нас от угнетения и спасти нам жизнь (фото: Pieps) При выборе лавинного рюкзака стоит знать несколько основных фактов. Рюкзак не является гарантией безопасности и не делает нас бессмертными. Сама механика эффективна до тех пор, пока снег движется и пострадавшему от лавины удается активировать систему.Без потягивания рукоятки активации ничего не произойдет. В истории нередки случаи, когда люди гибли в лавине, не активировав функциональный рюкзак. Те, кто его запускал, чаще всего частично засыпаны, т.е. на поверхности лавины видны подушки рюкзака. Вам может понадобиться помощь других людей, чтобы выбраться из лавины. Пятая часть жертв лавины – это люди, погибшие в результате травм, а лавинные рюкзаки не защищают от травм.
 В труднопроходимой местности также необходимо уметь пользоваться лавинным рюкзаком.(фото: Пипс)
В труднопроходимой местности также необходимо уметь пользоваться лавинным рюкзаком.(фото: Пипс) Основная слабость лавинного рюкзака имеет шанс проявить себя, когда лавина остановится. Все хорошо, пока лавина теряет скорость и растекается по все менее и менее крутой местности. Если лавина резко остановится при резком изменении угла с крутого на пологий или в овраге или овраге, новые порции снега будут наноситься на уже неподвижного пользователя, от которого уже нет никакой защиты.Дополнительным травмоопасным фактором может быть и ситуация, при которой лавина обрушивается на скальный порог.
Серьезный риск, связанный с использованием лавинного рюкзака, возникает также в случае поломки лыж в лавине. Конфликт между подушкой рюкзака, выталкивающей лыжника на поверхность, и широкими лыжами или сноубордом, затянутыми массами снега, может привести к серьезным травмам. Палочки могут быть так же неблагоприятны, когда мы надеваем петли на запястья. Они могут нанести серьезную травму, поэтому рекомендуется снять их перед спуском на опасную местность.
По мере того, как лавинные рюкзаки становятся все более популярными, их используют все менее и менее опытные люди. Иногда предполагают, что с таким рюкзаком можно вообще не бояться лавин. Такой подход приводит к тому, что использование рюкзака увеличивает уровень риска, а не снижает его. Вы должны знать, что это решение, которое может частично предотвратить неприятные последствия аварий. Это очень эффективно, но не дает добро на нарушение основных правил безопасности.Поэтому при выборе потенциально опасного участка так важно приобрести элементарные знания. Она должна основываться на знании механизмов образования лавин, распознавании типов снега, передвижении по такой местности, действиях при сходе лавин и оказании первой помощи. Лучше всего, если практика, полученная во время зимних тренировок, будет сочетаться со знаниями. Лавинный рюкзак не освобождает вас от лавинной азбуки.
 Наличие лавинного рюкзака не делает нас бессмертными и не освобождает от соблюдения правил безопасности (фотоПипсы)
Наличие лавинного рюкзака не делает нас бессмертными и не освобождает от соблюдения правил безопасности (фотоПипсы) При выборе лавинного рюкзака стоит ознакомиться с решениями, доступными на рынке. Сколько пользователей, столько и потребностей. Каждая из систем имеет свои преимущества и недостатки.
В этом решении после активации сжатый воздух заполняет два мешка по бокам рюкзака. Это классический дизайн лавинного рюкзака, который будет работать в любых условиях.Рюкзаки-цилиндры были единственным решением на протяжении многих лет и спасли жизни сотням лыжников. Однако и у них есть некоторые особенности, о которых следует помнить. Баллоны для рюкзаков ABS (как и для всех систем сжатого воздуха) заполняются газовой смесью только на заводе. Там же регенерируются пиротехнические рукоятки, используемые для активации системы. Это связано с затратами и необходимостью посетить магазин-партнер ABS. Конечно, нет необходимости ждать заправки баллона на заводе.В магазине можно сразу заменить пустой баллон на новый, полный.
Проблема со всеми цилиндровыми системами - транспортировка самолетом. Газовые баллоны нельзя провозить на борту самолета или в регистрируемом багаже. Баллонные системы со сжатым газом имеют еще одно принципиальное ограничение: их можно запустить только один раз. Повторный обжиг требует установки нового цилиндра. Примерами рюкзаков с системой ABS являются ABS s.CAPE + ZipOn 30-34L или сверхлегкий ABS A.Light Free.
 Рюкзак Avalanche из АБС-пластика A.Свет бесплатно (фото: ABS)
Рюкзак Avalanche из АБС-пластика A.Свет бесплатно (фото: ABS) Система JetForce состоит из нескольких компонентов: ручки активации, воздушной подушки, аккумуляторов и специального компрессора. При нажатии на ручку открывается запорная заслонка и запускается компрессор, который надувает подушку безопасности примерно за 3 секунды. В течение 3 минут работает на меньшей скорости, прерываясь кратковременной и быстрой прокачкой. Подушка обеспечивает дополнительную защиту головы и увеличивает объем попавшего в лавину человека, благодаря чему он переносится в ее верхний слой.Примером использования этой системы является рюкзак Pieps JetForce BT 25 или рюкзаки Black Diamond, такие как Black Diamond JetForce Tour 26L.
Основное преимущество системы JetForce на цилиндровых системах заключается в том, что она может срабатывать несколько раз за одну поездку. Более того, рюкзаки с этой системой не проблема при путешествии на самолете. Также очень важно, что через три минуты после надувания JetForce запускает вентилятор в обратном направлении и всасывает воздух из баллона.В результате на месте пустого баллона останется довольно большое открытое пространство, которое должно позволить дышать несколько дольше в случае частичного закапывания. При условии, конечно, что давление снега позволяет груди дышать. Более того, при покупке рюкзака с системой JetForce вы получаете бесплатную тренировку. Это может помочь автоматизировать правильные рефлексы. Однако у JetForce есть и обратная сторона: система немного тяжелее, чем конкурирующие продукты с цилиндрами. Однако разница не существенна.
 Ручка активации JetForce в рюкзаке Black Diamond (фото: Black Diamond)
Ручка активации JetForce в рюкзаке Black Diamond (фото: Black Diamond) Это решение используется в моделях лавинных рюкзаков Ortovox. Он состоит из ручки активации, специальной подушки безопасности и баллончика со сжатым газом (обычно приобретается отдельно). В случае угона лавиной, потянув за ручку, активируется подушка безопасности. Это помогает лавине оставаться на плаву, что увеличивает шансы на выживание.Это одна из самых легких систем благодаря соответствующей конструкции подушки безопасности и легкому блоку Вентури. Активация происходит без электричества. Подушка сшита так, что занимает минимум места внутри рюкзака, обеспечивая при этом достаточную прочность и герметичность. В отличие от системы ABS, подушка имеет С-образную форму и также защищает голову.
Важное преимущество Avabag, которое можно найти среди других На моделях Ortovox Free Rider 20 S или Ortovox Ascent 22 можно потренироваться запускать систему.Согласно исследованиям, проведенным группой экспертов под руководством Паскаля Хегелы, у некоторых пользователей рюкзаков возникают проблемы с активацией подушки. Проанализировано 106 лавинных происшествий с участием людей, использующих это решение. Каждый восьмой пользователь рюкзака не смог активировать систему. Это исследование показывает, насколько важно практиковать правильные рефлексы. Система Avabag позволяет тренировать правильное поведение без газового баллончика.

Руководство, содержащееся в этом тексте, не заменяет знания и практику, которые лучше всего приобретаются на курсах лавинного и зимнего туризма, проводимых опытными инструкторами.
[Однако, если вы не определились с лавинной моделью, а ищете лыжный рюкзак, читайте наш путеводитель: какой туристический рюкзак?]
.Автор: Марчин Качперек, горный и лыжный гид IVBV, группа гидов Фрирайда: фрирайды.номер
В автодомах одним из основных источников энергии является сжиженный углеводородный газ, также известный под названиями - сжиженный газ, СУГ или пропан-бутан. Для того чтобы знать все опасности, возникающие при использовании этого топлива, необходимо знать его физические свойства. Также стоит ознакомиться с принятыми правилами использования установок ГБО.
Жидкие газы представляют собой смеси углеводородов. Чаще всего мы получаем их путем стабилизации сырого бензина, сырой нефти или путем переработки газов нефтепереработки от риформинга бензина, крекинга, пиролиза и т.д.процессы обработки. Проще говоря: СНГ получают из сырой нефти и производят в дистилляционной камере как самую легкую фракцию.
Пропорции
Газ в баллонах, приобретаемый на АЗС, должен представлять собой смесь пропана и бутана в соотношении 1:1. К сожалению, практика заводов по розливу газа иная, и часто бутан, будучи более дешевым, может занимать больший процент.
Свойства
Одними из основных величин, характеризующих свойства газа, являются теплота сгорания и теплота сгорания.Рассмотрим подробнее, что именно характеризуют эти величины.
Теплотой сгорания газа является количество теплоты, выделяющееся при полном сгорании 1 м3, измеренное при температуре 25 °С и давлении 1013,25 гПа, где вода, образующаяся в процессе сгорания водорода и его соединений, находится в виде жидкости. Единицей теплоты сгорания является мегаджоуль, деленный на кубический метр [МДж/м3]. Теплотворная способность газа – это количество теплоты, выделившееся после полного сгорания 1 м3, измеренное при 25°С и давлении 1013,25 гПа, с образованием воды в в процессе горения водород и его соединения существуют в виде водяного пара.Единица такая же, как и для теплоты сгорания. Таким образом, теплотворная способность всегда ниже теплоты сгорания (около 11%). Это связано с выделением большого количества тепла при конденсации водяного пара. Поскольку в процессе работы устройств, приспособленных к сжиганию газа, не происходит конденсации водяного пара, теплотворная способность сгорания является основой для различного рода сравнений, анализов и расчетов.
газ Теплотворная способность [МДж/м3]
пропан 93,11
бутан 123,66
Из приведенной выше таблицы видно, что бутан является более энергоемким газом.Также упоминалось, что это более дешевое топливо. Так почему мы смешиваем его с пропаном? Давайте посмотрим на другое физическое свойство, которым является температура конденсации.
Температура конденсации
При нормальных условиях (температура 0°С, давление 1013,5 гПа) и пропан, и бутан являются летучими веществами. Чтобы изменить их агрегатное состояние, у нас есть два варианта: либо увеличить давление, либо уменьшить температуру. Просто изменив температуру, чистый бутан уже будет жидким при -0,5°С, а пропан при -42°С.На практике для сжижения газа используют повышение давления.
Помните, что баллоны всегда должны располагаться вертикально.
Почему температура конденсата так важна для нас, туристов? Все ресиверы в наших автомобилях работают на топливе в газовой фазе. Газ должен изменить фазу перед сгоранием, а для этого нужна правильная температура. Летом с этим проблем нет, к сожалению, при понижении температуры ниже -0,5°С (зимой или ранней весной) из смеси в цилиндре будет испаряться только пропан.Конечным результатом будет то, что баллон, в котором якобы не осталось газа, наполовину полон! Поэтому в зимних автодомах рекомендуется использовать чистый пропан.
Взрыв
Пределы взрываемости (воспламенения) выражают нам такие пределы содержания газообразного топлива в смеси с воздухом, между которыми происходит горение этой смеси. Нижний предел воспламенения дает нам минимальное содержание газообразного топлива, ниже которого воспламенение смеси не распространяется, а верхний предел показывает максимальное содержание топлива.
Пределы пропан бутан
нижний 2,1 1,5
верхний 9,5 8,5
Плотность
Сжиженный нефтяной газ, в отличие от природного газа, тяжелее воздуха. При любой протечке он скапливается в самой нижней точке и представляет опасность воспламенения. Поэтому в наших автомобилях стоит размещать форточки в полу под холодильником и плитой. Также следует помнить, что нельзя закрывать низко расположенные отверстия в изолированных помещениях для газовых баллонов.
Токсичность
Сжиженный газ в высоких концентрациях обладает наркотическими свойствами и может вызвать отравление, проявляющееся головной болью, рвотой и общей слабостью.Здесь я хотел бы упомянуть, что наиболее токсичным газом является угарный газ. Он образуется, когда элементарный углерод, содержащийся в газообразных топливах, не полностью сгорает. Поэтому давайте позаботимся о том, чтобы наши газоприемники всегда были исправны и отлажены.
Закон
В Польше установки сжиженного нефтяного газа в караванах и автодомах не подлежат каким-либо обязательным проверкам. Однако проверить герметичность установки стоит ради собственной безопасности и безопасности ваших близких.Думаю, что мастерские, устанавливающие ГБО на автомобили, не откажут в помощи.
Несколько очень важных правил при использовании системы ГБО:
• в помещении, где находится баллон, температура не должна превышать 35°С;
• Баллоны устанавливаем только в вертикальном положении;
• расстояние между баллоном и излучающим устройством должно быть не менее 1,5 метра;
• баллоны нельзя размещать ближе 1 метра от устройств, которые могут вызвать искрение;
• Газовая установка должна быть подсоединена к редуктору давления газа на баллоне с помощью гибкого шланга длиной не более 3 метров и сопротивлением давлению не менее 300 кПа, устойчивого к жидким компонентам газа, механическим повреждениям и повышению температуры. до 60°С.
Томаш Скуп
www.karawaning.pl
| В СТРАНЕ СТИХИЙ 9000 8 |
Здесь вы найдете самую интересную и важную информацию об элементах.
Каждый элемент описывается по схеме:
атомная масса, атомный номер, символ элемента, название ациска.
«Кирпичики вселенной»
Так называли химические элементы в энциклопедии.
Существует огромное разнообразие элементов, встречающихся на Земле: одни редки, другие встречаются очень часто. Одни, такие как золото, могут бросаться в глаза, другие, такие как азот, кислород, представляют собой невидимые для нас газы.
Около 300 лет назад было известно всего 12 элементов: антиномы, мышьяк, висмут, олово, середина, свинец, ртуть, сера, серебро, углерод, золото и железо. По мере того, как их было обнаружено больше, ученые увидели четкую связь между ними.
Были некоторые пробелы в выравнивании в определенном порядке элементов, и такие ученые, как Менделеев, Рамзи, Мозли и Бор предсказали существование неизвестных элементов и их свойств.Они были обнаружены позже и заняли то место, которое им предназначалось.
Элементы располагались в порядке, вытекающем из строения их атомов.
"Мало какая систематизация в истории науки может соперничать с понятием периодичности по масштабам показанного ею физического порядка мира. (...) - я буду следовать существующему порядку и иметь характеристики специфические в соответствующую группу» ( McGraw-Hill Encyclopedia of Science Technology) .
Элементы расположены в ряды - периоды и столбцы - группы в таблице Менделеева.
Элементы, принадлежащие к одной и той же группе, обнаруживают удивительное сходство.
Например: гелий, неон, аргон, криптон, ксенон и радон — это газы, которые ярко светятся под действием электрического разряда и поэтому используются в люминесцентных лампах. К тому же, в отличие от других газов, очень трудно вступает в реакцию с различными элементами.
Удивительный порядок и гармония творятся во Вселенной, вплоть до атомов и элементарных частиц.
Бартомей Сепсяк
| КИСЛОРОД |
- бесцветный газообразный элемент без вкуса и запаха,
- получен впервые около 200 лет назад как Джозефом Пристли после нагревания оксида ртути, так и Карлом Вильгельмом Шеелем, но Антуан Лоран Лавуазье считает его элементом.
- сжижен 15 апреля 1883 г. Врблевски и Ольшевски,
- в жидкой и твердой фазе имеет бледно-голубой цвет,
- другая, ароматная форма кислорода - озон (получается при электролизе воды на электроде)
- кислород состоит из двухатомных частиц, а озон из трех атомов кислорода
- в чистом виде применяется в медицине, сельском хозяйстве, металлургии, технике, химической промышленности, авиации,
- кислород вызывает повреждение материала - ржавчину, нержавейку, химическую коррозию.. Это один из самых распространенных элементов на Земле.
| АЗОТ |
- бесцветный, нетоксичный газ без запаха
- открыт в 18 веке Дэниелом Резерфордом,
г. - различные известные названия: «гнилой воздух», «флогистонный воздух», «атмосферный угарный газ»,
- в нормальных условиях образует двухатомную молекулу с очень прочной связью.
- не играет роли в дыхании человека,
- является важным компонентом аминокислот - основных строительных блоков всех живых организмов,
- сжиженный Врблевским и Ольшевским,
- в жидком и твердом виде бесцветен,
- используется для: электрических лампочек, в качестве защитного газа, производства аммиака и многих химических соединений,
- образует соединения с кислородом, и одно из них - монооксид, является веселящим газом.
| УГОЛЬ |
- чистый углерод встречается в природе в нескольких аллотропных разновидностях,
- наиболее важные виды угля: графит, алмаз и карбин,
- аллотропы угля имеют различную кристаллическую структуру, поэтому имеют разные физические свойства,
- углерод, содержащийся в биаке человеческого тела, бесценен,
- ископаемый уголь получит прозвище "черное золото",
- является сырьевой базой в энергетике и химии,
- изотоп С14 позволяет определить примерный возраст памятников из органических материалов.
| ВОДР |
- открыт в 1661 году Бойлем и назван «горючим воздухом»,
- название воды происходит от греческого «гидроген», что означает тот, кто рождает воду,
- своим нынешним названием обязан Каведишу,
. - самый простой в построении, имеет в ядре всего один атом,
- газ в виде двухатомной молекулы, без вкуса и запаха,
- самое легкое вещество в мире,
- встречается в виде смеси трех изотопов: обычного водорода, дейтерия и трития,
- Врблевский и Ольшевский определили его температуру конденсации,
- ранее использовался для трюков жонглирования (при смешивании с кислородом создает взрывоопасную смесь)
| ФЛУОР |
- название элемента происходит от латинского слова fluo - pyn,
- наиболее химически активный, т.е. наименее благородный,
- работает рко, пар, кизяк,
- в виде газа имеет зеленоватый цвет, а сжиженная и твердая фаза - светлый цвет,
- образует двухатомные молекулы, но со слабой связью между атомами,
- используется в быту - холодильники (фтористое соединение - фреон),
- Х.Муассан получает свободный фтор путем электролиза фтороводорода,
- химически и термически очень стойкий,
- соединения фтора применяются для: травления стекла, нанесения на нем надписей, изготовления тефлона, в ганице,
- фтор используется в атомной промышленности для очистки изотопов урана.
| SD |
- Получено Хамфри Дэви,
- польское название происходит от латинского слова sodanum - средство от головной боли,
- латинский символ и название происходит от natrun - стиральная сода,
- серебристо-белый, мягкий, легкий и очень реакционноспособный металл,
- загорается в воздухе,
- взрывается при контакте с водой,
- хранится в керосине,
- легче воды, мягкий - можно резать ножом,
- соединение натрия - хлорид натрия, это поваренная соль,
- форма сточных вод используется в ядерных реакторах и в производстве каучука,
- металлическая sd является хорошим проводником электричества.
| МАГНИЙ |
- официально открыт Дэви в 1808 г.,
г. - название происходит от города Магнезия в Малой Азии,
г. - светлый, серебристо-белый металл с блеском, быстро исчезающим на воздухе,
- второй по распространенности металл после бериллия,
- нагревается, бурно реагирует с кислородом, палец с белым, очень ярким пламенем,
- хороший проводник электричества,
- его соединения использовались в медицине две тысячи лет назад,
- легче алюминия, легко подвергается коррозии,
- "горький сл" - сульфат магния - слабительное,
- крупнейшим источником магния являются океаны, в 1 км3 содержится около 1,5 млн т,
- встречается в основном в соединениях - карбонатах, силикатах, хлоридах и сульфатах,
- в Польше месторождения солей магния находятся в Нижней Силезии,
- используется в производстве: деталей самолетов, двигателей, фотоаппаратов, пишущих машинок, ранее для производства фар,
- необходим зеленым растениям - компонент хлорофилла.
| ХЛОР |
- обнаружен Карлом В. Шееле при нагревании соляной кислоты с браунштейном, но оказался химическим соединением,
- в 1810 году сэр Хамфри Дэви доказывает, что он элемент и называет его хлором, от греческого слова khlros - зеленый,
- зеленый газ, 2,5 раза тишина с воздуха,
- сильно ядовитый газ с резким удушливым запахом,
- легко уплотняется,
- легко растворяется в воде,
- получен электролизом поваренной соли,
- очень реактивный элемент, не существует в природе в свободном состоянии,
- используется для: уничтожения бактерий, микроорганизмов, обеззараживания воды в водопроводах и бассейнах, в производстве пластмасс (напр.поливинилхлорид - ПВХ),
- наибольшее количество содержится в морской воде в виде хлорида натрия.
| СЕРА 9000 8 |
- название происходит от санскрита: sira - jasnes,
- другое название "сульфановое золото",
- элемент неметаллический, без вкуса и запаха, легковоспламеняющийся,
- при сжигании серы образуется газ с резким запахом,
- поставляется во многих аллотропных разновидностях,
- при его плавлении и затвердевании наблюдаются интересные эффекты - при фазовых переходах он проходит через несколько аллотропных разновидностей с разными свойствами, а после плавления затвердевает по-другому, не являясь точным обращением процесса плавления,
- очень важен для всех живых организмов как компонент белков,
- раньше использовался для религиозных ритуалов, для отпугивания злых духов, лечения болезней скелета и борьбы
с вредителями,
- в настоящее время используется для производства: пороха, горючих, взрывчатых веществ, серной кислоты, фосфорной кислоты, красителей, лекарств, удобрений, в резиновой промышленности, в качестве специального цемента и для лечения кожных заболеваний,
- месторождения серы в Польше были открыты в 1953 году в районе Тарнобжега.
| КАЛИЙ |
- открыт и назван Дэви в 1807 г.,
г. - название происходит от латинского kalium совы (alkali - от арабского al kalja - попи ролин, щелочь),
- очень легкий, мягкий металл = можно резать ножом,
- свежесрезанный, имеет серебристый цвет и яркий блеск, который очень быстро тускнеет из-за реакции с кислородом воздуха,
- очень реактивный элемент, - при контакте с водой мгновенно воспламеняется, краситель огненно-красно-фиолетовый,
- быстро окисляется на воздухе, хранится в керосине,
- является важным компонентом тканей растений и животных,
- большая часть находится в морской воде,
- соли калия применяются: в качестве удобрений, в мыловаренной и стекольной промышленности, для производства взрывчатых веществ,
- металлический калий используется в фотоэлементах - в звуковом кино, телевидении.
| МИЭД |
- известен с древних времен,
- используемые в производстве посуды, украшений, оружия, латуни и латуни,
- эпоха меди и ее сплавов продлилась до конца Средневековья,
г. - хорошо проводит электричество,
- характеризуется высокой теплопроводностью,
- широко применяется в электротехнике, автомобилестроении, авиации, радиотехнике, для производства проводов и деталей электрических машин,
- медные сплавы применяются в производстве боеприпасов, монет, клапанов, проушин, шестерен, подшипников, насосов, прецизионных оптических и художественных приборов,
- как один из микроэлементов потребляется человеком в количестве ок.100 мг в день (в виде растворимых солей),
- в Польше в 1957 г. Ян Выйковский обнаружил одну из самых богатых медных руд в Нижней Силезии недалеко от Любина.
| РТ |
- обнаружен в древности,
- самый редкий элемент в мире,
- известное как "живое серебро",
- температура замерзания -38,7 на С, температура кипения +357 на С,
- проглатываемая ртуть вредна для организма (включая пары ртути),
- в 16 веке Парацельс доказал, что его можно использовать в производстве лекарств;
- помогает в борьбе с микроорганизмами и паразитами, при лечении ран - как дезинфицирующее средство,
- Fafrenheit использовала ртуть в качестве жидкости для индикации индикаторов термометров,
- в настоящее время используются в ртутных барометрах, манометрах, кварцевых лампах, машинах для измерения артериального давления и т. д.,
- используется для т.н. огнеклевание как катализатор в производстве синтетического каучука,
- сейчас 1/3 мирового производства ртути используется для медицинских и химических целей, 1/5 - для производства взрывчатых веществ, 1/10 - для красок, 1/10 - для электроаппаратов.
Исследование на базе "Книги стихий" - Агнешка ПЕТШИКОВСКАЯ - IIIa класс; Конрад КРУ - класс IA
.
Монография, опубликованная World Scientific Publishing, доказывает эффективность генератора водорода и кислорода с небулайзером при лечении COVID-19
Вдыхание водорода и кислорода при лечении COVID-19, монография, обобщающая китайский опыт борьба с COVID-19, сообщает, что генератор кислорода водорода с небулайзером эффективен при лечении пациентов с коронавирусом COVID-19.
- Опубликовано профессором Сюй Кечэном, бывшим президентом -го Международного общества криохирургии, рецензировано и подготовлено Чжун Наньшанем, руководителем группы китайских экспертов высокого уровня по борьбе с пандемией COVID-19, монография официально опубликована World Scientific Publishing, Scientist Publishing и научные, технические и медицинские журналы, базирующиеся в Сингапуре.
Что может показаться неожиданностью Лечение Covid-19 вдыханием водорода было внедрено в Китае в марте прошлого года, тогда первая партия из 2000 единиц была отправлена в больницы по запросу правительства Китая.генераторы h3 (точнее, газы Брауна).
Они использовались и используются до сих пор в качестве первого и чаще всего достаточного лечения перед возможным подключением к аппарату искусственной вентиляции легких, что может объяснить чрезвычайно низкую смертность и почти 100% высокий уровень успеха лечения Covid-19 в Китае.
Китайские врачи лечат своих пациентов всеми видами терапии, запрещенными в Европе, США и Польше, включая гидроксихлорохин или будесонид, а также высокие дозы витамина D и инфузии «витамина С» и ДМСО.
Все эти процедуры лечения Covid-19 в Китае описаны и общедоступны для всех
на сайтах Министерства здравоохранения Китая.
История применения молекулярного водорода в медицине
Водород - самый легкий газ в мире и не оказывает токсического действия на человека (биобезопасность). Его можно использовать в качестве компонента уникальной газовой смеси для дыхания, а именно газа Hydreliox для глубоководных дайверов, который содержит 49 % H 2 , 50 % He и 1 % O 2 .
В 2007 году новаторское исследование профессора Осавы из Японии обнаружило, что селективные антиоксидантные свойства и терапевтические эффекты водорода при ишемии головного мозга. Позже в журнале Nature Medicine было опубликовано новое исследование, в котором было обнаружено, что H 2 может избирательно удалять токсичные свободные радикалы, такие как гидроксил (• OH) и пероксинитрит-анион (ONOO-), в культивируемых клетках, защищая клетки и значительно улучшая церебральную ишемию животных. реперфузионная травма (инсульт).
Это новаторское открытие открыло новую эру в водородной медицине и привлекло все больше и больше ученых-медиков к исследованиям в области биологии водорода. На сегодняшний день опубликовано около 1600 статей по водородной медицине, охватывающих показания, включая ишемическую реперфузию, повреждение трансплантата органов, нейродегенеративные заболевания, старение, сердечно-сосудистые заболевания, гипертонию, диабет, артрит, опухоли и т. д. В работе исследовались биологические эффекты.молекулярный водород, включая его влияние на нейтрализацию токсичных свободных радикалов in vivo, таких как гидроксильный радикал (-ОН) и нитратно-пероксидный анион (ONOO-), противовоспалительную и антиапоптотическую активность, а также способность регулировать клетки сигнализация.
Эффективность молекулярного водорода при лечении симптомов COVID-19
Патологически COVID-19 характеризуется воспалительным экссудатом в нижних дыхательных путях, включая мелкие бронхи и альвеолы.Многие исследования подтвердили, что терапевтический эффект водорода при заболеваниях в основном обусловлен его антиоксидантными, противовоспалительными, регулирующими клеточную сигнализацию и защитными клеточными эффектами. Кроме того, молекулярная масса смешанного водородно-кислородного газа чрезвычайно мала, а числа Рейнольдса, правило Бернулли и закон Грэма показывают, что водород может легко диффундировать и проникать через клеточную мембрану, поэтому он может увеличивать альвеолы для быстрого поглощения кислорода и уменьшают работу дыхания, улучшая тем самым использование кислорода без повреждения легочной ткани от избыточного давления.
Водород в лечении ковид-19 - Терапия также включена в Протокол диагностики и лечения новой пневмонии с коронавирусом (испытательные версии 7 и 8) и Протокол диагностики и лечения тяжелых и критических случаев новой пневмонии, вызванной коронавирусом (пробная версия 3), выпущенной Национальной комиссией здравоохранения и Государственным управлением традиционной китайской медицины.
В середине 2020 года медицинские эксперты из Первой дочерней больницы Медицинского университета Гуанчжоу сотрудничали с исследователями из 11 лучших больниц Китая для сбора патологических данных из больниц и провели фактические исследования терапевтических эффектов вдыхания водорода.кислородной смеси у пациентов с пневмонией COVID-19. Результаты подтвердили, что вдыхание смеси водорода и кислорода является одним из самых быстрых, безопасных и эффективных методов лечения этого заболевания.
Недавние публичные отчеты Национальной комиссии здравоохранения Китая и Китайского центра по контролю и профилактике заболеваний рекомендовали эффективные меры кислородной терапии в рамках общего лечения пациентов с новой коронавирусной пневмонией (COVID-19). 1, 2 Оба документа раскрывают экзотику и соотношение водорода и кислорода (66,6% H, 2 к 33,3% O 2 ) как состав газовой смеси для ингаляции. В то время как высокие уровни кислорода вводятся из-за очевидной дисфункции легких при COVID-19, смешивание с газообразным водородом для образования дыхательной смеси остается загадочным. Водород, скорее всего, добавляется в качестве инертной части дыхательного газа, но сам по себе может иметь полезные эффекты.
Недавнее исследование показывает, что газообразный водород подавляет воспаление дыхательных путей у пациентов с астмой 3 , что может уменьшить цитокиновый воспалительный шторм, наблюдаемый при COVID-19. 4 Два многоцентровых РКИ с ингаляционным водородом для COVID-19 внесены в Реестр клинических испытаний Всемирной организации здравоохранения (ВОЗ) в феврале и марте 2020 года, но до сих пор нет никаких доказательств в поддержку этого подхода. Также необходимо учитывать еще один фактор: способность водорода высокой концентрации вызывать взрыв из-за статического электричества.
Как и другие многообещающие (и срочно необходимые) лекарства от COVID-19, газообразный водород требует ускоренных, но тщательных исследований и путей утверждения с достаточными гарантиями эффективности и безопасности. 5 Отрезание рогов простейшей молекуле во Вселенной может стать шагом назад для сообщества исследователей водорода, помимо этого конкретного коронавируса.
Вклад авторов
Сергей М. Остойич: Концептуализация; Хранилище данных; Формальный анализ; Расследование; администрирование проекта; Надзор; Проверка; Оригинальный проект; Написание, проверка и редактирование.
Заявление о конфликте интересов
Автор заявляет об отсутствии конфликта интересов.
Финансирование
Автор не получал никакой финансовой поддержки для исследования, авторства и/или публикации данной статьи.
СООБЩЕНИЯ, ПРЕДСТАВЛЕННЫЕ ОТ
ШАНХАЙ, 11 ноября 2020 г. / PRNewswire / — Asclepius Meditec («Компания») рада сообщить, что генератор водорода и кислорода с распылителем — респираторное медицинское устройство, разработанное Компанией для борьбы с коронавирус, был представлен в монографии под названием «Ингаляции водорода и кислорода в лечении COVID-19».Планируется, что издание World Scientific Publication от 14 ноября -го -го года подчеркнет эффективность генератора водорода с распылителем в облегчении симптомов пневмонии COVID-19 и пояснит, что вдыхание водородно-кислородной смеси может уменьшить тяжесть пневмонии. заболевания и одышки у больных COVID-19 и сократить сроки их госпитализации.
Монография, опубликованная World Scientific Publishing, доказывает эффективность генератора водорода и кислорода Asclepius Meditec с небулайзером при лечении COVID-19 19.Компания Asclepius Meditec пожертвовала генератор водорода и кислорода с распылителем регионам, наиболее пострадавшим от COVID-19
Компания Asclepius Meditec разработала генератор водорода и кислорода с распылителем, полученный в 2020 году Национальный сертификат инновационного медицинского устройства класса III от NMPA (Китайское национальное управление медицинской продукции) другой вехой в истории водородно-кислородной медицины. В настоящее время прибор прошел тесты соответствия медицинских изделий в ЕС, в том числе на безопасность, электромагнитную совместимость, биосовместимость и т.д.Вскоре он должен пройти сертификацию CE. Тем временем устройство запрашивает у FDA разрешение на использование в чрезвычайных ситуациях (EUA).
Электронная версия монографии на английском языке опубликована 16 октября. Чтобы приобрести цифровую и физическую копию монографии, посетите https://www.worldscientific.com/worldscibooks/10.1142/11910
(PDF) Обзор инфекции SARS-CoV-2 (COVID-19) и Важность молекулярного водорода в качестве дополнительной терапии (researchgate.net) — Вдыхание смеси водорода и кислорода становится новым противовирусным препаратом для лечения COVID-19
Согласно данным, опубликованным на веб-сайте ВОЗ, более 46 миллионов человек дали положительный результат для COVID-19, из которых более 1 миллиона пациентов в более чем 200 округах умерли от этого заболевания по состоянию на 2 ноября na , 2020.Однако по мере распространения нового коронавируса ВОЗ SOLIDARITY показала, что многие многообещающие методы лечения COVID-19, такие как ремдесивир, гидроксихлорохин, лопинавир и интерферон, практически не действуют на госпитализированных пациентов с COVID-19.
В то время как мир сталкивается с острой нехваткой конкретных противовирусных препаратов, новая терапия от Asclepius Meditec подчеркивает потенциал водородно-кислородной терапии в борьбе с COVID-19 . В сочетании с реальными исследованиями (RWS), а также медицинскими теориями и клиническими случаями, монография обобщает, с точки зрения лечения, опыт врачей из различных регионов Китая в изучении использования дополнительной водородно-кислородной терапии при легкой степени тяжести. , среднетяжелых, тяжелых и критических больных на уровне вывода.
В монографии показано, что после нескольких часов вдыхания от 3 до 6 литров водородно-кислородной смеси почти у всех больных отмечалось ровное дыхание, легкий кашель и полипней. Через 1-2 дня лечения пациенты отмечали уменьшение болей и давления в груди, улучшение показателей физического здоровья и достоверно более короткие средние сроки госпитализации по сравнению с пациентами, не применявшими ингаляцию газоводородной смеси.
Кроме того, в другой научной статье под названием « Вдыхание смеси газов с водородом и кислородом улучшает тяжесть заболевания и одышку у пациентов с коронавирусной болезнью 2019.В недавнем многоцентровом открытом клиническом исследовании», , опубликованном в Journal of Thoracic Disease, также сообщается, что небулайзерный генератор водорода и кислорода в качестве адъювантной терапии у пациентов с COVID-19 может сократить продолжительность пребывания в больнице. Статья отправлена и находится на рассмотрении.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7459175/
С большим интересом читаем последнюю статью Wang, et al., 90 134 1, в она было показано, что однократное 45-минутное вдыхание газообразного водорода (КСЕН) уменьшало воспаление дыхательных путей у пациентов с астмой и хронической обструктивной болезнью легких (ХОБЛ), в основном за счет ингибирования провоспалительных цитокинов моноцитарного хемотаксического белка-1 (МСР-1), интерлейкина-1. 4 (Ил-4) и Ил-6.Также было обнаружено, что высокие уровни IL-6 тесно связаны с наличием определяемой вирусной нагрузки коронавируса 2 (SARS-CoV-2) в сыворотке крови с тяжелым острым респираторным синдромом и жизненными показателями пациентов с 2019 г. (COVID-19). с коронавирусной болезнью. 2 , 90 062 3 По состоянию на 14 сентября 2020 г. было зарегистрировано 28 637 952 подтвержденных случая заболевания COVID-19, из которых 917 417 человек умерли в 212 странах мира, 90 062 4 и COVID-19 вызвали беспрецедентный глобальный ущерб для общественного здравоохранения. кризис. 5 Однако на сегодняшний день эффективные терапевтические подходы или противовирусные препараты для лечения COVID-19 остаются ограниченными. 6
Водород (H 2 ) не имеет цвета и запаха и является самой легкой молекулой газа во Вселенной. С тех пор как водородная терапия была впервые описана на коже, модель рака у мышей из исследования, проведенного за последние 10 лет, показала, что H 2 оказывает терапевтическое действие на различные модели животных и заболевания человека, включая метаболический синдром, повреждение органов (дыхательная система, нервная система, репродуктивная система и др.), радиационное повреждение и рак, от острого до хронического заболевания. 7 , 8
Мы предполагаем, что ингаляционно-водородная терапия может быть эффективным и инновационным дополнительным методом лечения COVID-19 и обладает полезным потенциалом для предотвращения цитокинового шторма, связанного с COVID-19, и повреждения многих органов. за счет использования нескольких механизмов. 8 Во-первых, H 2 , как важный физиологический регулирующий агент с антиоксидантным действием на клетки и органы, может активировать сигнальный путь, связанный с эритроидным фактором 2 (Nrf2), обеспечивать цитопротекторную активность и уменьшать повреждение тканей, вызванное SARS-CoV -2 инфекция. 9 , 10 Кроме того, окислительный стресс при вирусных инфекциях может усугубить дефект метилирования ДНК, что может привести к дальнейшему высвобождению ангиотензинпревращающего фермента 2 (ACE2, функционального рецептора вирусного шиповидного гликопротеина, который позволяет SARS- CoV-2 для проникновения в клетки)) гипометилирование и усиленная виремия. 11 H 2 в качестве антиоксиданта, 8 может подавлять экспрессию ACE2 посредством эпигенетического контроля гена ACE2.
Во-вторых, активация апоптоза, вызванная SARS CoV-2, и передача сигналов белка 53 (53) по пути лимфоцитов могут играть важную роль в развитии лимфопении у пациентов, 12 , а H 2 могут оказывать анти- апоптотический эффект лимфоцитов объясняется их способностью поглощать свободные радикалы, что может предотвратить прогрессирование заболевания и может использоваться для профилактики и лечения пациентов с COVID-19. 13 И последнее, но не менее важное: H 2 может подавлять экспрессию провоспалительных генов (фактор некроза опухоли-α, IL-1β, IL-6, IL-10 и молекула межклеточной адгезии-1) посредством ядерного фактора каппа-энхансера Путь активированной легкой цепи В-клеток (NF-κb), в то время как эти провоспалительные цитокины могут быть сверхэкспрессированы при инфекции COVID-19 и играть важную роль в развитии заболевания. 14 , 15
Таким образом, с последствиями для селективных антиоксидантных, антиапоптозных, противовоспалительных, изменений экспрессии генов и в качестве газообразного сигнального модулятора 8 терапия Вдыхание водорода может быть новым, многообещающим и эффективное поддерживающее лечение до COVID-19.
Водородная терапия и ингаляционное (дыхательное) лечение – каковы преимущества водородной терапии – ингаляция водородом h3?
Благодаря широкому спектру действия использование водорода дает много положительных эффектов.среди прочего:
Записаться на прием.
Коронавирусная терапия медицинским газом
Можно ли предотвратить и вылечить вирус COVID-19 с помощью ингаляционной терапии молекулярным водородом?
Водородная терапия при Covid-19: видео и справочники
.Газ Брауна для здоровья: история, наблюдения и медицинские данные
Благородный газ, химический элемент с символом He , от лат. гелий - от греческого бога солнца Гелиоса.
Это второй по распространенности элемент во Вселенной после водорода. У него самая низкая температура замерзания -268,93°С, а застывает он только при повышенном давлении (абсолютный ноль минус 273,15°С).
На Земле встречается только в следовых количествах.
Существование этого бесцветного негорючего газа без запаха, примерно в 7 раз легче воздуха, было впервые обнаружено на Солнце во время затмения 18 августа 1868 года в Гунтуре, Индия.
Французский астроном Пьер Янссен, изучая спектр солнечной короны, наблюдал оранжевую полосу, которую нельзя было отнести ни к одному из известных в то время элементов, хотя первоначально считалось, что это натрий.
В том же году, 20 октября 1868 года, английский астроном Норман Локьер подтвердил наблюдение.
Долгое время считалось, что гелий присутствует на Солнце, но не на Земле.
Только в 1895 году Уильям Рамзи выделил гелий в экспериментальных условиях после обработки клевита (урановой руды) серной кислотой.
В том же году Теодор Клеве и Абрахам Ланглет в Швеции выделили гелий и определили его атомную массу.
Как самый легкий безопасный газ (благородный), им заправляли летательные аппараты, которые легче воздуха, т.е. аэростаты (воздушные шары, дирижабли).
В настоящее время гелий используется, когда необходимы чрезвычайно низкие температуры из-за его очень низкой температуры кипения. Он используется, в том числе, в для охлаждения сверхпроводников.
Получают в основном из природного газа, богатого этим элементом (месторождения, в том числе, в США), или при переработке сжиженного воздуха методом фракционной перегонки
.