В данном обзоре рассмотрим простую технологию меднения стали в домашних условиях без использования электричества.
Для этого нам потребуется кислотный электролит для аккумуляторов и медный купорос.
Советуем также прочитать на досуге: как быстро и легко очистить заготовки из металла от ржавчины.
В подготовленную емкость насыпаем медный купорос. Затем вливаем струйкой кислотный электролит. Все хорошо перемешиваем.
Соотношение компонентов — 1:3. То есть на 30 мл медного купороса потребуется 90-100 мл электролита.
В качестве испытуемого образца, который будем покрывать слоем меди, автор использует стальное сверло.

Желательно, чтобы деталь имела гладкую поверхность. Для этого ее необходимо хорошо зачистить (при возможности — отполировать). Также деталь надо обезжирить и высушить.
Погружаем сверло в раствор медного купороса на несколько секунд, и уже виден первый результат.

Если же подержать сверло в растворе немного дольше, то медная «корка» на его поверхности будет более выраженной.
Ну и, соответственно, погружаем сверло в раствор столько раз, пока результат вас полностью не устроит (но больше 3-4 слоев делать не нужно).
Причем для более качественного результата рекомендуются первый слой меди стирать, и делать меднение дальше.
При работе обязательно нужно использовать средства индивидуальной защиты — перчатки и очки.
Вообще рекомендуется разбавлять электролит дистиллированной водой, но в данном случае автор не стал этого делать, и результат получился вполне достойным.
Данный обзор подготовлен на основе авторского видеоролика с YouTube канала «Всё о сварке и самоделках».
https://youtu.be/gMCfSsD-X2o
Мне нравитсяНе нравится
Андрей Васильев
Задать вопрос
Когда речь идет о гальванотехнике, сразу же на ум приходят такие технологические операции, как хромирование и цинкование металлоизделий. Но если задать вопрос, а что представляет собой гальваностегия, то ответит не каждый – проверено. Хотя ничего сверхнового данный термин не подразумевает.
Проще говоря, это методика покрытия тончайшим слоем металла любого материала, будь-то сталь, алюминий, древесина или пластик. С тем, как произвести меднение какого-либо образца в домашних условиях, мы и разберемся.
 Меднение – методика отчасти более универсальная, чем то же цинкование. Для каких целей оно проводится?
Меднение – методика отчасти более универсальная, чем то же цинкование. Для каких целей оно проводится?
Вряд ли читателя заинтересуют такие нюансы, как классификация меди (рафинированная, бескислородная, общего применения), различные варианты растворов, использующихся при меднении, характеристики материалов и подобные вещи. Далее рассмотрены лишь простейшие методы нанесения Cu на любую поверхность, которые несложно организовать в домашних условиях, без каких-либо сложностей и финансовых затрат.
Такая методика подходит лишь для покрытия слоем Cu металлических деталей. По сути, технология мало чем отличается от того же цинкования в домашних условиях.
Оборудование понадобится простейшее:
Ванночка (емкость) стеклянная. Ее вместительность определяется габаритами обрабатываемой детали. Даже литровая банка или стакан – как варианты.

Медные электроды. Как правило, используются два. Это позволяет более качественно покрыть заготовку слоем со всех сторон и упрощает сам процесс. По ходу работы не придется периодически менять положение детали относительно электрода. Что именно использовать, зависит от конкретной ситуации – пластины из меди, куски толстой проволоки. Это непринципиально.
Источник тока и соединительные провода. Достаточно даже маломощного блока питания, на 6 – 8 В. Если в БП нет встроенного амперметра и не предусмотрена плавная регулировка напряжения, то придется использовать соответствующий прибор и реостат как отдельные элементы электрической цепи. Примерная схема, которую собирают для меднения деталей, показана на рисунке.
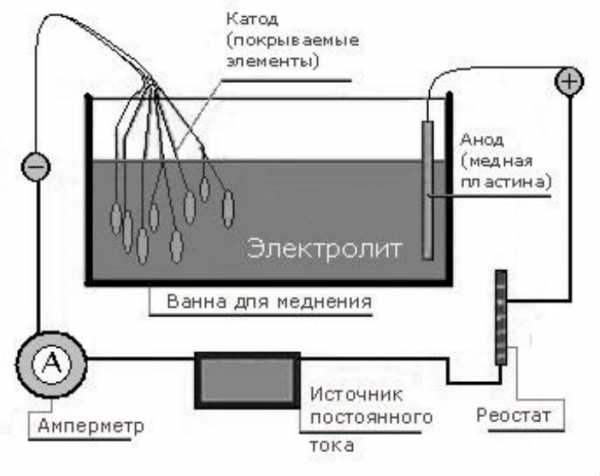
Электролит. Можно использовать покупной раствор, хотя придется и поискать. Если же его готовить самому, то на 100 мл воды дистиллированной понадобится серная кислота (3 мл) и медный купорос (20 г) – не дефицит.
После включения напряжения величина тока постепенно повышается до расчетного значения, и в таком режиме обработка осуществляется в течение ⅓ часа (время ориентировочное). Если меднение проводится впервые, то следует контролировать данный процесс. О том, что деталь можно вынимать из емкости, судят по оттенку ее поверхности и равномерности покрытия (отсутствию необработанных участков, раковин, вкраплений и так далее).
Остается лишь смыть с образца остатки электролита и просушить. Получается, что эта технология для реализации в домашних условиях никакой сложности не представляет.
Данным способом можно наносить металлическое покрытие на любые материалы. Суть заключается в «обмазке» (без прямого контакта) заготовки электролитом специальной кисточкой, щетинки которой – медные проволочки. Недостаток этой технологии в том, что добиться качественного меднения рельефных поверхностей вряд ли удастся. По крайней мере, понадобится много времени и усилий, чтобы тщательно обработать все «щели» и «выбоины».
Кисточка. В домашних условиях ее делают из многожильного медного проводника. Снять изоляцию и «распушить» один его конец – не проблема. Чтобы было удобнее работать, стоит подумать, из чего изготовить рукоятку кисточки. Ею придется водить по поверхности образца, а с учетом того, что провода гибкие, такое меднение станет испытанием для мастера. Как вариант – подвязать «рабочую часть» к карандашу, пластиковому корпусу шариковой ручки. Догадаться несложно.
Тара. Деталь перед меднением укладывается на любую подходящую посуду. Для удобства работы она не должна иметь высоких бортиков. Оптимальный вариант – тарелка. Плюс к этому – емкость, в которой будет электролит. В нее придется постоянно опускать кисточку, поэтому и здесь выбор не затруднен. Подойдет и стакан, если образец небольшой и раствора понадобится немного. Соответственно, вся тара предварительно обрабатывается – моется, чистится, кипятится, обезжиривается.
Сборка схемы. Аналогично предыдущему способу. Кисточка выполняет функцию анода, поэтому ее к «+» БП, а покрываемая деталь является катодом (к «–»).
Для обеспечения неразрывности электрической цепи в посуду наливается электролит, так, чтобы его уровень превышал высоту детали. Кисточкой, которая периодически также обмакивается в растворе (для этого он и заливается в отдельную тару), необходимо водить по-над образцом. В результате его поверхность покрывается слоем меди. По сути, производится ее напыление.

Понятно, что такой процесс в исполнении более сложный, так как проводится в «ручном» режиме. Необходимо постоянно следить, чтобы между кистью и обрабатываемой основой был небольшой зазор. Но и это не главное. Его неизменность – одно из условий равномерности покрытия.
В каких случаях целесообразно использовать такой способ меднения
Как определить требуемые параметры блока питания? Для плотности тока при меднении нормой считаются 0,5 А/дм² образца, который предстоит покрыть защитным слоем.
Медь довольно быстро окисляется. Перед началом процесса обработки изделия электроды следует хорошо зачистить.
Время выдержки детали в растворе выбирается исходя из того, какой толщины слой необходимо получить при меднении. Зависимость прямая – чем дольше идет обработка, тем толще покрытие.
При необходимости восстановления внешнего вида истершихся элементов фурнитуры (мебельной или иной) их меднение – неплохой выход из положения.
Автор не единожды сталкивался с тем, что люди, озабоченные проблемами экологии, сразу же задаются вопросом – а как в домашних условиях организовать утилизацию отработки? Ведь электролит не вечен, и использовать его всю жизнь точно не получится. Кстати, вполне резонное и более чем справедливое замечание.
Есть неплохое решение – собирать оставшуюся после меднения «бурду» в отдельной стеклянной емкости. Зачем? Пригодится. Этот раствор отлично подходит для обработки древесины. Ваш покорный слуга, читатель, сам пропитывал им лаги перед настилом полов на даче. Учитывая, что зимой она не отапливается, условия эксплуатации материала понятны. Когда спустя 12 лет потребовалось переложить половицы, выяснилось, что лаги – как новенькие. Не было даже малейшего намека на какую-то плесень, следы гнили.
Так как любому из нас приходится заниматься если не строительством, то уж ремонтом обязательно, нет смысла куда-то потихонечку, подальше от сторонних глаз, сливать использованный электролит. Не по-хозяйски это.
Благодаря своим многочисленным преимуществам данный металл получил широкое распространение. На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
Для этого понадобится:
Гальваническое меднение в домашних условиях
Медный купорос
Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора в соляную кислоту. После приготовления раствора медного купороса его следует тщательно размешать, чтобы не было частиц. Далее нужно соляную кислоту тонкой струйкой добавить в этот раствор. Не следует забывать про технику безопасности и использовать перчатки и защитные очки. После того, как вы добавили в раствор соляную кислоту, его следует тщательно перемешать.
Итак, раствор готов и можно приступать к меднению в домашних условиях. Для этого нужно взять металлическую деталь, на которую вы собрались наносить слой меди и подготовить ее к работе. Подготовка включает в себя ее обработку наждачной бумагой. Данная процедура позволяет не только зачистить металлическую поверхность, но и обезжирить ее. Такая же процедура будет актуальна и для детали из латуни или свинца. После этого, покрытие нужно тщательно промыть в растворе кальцинированной соды. Это позволит более тщательно обезжирить материал.

Кальцинированная соды для обезжиривания материала
Далее поверхность нужно погрузить в раствор медного купороса и соляной кислоты. Следует обратить внимание на то, что первый слой меди является очень тонким и слабым, поэтому его желательно снять при помощи металлической щетки. После того, как вы это сделали, поверхность стали или свинца следует повторно промыть в растворе кальцинированной соды и опять погрузить в раствор для меднения. Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
Этот способ позволяет сделать очень качественное медное покрытие, которое можно снять только наждачкой. Для улучшения медного покрытия в домашних условиях следует деталь еще раз погрузить в раствор. Указанный способ отличается своей простотой и высокой эффективностью в том числе и для изделий из свинца.
Меднением принято называть процедуру гальванического нанесения меди, толщина слоя меди в таких случаях может составлять-от 300 мкм и больше. Меднение стали это один из наиболее важных процессов в гальванике, поскольку используется, как дополнительный процесс перед нанесением других металлов для хромирования, никелирования, покрытие серебром.
Слой меди прекрасно держится на стали и способен выравнивать различные дефекты на поверхности.
Для медных покрытий характерно высокое сцепление с другими поверхностями, изделиями из свинца особенно металлическими, а также высокая электропроводность и пластичность. Нанесенное недавно покрытие имеет ярко-розовый матовый или же блестящий цвет. Под воздействием влияний атмосферы медные покрытия могут окисляться, покрываться налетом окислов с различными пятнами радужного вида.
 Как правило, гальваническое омеднение может использоваться:
Как правило, гальваническое омеднение может использоваться:
Меднение происходит вместе с нанесением других гальванических покрытий
Первый способ предполагает обработку металлического изделия наждачной бумагой, щеткой и промывки водой. После чего обезжиривания в горячем содовом растворе с повторной промывкой. Далее в стеклянную емкость опускают на медных проволочках две медные пластины –аноды. Между пластинками на проволоке подвешивают деталь, после чего пускается ток.
Второй способ актуальный для изделий из стали, алюминия и цинка.
Данная процедура актуальна для различных случаев, поскольку нанесение слоя меди может использоваться для алюминиевых столовых приборов, сувениров, подсвечников и т. д. Неповторимый эффект оказывают изделия не из металла, на которые был нанесен слой меди. Это могут быть стебли растений, листья и др. Ввиду того, что в покрываемых предметах отсутствует токопроводящий слой, вместо него используется специальный электропроводный лак, который наносят на поверхности.
В состав лака входит ряд органических растворителей, пенкообразователей и тонкодисперсионный графитовый порошок, благодаря которому создается электропроводность. Лак наносят тонким слоем на сухую поверхность, и после высыхания через час можно приступать к омеднению. При желании можно меди придавать различные цветовые оттенки, используя для этого специальные способы. Высокое качество и уникальность таких изделий вполне заслуженно приравнивается к настоящим ювелирным украшениям.
Процесс меднения металлических изделий называется гальваностегией. Он основан на осаждении на поверхность деталей другого металла, растворимого в специальной жидкости.
Технология омеднения включает изготовление раствора и создание разноименных электродов. В процессе гальваностегии, ионы меди, растворенные в электролите, притягиваются отрицательным полюсом (обрабатываемая деталь) на свою поверхность.
Омеднение различных деталей в промышленных масштабах применяется не только, как конечный процесс обработки поверхности металлических изделий. Он может использоваться для подготовки деталей к следующей операции, например, никелированию, серебрению или хромированию изделий.
Эти металлы плохо осаждаются на поверхность стальных деталей, а на омедненную поверхность ложатся очень хорошо. В свою очередь медь, осевшая на стальные детали, держится прочно и способствует выравниванию различных дефектов на ее поверхности.
Для металлических деталей можно выполнить меднение в домашних условиях. Рассмотрим меднение, с опусканием детали в раствор с электролитом. Для этого необходимо иметь:
Порядок работы
Второй способ меднения в домашних условиях металлических изделий, подразумевает выполнение этого процесса без опускания обрабатываемой детали в раствор электролита.
Этот вариант подходит для нанесения покрытия на цинковые и алюминиевые изделия.
Порядок работы
Медь - это один из древних металлов: люди начали применять ее для создания орудий труда еще в 4 тысячелетии до нашей эры. Такое широкое распространение меди объяснимо тем, что вещество встречается в природе в металлическом самородном состоянии. И сегодня медь используется повсеместно - в металлургии, автомобильной промышленности, электротехнике и строительстве.
Металлическая медь представляет собой тяжелый металл розово-красного цвета, ковкий и мягкий, который плавится при температуре больше 1080 градусов по Цельсию, очень хорошо проводит теплоту и электрический ток: электропроводимость меди выше в 1,7 раза, чем алюминия и больше в 6 раз выше, чем железа, и только немного уступает электропроводимости серебра.
Специфические особенности меди определяются содержанием в металле конкретных примесей, количество которых может различаться приблизительно в 10 - 50 раз. По содержанию кислорода принято использовать следующую классификацию меди:
В меди кроме кислорода может присутствовать водород, который в металл попадает в процессе электролиза или при совершении отжига в атмосфере, которая содержит водяной пар. При высокой температуре водяной пар разлагается с формированием водорода, который в медь легко диффундирует.
Атомы водорода в бескислородной меди размещаются в междоузлиях кристаллической решетки и на свойствах металла особо не сказываются. В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с закисью меди, при этом образуется в толще меди водяной пар, которому присуще высокое давление, что приводит к вздутиям, трещинам и разрывам. Это явление носит название «водородная болезнь».
Железо, висмут, сурьма и свинец ухудшают пластичность меди. Примеси, что являются малорастворимыми в меди (свинец, кислород, сера, висмут), провоцируют хрупкость при высокой температуре, что затрудняет процесс горячей обработки давлением.
Основное свойство меди, определяемое её использование, - высокая электропроводность или малое удельное электрическое сопротивление. Подобные примеси как железо, фосфор, мышьяк, олово и сурьма, значительно ухудшают её электрическую проводность. На величину электропроводности оказывает большое влияние механическое состояние меди.
Второе важное свойство меди - значительная теплопроводность. Легирующие добавки и свойства уменьшают теплопроводность меди, поэтому созданные на медной основе сплавы самой меди значительно уступают по этому показателю.
Медь при нормальных температурах является коррозиционно устойчивой в таких средах, как пресная вода, сухой воздух, морская вода при небольшой скорости движения воды, неокислительные кислоты и растворы соли при отсутствии кислорода, сухие галогенные газы, щелочные растворы за исключением солей аммония и аммиака, органические кислоты, фенольные смолы и спирты.

В аммиаке, хлористом аммонию, окислительных минеральных кислотах и растворах кислых солей медь не устойчива. Её коррозионные свойства также заметно ухудшаются в некоторых средах с возрастанием количества примесей. Допускается контакт меди с её сплавами, с оловом, свинцом во влажной атмосфере, морской и пресной воде. В то же время контакт меди с цинком и алюминием не допускается вследствие их быстрого разрушения.
Медь, ее сплавы и соединения нашли широкое применение в разных отраслях промышленности. Медь в электротехнике используют в чистом виде в производстве шин контактного и голого проводов, кабельных изделий, электрогенераторов, телефонного оборудования и радиоаппаратуры. Из меди изготавливают вакуум-аппараты, теплообменники и трубопроводы.
Сплавы меди с различными металлами используют в автомобильной промышленности и для изготовления химических аппаратов. Проволока из красной меди изготовления всевозможных шнуров и выгибания самых сложных элементов. Высокие свойства меди делают ее незаменимой при производстве филигранных деталей.
Меднением называют процедуру гальванического нанесения меди, толщина слоя которой составляет 1 - 300 мкм и больше. Меднение стали является одним из важнейших процессов в гальванике, что применяется в качестве предварительного процесса при подготовке металлической поверхности для покрытия другими металлами - при хромировании, никелировании и покрытии серебром, а также как законченный самостоятельный процесс.
Использование меднения как подготовительной манипуляции связано с тем, что этот металл способен очень прочно держатся на стали, выравнивать дефекты поверхности. Другие материалы на медь хорошо осаждаются, а вот на чистую сталь - не очень.

Медные покрытия характеризуются высоким сцеплением с разными металлами, высокой электропроводностью и пластичностью. Их принято наносить на стальные, цинковые и алюминиевые детали.
Только что нанесённое покрытие меди имеет ярко-розовый матовый или блестящий цвет, зависимо от технологии нанесения. Медные покрытия в атмосферных условиях способны легко окисляться и покрываться налетом окислов, приобретая пятна различных оттенков и радужные разводы.
В большинстве своем гальваническое меднение металлов используют в таких случаях:

Меднение применяется в сочетании с прочими гальваническими покрытиями:
Процедура меднения своими руками доступна для выполнения даже новичками. Для этого достаточно только знать её основные тонкости. Существует два способа меднения в домашних условиях: с погружением в электролит и без погружения.
Металлическое изделие обрабатывают наждачной бумагой для удаления оксидной пленки, протирают щеткой, промывают как следует водой, обезжиривают в горячем содовом растворе и промывают еще один раз. После этого принято опускать в стакан или банку на медных проволочках две медные пластинки, которые являются анодами.
Между пластинками подвешивают на проволочке деталь. Проволочки, идущие от медных пластинок, соединяют вместе и подключают к плюсу источника тока, а деталь - к минусу. После этого в цепь включается реостат для регулировки тока и миллиамперметр. Необходим источник постоянного тока, который имеет напряжение не больше 6 В.
Для меднения дома нужно приготовить следующий раствор электролита. Возьмите 20 грамм медного купороса и 2-3 миллилитра серной кислоты на 100 миллилитров воды и налейте в посуду. Следите, чтобы данный раствор полностью покрыл электроды.
При использовании реостата нужно установить ток в пределах 10 - 15 мА на каждый сантиметр квадратный поверхности детали. Где-то через 20 минут следует выключить ток и вынуть изделие, оно уже покрылось тонким медным слоем. Чем дольше будет идти процесс, тем слой меди получится толще.
Данную процедуру проводят для стали, алюминия и цинка. С одного конца многожильного провода снимают изоляцию, затем необходимо растеребить тонкие медные проволочки для получения медной кисти. Для удобства работы необходимо привязать ее к медной кисти или деревянной палочке, а другой конец кабеля нужно подсоединить к плюсу источника тока.
Дальше следует приготовить электролит - раствор медного купороса, лучше слегка подкисленный, и налить в широкую склянку, в которую кисть будет удобно макать. Подготовьте металлическую пластинку или какой-то другой маленький предмет с плоской поверхностью. Его нужно протереть с помощью мелкой наждачной шкурки и обезжирить посредством кипячения в растворе стиральной соды.

Затем необходимо положить пластинку в кювету или ванночку и подсоединить ее с помощью провода к минусу источника тока. После того, как схема собрана, вам следует только ввести электролит. Обмакните в раствор медного купороса «кисть», которой следует провести вдоль пластинки, не дотрагиваться до поверхности.
Рекомендуется работать так, чтобы между кистью и пластинкой всегда располагался слой электролита. Все время работы проводки должны быть смоченными раствором. Пластинка на глазах будет покрываться слоем металлической меди красного цвета. Для обработки маленькой детали понадобятся считанные минуты.
Когда вы нанесли покрытие, нужно высушить на воздухе деталь и натереть матовый слой меди до блеска с помощью суконной или шерстяной тряпки. Процесс меднения алюминия, когда изделие в электролитическую ванну не опускают, а обрабатывают небольшими участками снаружи, добавляя электролит, применяют в таких случаях, когда изделие настолько велико, что для него нельзя подобрать подходящую ванны.
Установки для меднения от обыкновенных гальванических ванн ничем не отличаются. Электролиты для меднения довольно просто получить, если иметь под рукой необходимые ингредиенты. Бывают два вида медных растворов: щелочные и кислые.
В кислых растворах вы не сможете получить хорошо сцепленные покрытия из меди на цинковых и стальных изделиях, потому что цинк и железо в этом случае растворяются с медью, и нарушается сцепление с защитным покрытием.
Для устранения данной особенности рекомендуется первый тонкий медный слой (2—3 мкм) создать в щелочном растворе для меднения, а в будущем наращивать покрытие до заданной толщины в кислом электролите, который является более экономичным. Цинковые изделия, что имеют сложную форму, лучше всего меднить в щелочных электролитах.

Самыми распространенными кислыми электролитами являются борфтористоводородные и сернокислые. Наибольшее использование нашли сернокислые электролиты, которые отличаются простотой состава, высоким выходом по току и значительной устойчивостью.
Перед меднением деталей из стали в кислых электролитах их рекомендуется предварительно меднить в цианистом электролите или осаждать тонкий подслой никеля. Данные электролиты имеют несколько недостатков.
Один из них состоит в невозможности непосредственного покрытия цинковых и стальных деталей из-за контактного выделения меди, которая имеет плохое сцепление с металлом основы. Также электролиты незначительную рассеивающую способность и более грубую структуру осадков по сравнению с прочими электролитами.
Среди щелочных электролитов меднения известны пирофосфатные и цианистые электролиты.
Цианистые электролиты из меди характеризуются высокими рассеивающими способностями, возможностью проведения меднения столярных изделий и мелкокристаллической структурой осадков.
К недостаткам щелочных электролитов относят низкую плотность тока и неустойчивость раствора вследствие карбонизации под действием двуокиси углерода свободного цианида. Помимо этого, цианистые электролиты отличаются уменьшенным выходом по току - не больше 60-70%.
Таким образом, медь является металлом, который используется повсеместно: в автомобильной промышленности, электротехнике и строительстве. А в гальванопластике известна технология меднения для подготовки металлической поверхности под покрытие другими металлами или как самостоятельный процесс.
Медные покрытия, как правило, не применяются в качестве самостоятельного покрытия ни для декоративных целей, ни для защиты стальных деталей от коррозии. Это связано с тем, что медь в атмосферных условиях легко окисляется, покрываясь налетом окислов.
Однако благодаря хорошему сцеплению осажденной меди с различными металлами медное покрытие применяется в многослойных защитно-декоративных покрытиях в качестве промежуточного подслоя, а также для защиты стальных деталей от цементации. В гальванопластике медные осадки применяются для изготовления металлических копий, барельефов, волноводов и матриц.
Электролиты меднения подразделяют на кислые и щелочные. Из кислых электролитов используют сернокислые и борфтористоводородные. Наибольшее применение нашли сернокислые электролиты, отличающиеся простотой состава, устойчивостью и высоким выходом по току (до 100%). Недостатком этих электролитов является невозможность непосредственного покрытия стальных и цинковых деталей вследствие контактного выделения меди, имеющей плохое сцепление с основным металлом. Поэтому перед меднением стальных детален в кислых электролитах их предварительно меднят в цианистых электролитах или осаждают тонкий подслой никеля. К недостаткам сернокислых электролитов относятся также их незначительная рассеивающая способность и более грубая: структура осадков по сравнению с другими электролитами.
К щелочным электролитам меднения относятся цианистые, пирофосфатные и другие электролиты. Цианистые медные электролиты обладают высокой рассеивающей способностью, мелкокристаллической структурой осадков, возможностью непосредственного меднения стольных деталей. К недостаткам относятся низкая плотность тока и неустойчивость состава вследствие карбонизации свободного цианида под действием двуокиси углерода воздуха. Кроме того, цианистые электролиты характеризуются пониженным выходом по току (не более 60-70%).
Будьте внимательны! Компания «ЛВ-Инжиниринг» не предоставляет услуги по нанесению гальванических покрытий! Наша организация осуществляет проектирование гальванических производств, изготовление гальванических ванн и линий из полипропилена, монтаж и пусконаладочные работы по данному направлению.
Кислые электролиты меднения
Медь сернокислая - 150-250 г/л
Никель хлористый - 50-70 г/л
Температура = 18-25°С
Плотность тока = 1-4 А/дм 2
При перемешивании электролита сжатым воздухом можно довести катодную плотность тока до 6-8 А/дм 2 .
Для приготовления сернокислого электролита меднения растворяют медный купорос, фильтруют его в рабочую панну и при непрерывном помешивании добавляют серную кислоту.
При нанесении медных покрытий из сернокислого электролита медные аноды растворяются в основном с образованием двухвалентных ионов, которые, разряжаясь на катоде, осаждаются в виде металлической меди. Однако наряду с этими процессами происходят п другие, нарушающие нормальное течение электролиза. Возможно также анодное растворение с образованием одновалентных ионов, хотя и в меньшей степени.
В электролите, омывающем металлическую медь, идет также химический обратимый процесс: Cu + Cu 2+ = 2Cu + .
Накопление в растворе ионов одновалентной меди в больших количествах приводит к сдвигу реакции влево, в результате чего выпадает металлическая губчатая медь.
В растворе, кроме того, происходит окисление сернокислой одновалентной меди за счет кислорода воздуха н серной кислоты, особенно при воздушном перемешивании: Cu 2 SO 4 + 1/2O 2 + H 2 SO 4 = 2CuSO 4 + H 2 O. На катоде процесс заключается в разряде двухвалентных и одновалентных ионов меди, но в связи с тем, что концентрация ионов одновалентной меди приблизительно в 1000 раз меньше концентрации ионов двухвалентной меди, катодный процесс выглядит так: Cu 2+ + 2е - = Cu. Выход по току составляет 100%.
Для получения плотного гладкого осадка в электролите необходимо присутствие сорной кислоты. Серная кислота выполняет ряд функций: значительно повышает электропроводность электролита; понижает активность ионов меди, что способствует образованию мелкозернистых осадков; предотвращает гидролиз сернокислой закисной меди, который сопровождается образованием рыхлого осадка закиси меди.
Дефекты при эксплуатации сернокислого электролита меднения и способы их устранения
| Дефект | Причина дефекта | Способ устранения |
| Грубая крупнокристаллическая структура осадков | Недостаток кислоты | Добавить кислоту |
| Высокая плотность тока | Снизить плотность тока | |
| Шероховатые осадки | Загрязнение электролита механическими примесями | Отфильтровать электролит |
| Черные и коричневые полосы на покрытии | Присутствие в электролите примесей тяжелых металлов, мышьяка, сурьмы | Проработать электролит, при большом содержании примесей электролит заменить |
| Пористые, рыхлые осадки | Наличие в электролите солей железа | |
| Светлые блестящие полосы на покрытии, осадки хрупкие | Присутствие в электролите органических примесей | Отфильтровать электролит, проработать его током |
Борфтористоводородный электролит обладает несколько более высокой рассеивающей способностью, чем сернокислый. Кроме того, в борфтористоводородных электролитах можно применять высокие плотности тока. Состав электролита (г/л) и режим меднения:
Медь борфтористоводородная - 35-40 г/л
Кислота борная - 15-20 г/л
Кислота борфтористоводородная - 15-20 г/л
Никель хлористый - 50-70 г/л
Температура = 18-25°С
Плотность тока = до 10 А/дм 2
Электролит перемешивают сжатым воздухом или механической мешалкой.
Для приготовления борфтористоводородного электролита в борфтористоводородную кислоту небольшими порциями вводят свежеосажденную углекислую медь. Раствор углекислой меди готовят подливанием подогретого концентрированного раствора соды к раствору сернокислой меди при перемешивании. Полученный осадок декантируют, промывают и растворяют в борфтористоводородной кислоте. В приготовленный раствор добавляют свободную борфтористоводородную и борную кислоту до требуемого значения рН (1-1,5). В ванну с полученным электролитом доливают воду до рабочего уровня.
В этом интересном видео-уроке рассмотрим, как можно сделать раствор, который будет выполнять функции электролита для омеднения любых предметов из металла, например, алюминия с помощью туалетного утенка.
Для этого нам понадобится пластиковая бутылка с водой, медный провод без изоляции. Желательно, брать проволоку минимального сечения, чтобы площадь реакции была максимально большой. Если нет медной проволоки, подойдут монетки, в состав которых входит медь не желтого цвета. Вместо провода или монеток можно использовать абсолютно любую медную стружку, обрезки, отходы, в которые входит медь. Также нужно добавить небольшой кусочек олова.

В качестве предмета для омеднения в данном видеоуроке будет выступать стальная рукоятка ножа. Кроме туалетного утенка может подойти и другое чистящее средство, в состав которого входит соляная кислота, которая входит в реакцию с медью и растворяет ее.
Итак для начала сделаем следующее. Содержимое туалетного утенка необходимо влить в бутылочку с водой, чтобы получить раствор, в который будет погружена медь. Теперь в раствор кладем медный провод и кусочек олова. После этого этот раствор необходимо оставить, желательно, в теплом месте на как можно более долгий срок. Концентрация соляной кислоты, которая содержится в утерке, требует держать баночку для растворения меди в течение одного месяца. Вот и весь состав раствора.
Желательно металлическую заготовку очистить от ржавчины и грязи кипячением в растворе щёлочи или, на худой конец, обычный шкуркой.
Когда очистка и шлифовка закончена, необходимо заготовку обезжирить, так как пальцы рук человека содержат жир.
Перед использованием раствора для омеднения, его нужно хорошо встряхнуть, чтобы соли меди смешались с жидкостью. Теперь можно поместить заготовку в меднящий раствор. Желательно во время омеднения емкость с электролитом иногда покачивать, и переворачивать заготовку, чтобы создать приток свежего раствора к ней.
Прошло уже полтора часа, можно посмотреть, как прошел процесс. Хорошо видно, что заготовка покрылась медью. Ее нужно обязательно промыть водой. Медь на ней держится очень хорошо. Очень красиво получилось, но лучше не покрывать рукоять ножа медью, так как она имеет свойство окисляться и пачкать, соответственно, руку. можно сделать и не только это.
Главная › Новости
Опубликовано: 06.09.2018
Простейший способ меднения ножа в домашних условиях .В современном мире больше распространение получил медный сплав. Он наносится на поверхность для придания внешней привлекательности различных изделий. Меднение в домашних условиях зачастую проводится для существенного повышения показателя электропроводности. В некоторых случаях рассматриваемый процесс является промежуточной операцией, которая позволяет нанести другое вещество на поверхность.

Меднение в домашних условиях
Покрытие медью различных заготовок в последнее время часто проводится в домашних условиях. В большинстве случаев технология применяется для достижения следующих целей:

Меднение стали
Меднение пластика в домашних условиях проводится крайне редко, так как подобный материал не выдерживает воздействие высокой температуры. Кроме этого, пластичность основания приводит к появлению структурных трещин.
Меднение металла – особая технология нанесения слоя меди толщиной 1-300 мкм и больше. Особенности применяемых технологий определяют то, что медное покрытие будет прочно держаться на поверхности металла. Среди особенностей, которые приобретает заготовка, отметим следующие моменты:
Пластичность. Высокая электропроводность. Медные изделия хорошо известны с тем, что могут проводить электричество и при этом не нагреваются. Именно поэтому часто создаются изделия, которые покрываются подобным сплавом. Более привлекательный вид. Медь блестит на солнце, на поверхности появляются блики. В атмосферных условиях сплав легко окисляется и покрывается налетом. Этот момент стоит учитывать при рассмотрении того, где и как именно будет использоваться изделие. Медная пленка со временем покрывается пятнами и радужными разводами.
Окисление стали
Обмеднение в домашних условиях может проводиться при применении специального раствора. Стоит учитывать, что процесс предусматривает использование специальных реагентов. Поэтому нужно предусмотреть наличие эффективной приточной вентиляции, а также индивидуальных средств защиты. Меденение пластика несколько отличается, предусматривает применение особой технологии.
Рассматриваемая процедура доступна для выполнения даже новичкам в сфере металлургии. Для получения качественной поверхности нужно знать все особенности процесса. Меднение свинца и других металлов в домашних условиях может проводиться при применении двух различных технологий:
С погружением в электролит. Подобная технология предусматривает окунание заготовки в подготовленный раствор, после чего подводится напряжение. Зачастую применяется в том случае, если размеры заготовки небольшие, так как требуется меньшее количество специального электролита. Для погружения заготовки требуется ванная или другая емкость, которая не реагирует на воздействие применяемого раствора. Без погружения в заранее подготовленную емкость. Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки.В обоих случаях предусматривается подвод электричества, за счет чего вещество активизируется.
Наиболее подходящий способ обработки выбирается в зависимости от того, какой нужно достигнуть результат. Примером назовем:
Получение защитно-декоративного слоя. В этом случае часто проводится смешивание хрома с никелем и медью. За счет подобного сочетания сплавов можно получить надежную поверхность. Для защиты поверхности на момент цементирования. Нанесение тонкого слоя меди позволяет защитить заготовку от цементирования. Покрывается раствором поверхность, которая в дальнейшем будет обрабатываться резанием. Восстановление и ремонт деталей. При восстановлении хромированных деталей автомобиля и мотоциклов может применяться рассматриваемая технология. При нанесении слоя не более 250 мкм можно скрыть поверхностные дефекты металла.Обе технологии обработки характеризуются своими определенными особенностями, которые нужно учитывать.
Гальваническое покрытие медью в домашних условиях с погружением проводится крайне часто. Подобная технология позволяет получить равномерное покрытие. К особенностям подобного способа обработки можно отнести следующие моменты:
Для удаления оксидной пленки перед меденением заготовка обрабатывается наждачной бумагой. После этого изделие промывается и обезжиривается горячей смесью из соды. Если не уделить внимание подготовительному этапу, то проводимый процесс не позволит получить устойчивое к механическому воздействие изделие. Металл, который подвержен воздействию коррозии, должен быть хорошо очищен, так как даже мелкая крошка может сделать поверхность неоднородной. В банку или другую емкость на медных проволоках опускается две пластины из этого же сплава. Они выступают в качестве анода. Применяемая тара должна быть из стекла. Между двумя анодами подвешивается обрабатываемая деталь, которая подключается к минусу, а пластины к плюсу. В качестве источника питания может использоваться батарея, выдающее напряжение 6В. Гальваническое меднение предусматривает применение определенного раствора. Он является связующим элементом между деталью и анодами. Раствор для гальванического меднения можно создать изготовить, для чего берется 20 грамм медного купороса и 3 миллилитра серной кислоты. Для разбавления и смешивания этих ингредиентов можно использовать 100 миллилитров дистиллированной воды. При работе с полученным раствором нужно быть крайне внимательным, так как при попадании вещества на открытые участки кожи могут возникнуть ожоги. Меднение алюминия медным купоросом в домашних условиях может проводиться только в том случае, если электроды были полностью покрыты раствором. Если они будут находиться в сухом состоянии, то они могут нагреться и расплавиться. При длительной обработке вещество может нагреться и его объем уменьшится.
Гальваническое меднение
При применении рассматриваемой технологии сила тока устанавливается на уровне 15 мА на каждый квадратный сантиметр. На покрытие всей поверхности специальным сплавом, как правило, уходит не менее 20 минут. При увеличении протяженности срока покрытие становится толще.
Подобный метод применяется для покрытия стали, цинка или алюминия. Покрытие изделия медью в домашних условиях в этом случае проводится проводом, с которого предварительно снимается изоляция для получения своеобразной кисти. Обратный конец провода подключают к плюсу источнику энергии. Химическое меднение в домашних условиях также предусматривает использование специального раствора, который повышает эффективность процесса.
Среди особенностей создания требующего раствора можно отметить следующие моменты:
Используется раствор медного купороса. Его можно приобрести в специализированных магазинах. Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов. Состав немного подкисляют. За счет этого существенно повышается эффективность проводимой процедуры.Вещество наносится на поверхность, после чего подготавливается металлическая поверхность. Она очищается от загрязняющих веществ, после чего обезжиривается. После этого подготовленная заранее пластина укладывается в ванночку и к ней подводится минус от источника тока.

Меднение алюминия
Подобный процесс предусматривает, чтобы между собранными проводками и пластиной постоянно был слой электролита. За счет этого обеспечивается высокая степень проводимости. Для того чтобы покрыть изделие небольших размеров требуется сего несколько секунд.
После нанесения покрытия изделие сушится на воздухе. Нельзя допускать попадания различных загрязняющих веществ. Следующий шаг заключается в натирании медной прослойки шерстяной тряпкой или другим сукном. В большинстве случаев рассматриваемая технология применяется в том случае, когда изделие имеет большие размеры и не может погружаться в ванную.
Медное покрытие может наноситься в домашних условиях при применении даже самого обычного оборудования. Установка ванной для проведения рассматриваемой процедуры проводится примерно также, как и гальванических. Стоит учитывать, что существует два типа активных растворов: кислые и щелочные.
При работе может применяться:
Небольшие медные пластины в качестве электродов. Проволока для подачи тока. Источник тока, к примеру, АКБ, который рассчитан на подачу тока напряжением 6 В. Для регулировки силы тока может устанавливаться реостат.Меднение алюминия и других сплавов в домашних условиях не требует большого количества времени. Для очистки получаемой поверхности могут применяться различные ткани.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Если перед вами стоит задача омеднения каких-либо деталей в автомобиле, то оказывается это вполне возможно сделать в домашних условиях. Для этого не потребуется особых знаний и умений, да и все материалы и реагенты вполне можно найти в магазинах или своих запасах. Что же, давайте посмотрим как можно сделать омеднение.
Прежде чем рассказать о самом процессе, хотелось бы сказать пару слов о прагматичности такой операции. Многие из автолюбителей не особо знакомых с химией сейчас скажут о необходимости омеднения всего чего попадется под руку, но мы вас предостерегаем от этого! Почему!? Да потому что все металлы между собой образуют гальваническую пару. Такая гальваническая пара образуется даже при попадании воды, а если средой будет еще и кислота, то процесс пойдет в разы быстрее. Суть процесса в гальванической паре сводится к следующему. Более активный металл отдает свои электроны, а менее активный принимает. Вот так и образуется самая простая «батарейка» в которой протекает электрический ток. Давайте теперь взглянем на стандартные электродные потенциалы:
- для меди Е0(Сu2+/Cu)=0,34В;
- для железа E0(Fe2+/Fe)=-0,44В.
В итоге получается не все так гладко. Ведь в такой гальванической паре У железа электродный потенциал более активным. Опять же у меди электродный потенциал более положителен, чем у железа, поэтому она будет менее активна. В итоге электроны потекут от железа к меди, что приведет к коррозии железа.
Все это мы рассказали к тому, что бездумно покрывать медью все что вам попадется под руку на машине не рекомендуется. Ведь в этом случае вы можете значительно сократить жизненный цикл многих железных деталей (крепеж, кузовные детали).
Не зря для сохранения железа применяют цинк, там ситуация с электродными потенциалами обратная.
Однако омеднение может применяться для декоративной отделки железа, если покрытие будет находиться в сухости. Также медь может применяться в случаях, где необходимо обеспечить передачу электрического тока между контактами. Опять же надо следить за их чистотой.
Медь может применяться в условиях применения пар с незначительным трением скольжения. Все это в целом вполне жизнеспособные варианты. А значит и омеднение все же имеет шанс на его реализацию. Тогда не будем более медлить, расскажем непосредственно о процессе омеднения.
Омеднение происходит в растворе. По сути этот процесс обратный гальванической паре, то есть тому, о чем мы рассказывали в абзаце выше.
Для раствора нам понадобиться кислота, можно взять электролит используемых для аккумуляторов. Воду и медный купорос.
Для раствора берется 100 мл электролита на 20 мл воды и добавляется 20 г медного купороса. В качестве донора меди можно взять медные пластинки или обычный медный провод, предварительно очищенный от изоляции. Итак, именно в этот самый раствор и помещаем медь. При этом подключаем блок питания постоянного напряжения питания к меди (+) и к железу (-). Ток на блоке питания выставляем тот, при котором мы планируем за определенный период времени нанести определенный слой меди. Это уже задача по химии школьной программы. И получается все так…
I= (плотность меди (8920 кг/м3)*площадь детали (скажем 0,1 м3)*(требуемый слой (скажем 0,0001 м, то есть 0,1 мм))/ (электрохимический эквивалент для меди это 6,6*〖10〗^(-7)
* желаемое время, скажем 3 часа – 10800 секунд). Считаем…
I=8920*0,1*0,0001/0,0000066*10800=0,0892/0,07128=1,25 А
То есть за 3 часа при токе 1,25 А у нас будет покрытие в 0,1 мм на детали площадью 0,1 м3. Вот как-то так и считаем все аналогичные вариации.
А да, время от времени не забываем помешивать раствор, чтобы процесс шел равномерно.
После того как омеднение завершено, вытаскиваем детали из раствора и отмываем хорошо с щелочью, то есть с мылом.
Если есть каике-то заусенцы и отклонения от формы, то их вполне можно пройтись наждачной бумагой и заполировать.
Собственно вы теперь не меньше знаете, как производить омеднение поверхности. Надо сказать, что по тому же принципу производится и оцинкование и хромирование… В итоге понимая принцип происходящего процесса можно перенести процесс покрытия поверхности и на другие металлы.
Может ли стальной гвоздь быть медным?
Металлические предметы могут быть покрыты тонким слоем другого металла, этот процесс называется гальванопокрытием. В гальванике используются электрохимические явления, сопровождающие протекание тока между электродами, помещенными в гальваническую ванну.
Примером гальванического покрытия является химическое меднение, процесс покрытия металла медью без использования внешнего источника питания.
Это текущее меднение без электричества. При этом используется явление вытеснения «более благородных» металлов «менее благородными».
В случае меднения изделий из железа или стали, погруженных в раствор соли меди, например сульфата меди, медное покрытие осаждается на поверхности железа или стали. В результате химического меднения образуются очень тонкие покрытия.Химическое меднение подходит только для нанесения декоративных покрытий, поэтому в технологических процессах его практически не применяют.
Это меднение можно сделать в домашних условиях. Попробуйте этот эксперимент.
Вам понадобится:
В банку налить полстакана воды и добавить 1 пакетик лимонной кислоты (20 г), сделать раствор, т.е. тщательно перемешать.Поместите медные элементы в готовый раствор и оставьте примерно на 1 час.

За это время подготовьте ноготь: тщательно зачистите его наждачной бумагой, тщательно вымойте с мылом и промойте от грязи (этот процесс называется обезжириванием).
Удалить медные предметы из раствора лимонной кислоты.
Обратите внимание, что медные предметы теперь идеально чистые и блестящие! Теперь опустите подготовленный ноготь в тот же раствор.

Оставляем ноготь в растворе на несколько часов, и в это время наблюдаем за тем, что происходит с нашим ногтем.

Через полчаса видно, что ноготь меняет цвет.
В ходе эксперимента частицы меди переходили в раствор лимонной кислоты и приобретали электрический заряд, после чего оседали на поверхности железа и прочно связывались с ним.В результате получается тонкий слой коричневого налета, состоящий из чистой меди, хотя он немного похож на ржавчину.

Способность утончать один металл над другим тоже была полезна в старые времена, особенно преступникам и фальшивомонетчикам.
Такое тонкое покрытие может быть изготовлено из различных металлов, например хрома, цинка, золота, серебра.
В настоящее время украшения, скульптуры и кубки позолочены, а хромированный кран не только не ржавеет, но и блестит как зеркало.
Экспериментируйте с удовольствием!
Драгоценность Виолетты
.Меднение — это процесс гальванического покрытия медью различных поверхностей. Медный слой имеет прочную адгезию к металлам, сглаживает каверны на покрытой поверхности, обладает высокой электропроводностью и пригоден для дальнейшей обработки. Меднение может применяться как самостоятельный процесс или в составе более сложных процессов (серебрение, никелирование, хромирование). Наряду с промышленным методом практикуется меднение в домашних условиях, что позволяет решить многие бытовые задачи.Помимо высоких технических параметров, это покрытие прекрасно выглядит, что определяет его использование в различных дизайнерских решениях.
В промышленных условиях меднение происходит в мощных гальванических ваннах, оборудованных автоматикой и другими специальными устройствами. Однако этот процесс также доступен внутри компании, что устраняет необходимость в сложном химическом оборудовании.
Последовательность технологических операций следующая:
1.Оксидная фольга удаляется с поверхности металла. Используемая наждачная бумага, щетка, полировальная паста;
2. Обезжирить окрашенный предмет содовым раствором и тщательно промыть водой;
3. Две медные пластины (аноды) погружены в стеклянную емкость на медной проволоке, часть подвешена между ними;

4. Аноды подключаются к «плюсу» источника постоянного тока, а медная часть к «минусу»;
5. Токорегулирующий реостат и амперметр включены последовательно в электрическую цепь.В качестве источника постоянного тока можно использовать автомобильный аккумулятор или адаптер питания;
6. Электролит заливают в емкость так, чтобы полностью покрыть поверхность анодов. Эту операцию необходимо выполнять с особой осторожностью, не допуская попадания агрессивных жидкостей на открытые участки кузова!
7. Плотность тока устанавливалась 2А на дм2 обрабатываемой поверхности, температура электролита 20-26 градусов, время обработки 20-25 минут;

8. Медная деталь вынимается из контейнера, и процесс завершается.Толщина медного слоя может быть увеличена за счет увеличения времени пребывания деталей в гальванической ванне.

Состав электролита не сложный: серная кислота - 40 г, медный купорос - 190 г, вода - 980 г.
Несколько советов по меднению:
медный купорос 
Иногда требуется заменить сломанную медную мебельную фурнитуру, а в продаже есть только никелированные изделия.В этом случае медную крышку можно легко собрать. Необходимое оборудование и материалы: блок питания 12 В/3 А, серная кислота и медный купорос.
Сначала снимите никелированное покрытие. Для этого деталь удерживается пинцетом, который подается «вниз» от источника питания. С прикрепленной тканью
Положительный электрод, смоченный 5% серной кислотой, протирает поверхность изделия.
При удалении никелирования образуются ядовитые пары, от которых следует защищать органы дыхания.Желательно использовать специальные очки и респиратор с угольным фильтром. Очищенная поверхность полируется.
Следующим шагом будет установка простейшей гальванической установки. В банку помещают медный электрод, подключаемый к «плюсу» источника питания, а заготовку – к «минусу».
Заливают электролит, состоящий из медного купороса, воды и 5% серной кислоты в соотношении 1/5/3 и подают электричество. Готовые изделия полируются до приятного блеска.

Существует множество различных применений внутреннего меднения. Медь можно наносить на алюминиевые столовые приборы, давая им вторую жизнь, рыболовные приманки, подсвечники и многое другое. Особенно впечатляют работы, в которых декоративное покрытие наносится на неметаллические предметы: стебли растений, листья, желуди и даже засушенных насекомых. Натуральная фактура исходного материала в сочетании с красотой гальванического покрытия создают неповторимый художественный эффект.
Технология изготовления таких изделий немного сложнее, но в домашних условиях вполне выполнима. В покрытом материале нет токопроводящего слоя, поэтому вместо него на поверхность наносится специальный токопроводящий лак. В состав лака входят органические растворители, пленкообразующие вещества и мелкодисперсный графитовый порошок, обеспечивающий электропроводность.
Лак наносится тонким слоем на сухое растение, высыхает, и через час все готово к меднению.После гальванического покрытия внешний вид изделия может быть дополнительно улучшен. Существует несколько способов придания гальваническим покрытиям меди различных оттенков, включая патинирование, химическое окрашивание и окисление.
Качество графики, полученной с применением этих технологий, на уровне настоящих ювелирных украшений.
Уважаемые читатели, комментируйте статью, задавайте вопросы, подписывайтесь на новые публикации - нам интересно ваше мнение :)
Гальванопокрытие — это электрохимический процесс, при котором форма объекта воссоздается путем осаждения на него металла.Гальваника – это покрытие неметаллических поверхностей металлом.

Гальванику часто наносят на различные изысканные изделия (ювелирные изделия, ордена и медали, монеты, раковины, цветочные горшки, скульптуры, портреты и т.д.). Медь чаще всего используется в гальванике. Однако можно использовать и другие металлы, включая никель, хром, сталь и серебро.
При соблюдении любых технологических требований копируемый объект можно отличить от оригинала только по барьерному слою или удалению оригинала.Тем более, что все работы вполне можно выполнить своими руками в домашних условиях.
Внимание! Покрытие копируемого изделия должно быть электропроводным. Если материал не обладает этим свойством, то на него наносится бронза или графит.
Снимаем отпечаток с копируемого изделия. Для этого понадобится какой-нибудь легкоплавкий металл, пластилин, гипс или воск. Если используется металл, скопированный предмет обрабатывают мылом и укладывают в картонную коробку.Затем заливаем туда легкоплавкий сплав.

После литья снять изделие, обезжирить полученную форму и затем омеднить в электролите. Чтобы избежать отложения металла на нетисненых сторонах, расплавьте металл в кипящей воде, чтобы сформировать матрицу. Заполните форму гипсом. На выходе получаем копию.
Для изготовления матрицы нужен следующий состав:
Если форма изготовлена из диэлектрического материала, на ее поверхность наносится электропроводящее покрытие. Токопроводящий слой наносится обжатием металла или механическим способом, т.е. нанесением чешуйчатого графита кистью.
Перед обработкой поверхности графит растереть в ступке и просеять. Лучшее сцепление графита наблюдается с пластилином. Гипсовые, деревянные, стеклянные и пластмассовые формы, а также папье-маше наиболее эффективно обрабатываются раствором бензина и воска.Когда поверхность еще не высохла, нанесите на нее графитовую пыль и сдуйте налипшее вещество направленным потоком воздуха.
Оцинкованное покрытие легко отделяется от матрицы. Если форма металлическая, мы создаем электропроводящий слой на поверхности оксидов или сульфидов. Например, на серебре это будет хлорид, на свинце - сульфид. Фольга поможет легко отделить форму от покрытия. В случае меди, серебра и свинца покройте поверхность 1% раствором сульфида натрия, чтобы образовались нерастворимые сульфиды.
Когда форма будет готова, поместите ее в гальваническую ванну, подключенную к электрическому току (во избежание растворения разделительной фольги). Во-первых, мы покрываем проводящий слой меди в условиях низкой плотности тока.
Нам нужен следующий состав:
Рабочая температура в электролитной ванне 18-25 градусов Цельсия. Плотность тока составляет от 1 до 2 ампер на квадратный дециметр. Для улучшения смачиваемости покрытия потребуется спирт. Автомобильное зарядное устройство можно использовать в качестве источника постоянного тока. Нам также нужен амперметр, способный измерять от 0 до 3 или 5 ампер. Обычно амперметр уже доступен за отдельную плату.

Нихромовая проволока будет служить реостатом.Наматываем на любую керамическую плитку. Достаточно спирали от электронагревателя.
В качестве ванны подойдет любая пластиковая емкость объемом от 2 до 50 литров, в зависимости от ваших потребностей. В качестве анода используем медную пластину.
Внимание! Площадь анода должна быть примерно равна площади заготовок.
Для создания токопроводящего слоя изделия добавьте в коричневый порошок несколько капель лака. Рекомендуется использовать бесцветный нитролак.Лак необходимо разбавлять, поэтому разбавляем его ацетоном до консистенции жидкого состава лакокрасочных материалов.
Берем 20 см кусок многожильного кабеля и снимаем с него провод. Закрепляем изоляцию с обеих сторон провода, загибаем один конец под углом 90 градусов и приклеиваем к пластиковой части моментальным клеем. Более того, клей БФ не подойдет, так как расплавится.
Когда вещи высохнут, обезжирьте их бытовой химией (напр.стиральный порошок). Затем промываем изделие под проточной водой или обрабатываем ацетоном.
Детали прочно прикреплены к проволоке. Теперь их можно обмакивать по отдельности в заранее приготовленную коричневую краску или наносить кистью. Вся поверхность должна быть окрашена равномерно. От кабеля рекомендуется использовать изолированный провод, иначе медь попадет на оголенный провод, что вызовет дополнительный износ анода.
После высыхания поверхности в течение часа скрутите вместе высушенные концы проводов.Детали не должны касаться друг друга. Затем соединяем продукты для положительного контакта и погружаем их в ванну. Через несколько секунд после погружения начнется процесс меднения, видимый невооруженным глазом.

Толщина медного покрытия может варьироваться в зависимости от обстоятельств, но для мелких предметов она будет составлять примерно 0,05 миллиметра. Детали остаются в ванне на 15 часов. Ток регулируется перемещением контакта по нихромовому реостату в пределах 0,8-1,0 ампер. После меднения увеличиваем ток до 2 ампер.По истечении срока старения деталей промойте их под проточной водой, высушите и отрежьте проволоку. Зачищаем проволоку и подготавливаем к следующей процедуре.
Следующий шаг — полировка. Для этого пригодится моторчик с круглой металлической щеткой. Эта работа требует определенных навыков. В результате у нас должна получиться поверхность, напоминающая почерневшую бронзу с несколькими блестящими участками. Если сразу не удалось добиться желаемого результата, повторно нанесите серную мазь, нагрейте изделие на огне и отполируйте.
Если у вас есть сомнения в эффективности описанной выше процедуры, предлагаем провести тест. Для этого вам понадобится емкость с электролитом, в которую нужно капнуть немного меди. Одну часть красим краскопультом в 2-3 слоя в коричневый цвет. Затем нужно подключить аккумулятор без использования реостата. Адаптер плеера тоже работает.
Помимо меди, на неметаллическую поверхность можно наносить другие металлы, в том числе золото или серебро.Гальванизация серебром может производиться двумя способами: химическим или электрохимическим. Химическое серебрение производится путем погружения предмета в кипящий раствор с серебром. Электрохимический процесс дает более достоверные результаты, поскольку покрытие более прочно при воздействии электрического тока. Серебряное гальванопокрытие широко используется в ювелирном деле.
Так что гальванопластика в домашних условиях вполне возможна. Процесс достаточно трудоемкий и требует некоторой сноровки, но конечный результат того стоит.
Проблема номер один - из чего делать аноды? Люди делятся своим опытом на форумах. Они сделаны из всего (гвоздь, ложка, ядро батареи и т. д.). Кто-то хвалит медные пластины, кто-то хвалит нержавеющую сталь, а кому-то просто нужна фольга от пивной банки. Лично я буду делать графитовые аноды. Предвосхищаю вопрос "откуда мы это берем? Говорят, мы не работаем на графитовом заводе…». Одни предлагают вскрыть аккумулятор и вытащить из него стержни. Во-первых, не все аккумуляторы сейчас имеют графитовые стержни, во-вторых, если они и есть, то они маленькие, и в-третьих, аккумуляторы стоят денег.Кто-то предложил использовать графитовые щетки от электродвигателей. Опять же, выхода нет, так как они стоят денег, и вам придется искать его. Нашел следующее решение - графитовые вставки "из-под углов" троллейбуса.
Выглядят так:
С одной стороны они плоские, а с другой стороны имеется углубление для кабеля. Лично меня эта выемка не волнует, если она вас раздражает, вы можете отшлифовать ее. Я взял 4 вкладыша, как видите. Я вышел со словом "спасибо". Думаю, любой водитель троллейбуса отдаст его вам за плитку шоколада.В крайнем случае они периодически переворачиваются на конечных остановках троллейбуса. Попутно рассказали историю, что эти патроны старые и новые. Почему-то "троллейбусы" любят старые. Не знаю... может они "более графитные"... для меня так и осталось загадкой. И это не главное.
Потом нашел в гараже у знакомого 2 электрода (они используются для сварки).
Это выглядит так:
В принципе, вы можете использовать что угодно. Тут ко мне обратились.Я их скинул и зачистил наждаком. Затем ножовкой вырезал 3 одинаковых куска.
Я использовал баклажан на 5 литров под бак с электролитом. Я отрезала верхушку и сделала надрезы по краям ножницами, чтобы булавки не катились.
Получилось так:

Один вырез я сделал по центру, остальные равноудалены по бокам. Это может выглядеть не очень эстетично, зато практично и совершенно бесплатно.
Так как блоки все же довольно узкие (примерно 2,5 - 3 сантиметра... мерить точно лень), решаю их склеить. Задача на самом деле простая. Только надо помнить, что через место нашей склейки протекает ток. Берем и затачиваем край ботинка ножом до пыли.
Получаем это:

Далее берем 2 композитных эпоксидных клея. Есть пять минут. У меня не было под рукой, так что пришлось натягивать клей с удовольствием :( Заливаем смолу в пробку, добавляем в нее графитовую пыль, все перемешиваем.Затем влить отвердитель (поставляется с клеем) и снова все перемешать.
Вот такая картинка:
Получается, что 2 анода:


Края большие, один красный, другой черный. Это не потому, что я стреляю плюсом по одному, а минусом по другому, а потому, что у меня их было всего 2 на руках (на оба плюс пойдет). Внутри маленький крокодильчик, к которому я прикреплю монетку. Делать этих крокодилов или нет, решать вам.Кто-то использовал женские шпильки и зацепил монету за край. Я накрутил то, что было под рукой. Тем более, что все на ваше усмотрение. Делай, что хочешь, пока нет электричества.
В клеевых матрицах делаю продольный паз сверху и таким же образом (эпоксидка плюс графитовая пыль втыкаю штыри на электроды).

Ждем пока высохнет (благо работа не пыльная).
После того, как все высохнет, предлагаю проверить, как ток течет по нашей конструкции.Для этого беру мультиметр, ставлю на омы и щупы ставлю с противоположной стороны склейки. Я вижу, что ток течет.

Собственно все готово.
Осталось подключить нашу конструкцию к источнику постоянного тока. Кабеля прикручиваю большими крокодилами к плюсу и маленькими крокодилами к минусу. Где взять текущий источник? Я использовал игрушечный железнодорожный блок. Вы можете найти блоки питания от других устройств. Обратите внимание на силу тока.Полуамперные устройства точно будут работать, но как? Лучше все же поискать что-то на 1,5-2 ампера.
Мы собираем наш продукт. Я наливаю воду в ванну и добавляю пищевую соду, которую купила в первом же попавшемся продуктовом магазине.

Где-то говорят, что надо использовать 5% раствор едкого натра (едкого натра). Ну, каустической соды у меня дома нет, поэтому пользуемся тем, что есть. На литр воды несколько столовых ложек обычной соды и она в пакетике ;) Все смешать.К стержням на графитовых анодах прикрепляем большие крокодилы, а на маленьком крокодиле подвешиваем изделие.
Кстати, вот тема:

Отличный тестовый объект. Монета полностью убита. Его выгнали на берег. Картинку вообще не видно. Видны впадины глубокой коррозии, к тому же мы сверху забиты песком и прочим твердым мусором. Кашемир, а не монета ;)
Подключаем нашу установку к розетке и подаем около 5 вольт напряжения.

Картинка - любуешься, все булькает, все работает... одним словом красота.
Ну а теперь о результате. Конечно, перед электролизной очисткой монету нужно было промыть, постараться удалить налипшие твердые частицы и т. д. Не погружайте монету в ванну надолго. Иногда снимать и чистить. Комбинируйте механические, химические и электрохимические методы очистки. Я не делал этого намеренно. Задача состояла в том, чтобы показать, что электролиз сделает с монетой.
Это было на самом деле:


Я особо не терся. Не имеет смысла. Как видите, дырки и прочие недостатки раскрылись, но сама монета почистилась. Если не злоупотреблять этим методом, не торопитесь, а если сам предмет чистки хорошо сохранился, поможет электроэпиляция.
Надеюсь, моя статья окажется вам полезной. Вы можете обсудить это и задать вопросы об уборке таким образом, сделать рационализацию и т.д.На форуме в теме "Гальваническая ванна своими руками".
Гальваника — это бытовой процесс покрытия одного металла частями другого металла.
Гальваническое покрытие представляет собой прохождение электрического тока через раствор, называемый электролитом. Это делается путем погружения двух наконечников, называемых электродами, в электролит и их подключения к цепи с батареей или другим источником питания. Электроды и электролит являются выбранными элементами. При протекании тока по цепи электролит начинает расслаиваться, и часть атомов металла из его состава осаждается тонким слоем на поверхности одного из электродов.Таким способом можно обрабатывать все типы металлов, включая золото, серебро, олово, цинк, медь, кадмий, хром, никель, платину и свинец.
Итальянский изобретатель Луиджи В. Бруньятелли изобрел искусство гальваники в 1805 году. Подключил провод между вольтом (батарейкой) и золотым раствором.
Провод, подключенный к металлическому предмету, заземляет цепь, и по мере прохождения тока золото прилипает к поверхности металлического предмета, создавая гладкую блестящую поверхность.

Гальваника стала важным коммерческим процессом в 1840-х годах, когда Джон Райт (Англия) обнаружил, что золото или серебро можно растворять в цианиде калия для использования в гальванотехнике. Одной из первых компаний, внедривших новый процесс, была британская компания Elkington & Mason, которая запустила производство серебра и производила оправы для очков, ручки и другие мелкие металлические детали, которые можно было использовать большими партиями.
В течение многих лет гальваническое покрытие использовалось в основном для производства дорогих изделий из недорогих материалов.
В XIX веке национальные церкви использовали, в частности, тысячи религиозных икон, покрытых золотом или серебром. Однако в последующие годы компании использовали гальваническое покрытие для создания объектов, которые было нелегко воспроизвести даже с использованием дорогих материалов. Классический пример – автомобильный бампер.
Особенности процесса
Гальваника, в том числе в домашних условиях, очень похожа на электролиз (при котором используется электричество для разделения химического раствора), который представляет собой обратную процедуру, при которой батареи вырабатывают электричество.
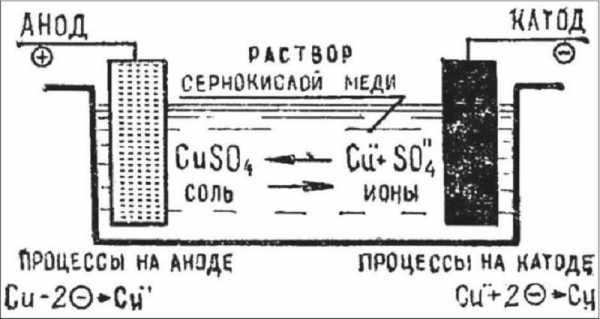
Крайне важно использовать правильные электроды и раствор электролита для гальваники в домашних условиях, предопределяя химическую реакцию или реакции, которые произойдут, когда электрический ток начнет действовать. Атомы, которые прилипают к продукту, поступают из электролита. Поэтому, если есть процесс гальванического покрытия медью, вам нужен медный электролит, а для золотого покрытия вам нужен электролит на основе золота.
Во время нанесения гальванического покрытия техник должен убедиться, что используемый продукт полностью чист.В противном случае, когда атомы из электролита достигнут его, они не образуют хорошей связи, и элементы могут просто выпасть в осадок. Обычно очистку производят погружением электрода в сильнокислый или щелочной раствор или (на короткое время) подключением гальванической цепи в обратном направлении. Если электрод действительно чистый, атомы металлизации объединяются, образуя очень прочную кристаллическую структуру.

Внутренняя гальванизация – это пропускание электрического тока через электролит.Это делается путем погружения двух наконечников, называемых электродами, в электролит и их подключения к цепи с батареей или другим источником питания. Электроды и электролит изготовлены из тщательно отобранных элементов или соединений. При прохождении тока по цепи электролит разрушается, и часть атомов содержащегося в нем материала осаждается тонким слоем на одном из электродов. Таким образом, выполняется внутреннее гальваническое покрытие, все виды металлов могут быть покрыты, включая золото, серебро, олово, цинк, медь, кадмий, хром, никель, платину и свинец.
Для получения ровного гальванического покрытия мастер должен предварительно очистить поверхность металлического предмета и подготовить необходимое оборудование. Грязь и масла на поверхности могут помешать донору покрыть поверхность. Начните с обезжиривания моющим средством (средством для мытья посуды), а затем протрите металл абразивным кислотным очистителем, чтобы поверхность оставалась очень чистой.
Материалы для технологии
Необходимое оборудование при гальванике в домашних условиях
- Металлический предмет с покрытием (должен быть из стали).
- Питание (3В-6В).
- Сульфат цинка/гидроксид цинка/хлорид цинка.
- Вода.
- Стекло (вместо стеклянного или пластикового предмета).
- Цинк (можно найти в батареях Zn-C).
- Наждачная бумага (120).
- Ванна для гальваники своими руками или аналогичная емкость.
- Папиросная бумага.
- Провода.
- Достаточно чистая рабочая зона для гальваники.
- Требуется переменный источник постоянного напряжения, бытовая розетка не подходит.

Что нужно для приготовления электролита в домашних условиях? Разные продукты требуют разных рецептов растворов. Для раствора используют воду с кислотами и другими важными включениями солей и металлов. Гальваника своими руками позволит обработать многие детали и инструменты для украшения или повышения износостойкости. Температура электролита играет различную роль в разных операциях. Например, при хромировании чем выше температура, тем чище покрытие.
Начало работы
Как подготовить изделие из стали или другого материала перед началом процесса в домашних условиях?

Многие защитные покрытия содержат специальные правила подготовки поверхности для гальванического покрытия при самодельном покрытии.
Материалы, которые нельзя удалить с помощью чистящих химикатов
Существуют материалы, которые нельзя удалить с помощью химикатов или которые трудно удалить с помощью гальванического покрытия. Вот список наиболее распространенных из этих материалов:
- сварочный шлак и другие остатки сварочного флюса;
- разбрызгивание и разбрызгивание;
- Заусенцы (могут включать чрезмерно шероховатые края от газопламенной резки)
- фрезерные покрытия, такие как лак или лак на некоторых типах труб;
- эпоксидная смола, винил и асфальт;
- песок и прочие примеси для отливок;
- масляные краски и маркеры;
- карандашные маркеры;
- очень тяжелые или толстые отложения парафина или жира.
Эти материалы должны быть удалены с поверхности перед доставкой на завод по цинкованию или в бытовых условиях.

Существуют различные общепринятые стандарты для абразивоструйной очистки, ручной очистки и очистки с помощью механического инструмента, которые эффективны при удалении этих материалов. Для отливок обычно требуется абразивоструйная очистка для удаления песка и других загрязняющих веществ в процессе литья. Кроме того, вы можете использовать различные продукты, совместимые с процессом гальванического покрытия, чтобы уменьшить потребность в дробеструйной очистке или очистке электроинструментов.Использование непокрытых электродов позволяет избежать проблемы отложения флюса при сварке, что вредно для эксплуатации. Доступны маркеры, которые легко растворяются в ваннах, используемых в процессе цинкования.
Внутридомовая гальваника кладочной кислотой
Для установки внутридомовой системы гальванизации вам понадобится вода, соляная кислота, батарейка для фонарика на 6 вольт, пара зажимов для проводов, кусок меди, кусок металла для обработки и емкость для хранения компонентов, которые используются при гальванике в жидкой среде.Аккумулятор 6В имеет два контакта для легкого подключения к системе. Можно использовать более слабый блок питания.
- Крокодилы фиксируют кусок меди (как источник ионов для элементов покрытия) и основную заготовку. Сталь и никель — это два компонента, которые легко покрываются медью.
- После очистки поверхности материала различными моющими средствами необходимо создать гальванический раствор.
- 5 частей воды смешивают с 1 частью соляной кислоты. Не добавляйте воду непосредственно в кислоту! Подобные действия вызывают бурные реакции с возможными вспышками.
- Всегда соблюдайте соотношение 5: 1. Например, если вам нужно больше 5 чашек, отмерьте 10 чашек воды и добавьте 2 чашки кислоты. Используйте пластиковые инструменты для смешивания, так как кислота разрушит металл. Верхняя часть контейнера начнет нагреваться, когда кислота вступит в реакцию с водой.
- Подсоедините зажим типа «крокодил» к клеммам источника питания. Аккумулятор будет нести ток, необходимый для процесса гальваники. Прикрепите один зажим к одному зажиму типа «крокодил», а другой — к другому зажиму аккумулятора.
- Подсоедините медь к положительному выводу аккумуляторной батареи. Используя крокодил, прикрепленный к положительному зажиму источника, закрепите другой конец куском металлической меди. В других случаях гальваника не работает.
- Подключите к цепи ту часть, которая будет подключена к отрицательной клемме аккумулятора. Прикрепите зажим, где это возможно, в области, где гальваническое покрытие не требуется. Если нет свободного места для крепления клипсы, придется в процессе переставить крокодил, чтобы на изделии не осталось следов использования клипсы, а покрытие было равномерным по всей площади.
- Если процесс не запущен, убедитесь, что установлены правильные терминалы.
- Погрузите обе части в подготовленную ванну с разбавленной соляной кислотой. Кусок меди не обязательно должен быть полностью погружен в раствор, но обрабатываемое изделие полностью погружается в рабочую среду.
- Для получения ровного слоя рекомендуется периодически перемешивать раствор в емкости.
- Держите две детали отдельно друг от друга, чтобы избежать слишком быстрого накопления меди.
- При использовании этого метода трудно получить толстый слой меди, но можно добиться тонкого напыления. Когда вас устраивает внешний вид материала, вещь достают и сушат.
Нанесение покрытия может занять от нескольких минут до нескольких часов. После создания нужного слоя материал необходимо просушить.
Гальванизация раствором электролита с ионами металлов в домашних условиях
Для гальваники в домашних условиях данным методом вам потребуется кусок меди, металл для гальваники, уксус, перекись водорода, скрепки, батарейка для фонарика на 6 вольт и пластиковый контейнер .
Используйте достаточно большой контейнер, чтобы залить материал, который вы пытаетесь залить.
- Смешайте и нагрейте равные части уксуса и перекиси водорода. Чтобы приготовить четыре стакана раствора, добавьте два стакана уксуса к двум стаканам перекиси водорода. Сочетание уксуса и перекиси водорода образует надуксусную кислоту, с которой нужно обращаться осторожно.
- Растворить медный стержень в составе. Жидкость становится синей, что указывает на то, что раствор содержит ионы меди, которые можно использовать для гальванического покрытия материала.
- Замочите медь, пока раствор не станет синим. Лучше, чтобы раствор был слабой концентрации, раствор не должен быть слишком темным.
- Прикрепите зажимы к аккумулятору. Аккумулятор поставляет электричество, необходимое для транспортировки металлов от донора к реципиенту. Подсоедините один зажим к положительной клемме аккумулятора, а другой зажим к отрицательной клемме.
- Чистый металл в быту для гальваники. Прежде чем приступить к гальваническому методу, убедитесь, что металл чистый, чтобы новые атомы могли образовать постоянную связь с металлом-получателем.
- Подсоедините положительный зажим к медному элементу.
- Прикрепите негативный крокодил к металлической крышке. Попробуйте приколоть аллигатора в незаметном месте. Если вы прикрепите металл к положительному полюсу, гальваника не сработает.
- Погрузите элементы в медную жидкость. После того, как два металла будут объединены, окуните их в предварительно приготовленный раствор синей меди. Поскольку они подключены к батарее, ток течет по цепи. Лечение продолжается до тех пор, пока не будет достигнут удовлетворительный уровень покрытия.
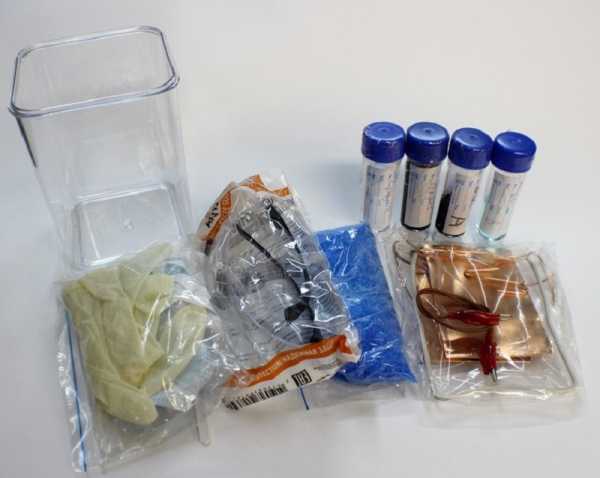
Особенности гальваники различными металлами в быту
Возможность нанесения тонкого слоя на металлический предмет в быту может выполнять декоративную функцию или придавать деталям коррозионную стойкость и восстанавливать работоспособность.
Никелирование — это процесс нанесения никеля на металлическую деталь. Широко используется декоративный блестящий никель. Обеспечивает высокий блеск, защиту от коррозии и износостойкость. В автомобильной промышленности блестящий никель можно найти на бамперах, дисках, выхлопных трубах и отделке салона.Он также используется для экстравагантных работ на велосипедах и мотоциклах.

Слой хрома в доме может быть декоративным, обеспечивать коррозионную стойкость, облегчать очистку или повышать твердость поверхности. Иногда в эстетических целях можно использовать более дешевую имитацию хрома. Домашнюю гальванику можно сделать и в домашних условиях.

Меднение применяется для создания защитного слоя или увеличения электропроводности материала.Для создания такого слоя используются ядовитые, опасные для жизни цианиды. В домашних условиях такую операцию не проводят. Изначально стальные изделия никелируют, а уже потом меднеют.

Гальваника считается самым простым способом гальванизации изделий. Электролит состоит из сульфата цинка (200 г), сульфата аммония (50 г), ацетата натрия (15 г) на литр воды. В этом растворе цинк растворится и потом успешно покроет заготовку.

Латунное покрытие используется в декоративных целях для арматуры. Для работы электролит должен содержать соли меди и цинка, смешанные с раствором цианида. Гальваническое покрытие латуни также не рекомендуется.
Серебро и позолота применяются в промышленности в качестве токопроводящего и декоративного слоя. Изделие предварительно покрывается никелем, а затем покрывается серебром или золотом. Для работы электролит должен содержать хлорид серебра, железо, цианистый калий и кальцинированную соду.Такую жидкость следует нагреть до 20 градусов, при этом в качестве анода можно использовать графитовый материал.

Внутреннее гальванопокрытие может быть использовано для создания точных копий металлических деталей, плат или схем. Кроме того, использование технологии позволит улучшить рабочие свойства заготовки. Используйте для этих целей золото, серебро, никель, хром или аналогичные металлы.
Меры предосторожности при обращении с опасными химическими веществами
Носите соответствующие средства защиты при работе дома.При гальванике металлов люди имеют дело с кислотами и другими химическими веществами, от которых необходимо защищаться. Требуются защитные очки, перчатки и лабораторный халат. Приветствуется одежда, не наносящая вреда гальванопокрытию металла.
Метод цинкования является одним из самых распространенных в создании надежной защиты металла от коррозии. Это просто и дешево. Поэтому данный способ обработки можно проводить в домашних условиях, для чего необходимо соблюдение определенных условий.
При создании качественных и долговечных металлических покрытий чаще всего используется технология цинкования. Это связано с низкой стоимостью расходных материалов и отличным результатом. Сама оцинковка производится по самой простой технологии. Его выполнение не требует дополнительных затрат и больших усилий, что позволяет проводить такую обработку в домашних условиях.

Цинковое покрытие получается благодаря тому, что цинк вступает в реакцию окисления с кислородом воздуха.Затем на поверхности обрабатываемого металла образуется прочная защитная пленка, предохраняющая его от негативного воздействия внешней среды.
Цинк является более активным металлом, чем железо или сталь. Поэтому он взаимодействует в первую очередь с кислородом и водой, предотвращая коррозию. Даже если хотя бы часть покрытия находится на поверхности металлических изделий, оно защищает ее от повреждений.
Технологический процесс цинкования означает осаждение катионов металлов на аноде.Аналогичная химическая реакция протекает в ванне электролита под действием электрического тока.
В качестве электролита можно использовать любой раствор соли цинка. Наиболее популярными и легкодоступными являются хлорид цинка и соляная кислота. Также электролит с требуемыми свойствами можно получить травлением цинка в серной кислоте. Эту реакцию нужно проводить очень осторожно. Это сопровождается выделением большого количества тепловой энергии и взрывоопасного водорода.

Травление цинка в серной кислоте с выделением водорода для получения соли цинка
Для домашнего цинкования необходимо подготовить цинк, который можно получить следующим образом:
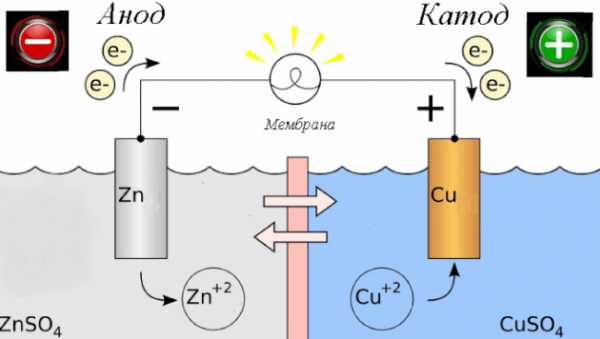
Для создания качественного металлического покрытия необходимо провести несколько подготовительных операций:

Бытовая машина для цинкования
Для создания качественного защитного покрытия на поверхности металла после подготовительных операций источник тока подключают к сети и катод погружают в гальваническую ванну. Этот процесс должен протекать без энергичной варки. Если это наблюдается, можно заподозрить, что в системе слишком большой ток. Для его уменьшения к электрической цепи подключают несколько дополнительных потребителей.
На поверхности катода постепенно образуется металлическое покрытие. Чем дольше длится этот процесс, тем больше будет толщина защитного слоя на металле.
Существует множество эффективных химических методов цинкования, каждый из которых имеет свои преимущества и недостатки. В любом случае созданное покрытие прослужит долго, если не подвергать его механическим воздействиям и правильно подобрать толщину защитного слоя с учетом специфики эксплуатации изделий.

Этот способ цинкования является одним из самых эффективных. После проведения такой обработки можно создать надежное покрытие, которое длительное время сохраняется на поверхности металлических изделий. Недостатком горячего метода является его вредность для окружающей среды.
Для выполнения данной обработки необходимо придерживаться следующей технологии:
Этот способ цинкования не подходит для обработки деталей большой площади и требует некоторой подготовки, поиска подходящей тары.
Этот метод обработки заключается в покраске металлических изделий специальными смесями. В их состав входит цинк, что позволяет в кратчайшие сроки создать на поверхности надежное покрытие. Наносится эта краска обычным способом – валиком, кистью, краскопультом. Этот метод обработки идеально подходит для деталей, которые не могут быть покрыты обычным горячим цинкованием.

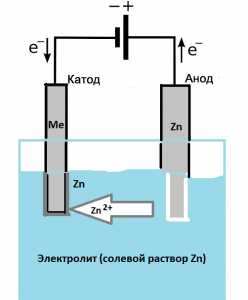
Схема цинкования
Такая внутренняя гальванизация осуществляется путем электрохимического воздействия на металл. При его выполнении на поверхности металла образуется тонкий защитный слой, который эффективно защищает металл от внешних негативных воздействий.
Для обработки продукт помещается в специальную емкость, содержащую цинковую пластину. Затем проводится электричество.Именно он переносит частицы цинка с пластин на поверхность обрабатываемых изделий.
Основным недостатком этого метода является его высокая стоимость. Также в процессе обработки металла остаются опасные яды, требующие специальной утилизации.
При выполнении термодиффузионного цинкования создается среда, характеризующаяся наличием высоких температурных показателей. При температуре около +2600°С цинк распадается на мелкие частицы, которые оседают на поверхности металлических изделий.Основное преимущество этого метода цинкования заключается в том, что он создает особенно толстый защитный слой.
Процесс нанесения защитного покрытия на металлические изделия происходит в специальной камере закрытого типа. Сначала на поверхность детали наносится порошок цинка, после чего она нагревается. Эта технология используется только в промышленных условиях. Использовать его в домашних условиях очень сложно, дорого и опасно.
Преимуществом термодиффузионного цинкования является его безопасность для окружающей среды.Полученное покрытие имеет значительную толщину, что обеспечивает отличные защитные свойства.
Цинк наносится интенсивным газовым потоком. После такой обработки поверхность следует покрасить. Несмотря на специфику данной технологии, она обеспечивает высокое качество и долгий срок службы обрабатываемых деталей.

, можно получить блестящие медные покрытия, превосходящие по качеству получаемые в сульфатной ванне.
Упомянутая ванна готовится путем растворения сульфата меди в воде, затем добавления аммиака для образования комплекса амина с медью и, наконец, винной кислоты для получения слегка кислого рН раствора.
Как и при меднении в сульфатной ванне, изделия не должны находиться длительное время в указанной ванне, а когда меднение полностью покроет их, их следует немедленно вынуть и промыть.
Рассматриваемая ванна также может быть использована для мелкосерийных изделий.Для этого чистые (без смолы) опилки пропитывают этим раствором и перерабатывают вместе со стальными предметами в деревянном барабане. Процесс проводят в течение 30 минут при медленном вращении барабана. Затем вставленные предметы отделяют от опилок на сите, промывают и сушат. Омедненные предметы блестят, так как при такой обработке покрытие наносится и полируется одновременно.
******************************************************* *****
Несколько более толстые медные покрытия можно получить в эдетатной ванне следующего состава:
медный купорос 37,5 г/дм3,
натрия эдетат2 87,5 г/дм3.
Обезжиренные, протравленные и активированные стальные предметы погружают в эту ванну на 1-10 минут при интенсивном перемешивании. Температуру ванны можно поддерживать в широких пределах, от 20 до 50°С.
Процесс меднения в ваннах данного состава может осуществляться также путем протирания поверхности изделий тампоном, смоченным в ванне.
Процессы описаны в Руководстве по гальванике.
В промышленных условиях сталь обычно омедняют в ваннах с щелочным цианидом.
Полученные таким образом слои меди могут быть покрыты даже слоем в несколько миллиметров в кислотных ваннах
Основной задачей меднения в домашних условиях или другого меднения является подготовка поверхности металла к дальнейшей обработке. Этой операции могут подвергаться различные металлы, но не металлы, среди которых следует отметить: сталь
,Благодаря своим многочисленным достоинствам этот металл стал распространенным.Сегодня медь и ее многочисленные сплавы широко используются в промышленности. Металл находит применение в авиастроении, автомобилестроении, приборостроении и других отраслях промышленности. Металл и изделия из металла не менее популярны в бытовой сфере. Меднение само по себе является одним из лучших методов тонкого покрытия металла. В домашних условиях меднение можно выполнить несколькими способами.
Для этого вам понадобится:
Внутренняя гальваническая медь

Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора к соляной кислоте.После того, как раствор медного купороса приготовлен, его необходимо тщательно перемешать, чтобы не было частиц. Затем к этому раствору тонкой струйкой следует добавить соляную кислоту. Не забывайте соблюдать меры предосторожности и использовать перчатки и очки. После добавления в раствор соляной кислоты тщательно перемешайте.
Итак, раствор готов и можно приступать к омеднению дома. Для этого нужно взять металлическую деталь, на которую вы будете наносить медный слой и подготовить ее к работе.Подготовка включает измельчение. Эта процедура позволяет не только очистить металлическую поверхность, но и обезжирить ее. Та же процедура применима к латунным или свинцовым деталям. Затем покрытие следует тщательно промыть в растворе кальцинированной соды. Это позволит более тщательно обезжирить материал.

Кальцинированная сода для обезжиривания материала
Затем поверхность погружают в раствор медного купороса и соляной кислоты. Следует отметить, что первый медный слой очень тонкий и непрочный, поэтому его желательно удалить металлической щеткой.После этой операции стальную или свинцовую поверхность следует еще раз промыть раствором кальцинированной соды и повторно погрузить в раствор меднения. Эти манипуляции приведут к тому, что слой меди в доме на поверхности будет гораздо толще и намного прочнее, так как удалить его с предмета можно будет только наждачной бумагой, а не металлической щеткой, как в прошлый раз.
Этот метод позволяет получить очень качественное медное покрытие, которое можно удалить только наждачной бумагой.Для улучшения медного покрытия в домашних условиях деталь необходимо повторно погрузить в раствор. Этот метод отличается простотой и высокой эффективностью, в том числе и в случае свинцовых изделий.
Омеднение обычно называют методом меднения, толщина медного слоя в таких случаях может быть от 300 мкм и более. Меднение стали является одним из важнейших процессов в гальванике, так как применяется как дополнительный процесс перед напылением других металлов для хромирования, никелирования, серебрения.
Медный слой отлично сцепляется со сталью и способен сглаживать различные дефекты поверхности.
 Медные покрытия характеризуются высокой адгезией к другим поверхностям, свинцовым изделиям, особенно металлу, а также высокой электропроводностью и пластичностью. Последнее нанесенное покрытие — ярко-розовый матовый или глянцевый цвет. Под влиянием атмосферных воздействий медные покрытия могут окисляться и покрываться оксидами с различными радужными пятнами.
Медные покрытия характеризуются высокой адгезией к другим поверхностям, свинцовым изделиям, особенно металлу, а также высокой электропроводностью и пластичностью. Последнее нанесенное покрытие — ярко-розовый матовый или глянцевый цвет. Под влиянием атмосферных воздействий медные покрытия могут окисляться и покрываться оксидами с различными радужными пятнами.
 Обычно может использоваться гальваническое меднение:
Обычно может использоваться гальваническое меднение:
Меднение происходит вместе с другими гальваническими покрытиями
Первый способ заключается в обработке металлического изделия наждачной бумагой, щеткой и ополаскивании водой. Затем обезжиривание в горячем содовом растворе с многократным полосканием. Затем в стеклянную емкость на медных проволоках опускают две медные пластины-аноды. Деталь подвешивается между пластинами на проводе, после чего включается ток.
Второй метод предназначен для изделий из стали, алюминия и цинка.
Данная процедура применима в различных случаях, так как медное покрытие может быть нанесено на алюминиевые столовые приборы, сувениры, подсвечники и т.д.Изделия не из металла со слоем меди дают неповторимый эффект. Это могут быть стебли растений, листья и т. д. Из-за отсутствия у покрываемых объектов токопроводящего слоя вместо него используется специальный электропроводящий лак, который наносится на поверхность.
Лак содержит ряд органических растворителей, пенообразователи и мелкодисперсный графитовый порошок, благодаря чему создается электропроводность. Лак наносится тонким слоем на сухую поверхность, и после высыхания через час можно приступать к медению.При желании меди можно придать различные оттенки цвета с помощью специальных методов. Высокое качество и уникальность таких изделий заслуженно приравниваются к настоящим ювелирным украшениям.
Меднение — это процесс гальванического покрытия медью различных поверхностей. Медный слой имеет прочную адгезию к металлам, сглаживает каверны на покрытой поверхности, обладает высокой электропроводностью и пригоден для дальнейшей обработки. Меднение может применяться как самостоятельный процесс или в составе более сложных процессов (серебрение, никелирование, хромирование).Наряду с промышленным методом практикуется меднение в домашних условиях, что позволяет решить многие бытовые проблемы. Помимо высоких технических параметров, это покрытие прекрасно выглядит, что определяет его использование в различных дизайнерских решениях.
В промышленных условиях меднение происходит в мощных гальванических ваннах, оборудованных автоматикой и другими специальными устройствами. Однако этот процесс также доступен внутри компании, что устраняет необходимость в сложном химическом оборудовании.
Последовательность технологических операций следующая:
1. С поверхности металла удаляется оксидная пленка. Используемая наждачная бумага, щетка, полировальная паста;
2. Обезжирить окрашенный предмет содовым раствором и тщательно промыть водой;
3. Две медные пластины (аноды) погружены в стеклянную емкость на медной проволоке, часть подвешена между ними;

4. Аноды подключаются к «плюсу» источника постоянного тока, а медная часть к «минусу»;
5.В электрическую цепь последовательно включены токорегулирующий реостат и амперметр. В качестве источника постоянного тока можно использовать автомобильный аккумулятор или адаптер питания;
6. Электролит заливают в емкость так, чтобы полностью покрыть поверхность анодов. Эту операцию необходимо выполнять с особой осторожностью, не допуская попадания агрессивных жидкостей на открытые участки кузова!
7. Плотность тока устанавливалась 2А на дм2 обрабатываемой поверхности, температура электролита: 20-26 градусов, время обработки: 20-25 минут;

8.Медная часть вынимается из контейнера, и процесс завершается. Толщина медного слоя может быть увеличена за счет увеличения времени пребывания деталей в гальванической ванне.

Состав электролитов несложный: кислота серная - 40 г, медный купорос - 190 г, вода - 980 г.
Несколько советов по меднению:
медный купорос 
Иногда требуется заменить сломанную медную мебельную фурнитуру, а в продаже есть только никелированные изделия.В этом случае установка для напыления меди собирается легко. Необходимое оборудование и материалы: блок питания 12 В/3 А, серная кислота и медный купорос.
Сначала необходимо удалить никелированное покрытие. Для этого деталь удерживается парой пинцетов, которые подаются «вниз» от блока питания. С прикрепленной тканью
Положительный электрод, смоченный 5% серной кислотой, протирает поверхность изделия.
При удалении никелирования образуются ядовитые пары, от которых следует защищать органы дыхания.Желательно использовать специальные очки и респиратор с угольным фильтром. Очищенная поверхность полируется.
Следующим шагом будет установка простейшей гальванической установки. В банку помещают медный электрод, подключаемый к «плюсу» источника питания, а заготовку – к «минусу».
Заливают электролит, состоящий из медного купороса, воды и 5% серной кислоты в соотношении 1/5/3 и подают электричество. Готовые изделия полируются до приятного блеска.

Существует множество различных применений внутреннего меднения. Медь можно использовать для алюминиевых столовых приборов, дав им вторую жизнь, для рыболовных приманок, подсвечников и многого другого. Особенно эффектны работы, при которых декоративное покрытие наносится на неметаллические предметы: стебли растений, листья, желуди и даже засушенных насекомых. Натуральная фактура исходного материала в сочетании с красотой гальванического покрытия создают неповторимый художественный эффект.
Технология изготовления таких изделий немного сложнее, но вполне реальна в домашних условиях. В покрытом материале нет токопроводящего слоя, поэтому вместо него на поверхность наносится специальный токопроводящий лак. В состав лака входят органические растворители, пленкообразующие вещества и мелкодисперсный графитовый порошок, обеспечивающий электропроводность.
Лак наносится тонким слоем на сухое растение, высыхает, и через час все готово к меднению.После гальванического покрытия внешний вид изделия может быть дополнительно улучшен. Существует несколько способов придания гальваническим покрытиям меди различных оттенков, включая патинирование, химическое окрашивание и окисление.
Качество графики, полученной с применением этих технологий, на уровне настоящих ювелирных украшений.
Уважаемые читатели, комментируйте статью, задавайте вопросы, подписывайтесь на новые публикации - нам интересно ваше мнение :)
Медь – один из древних металлов: люди начали использовать его для изготовления инструментов еще в 4 тысячелетии до н.э.CE Столь широкое распространение меди объясняется тем, что в природе это вещество встречается в самородном металлическом состоянии. И сегодня медь используется повсеместно — в металлургии, автомобилестроении, электротехнике и строительстве.
Металлическая медь — тяжелый розово-красный металл, ковкий и мягкий, плавится при температуре выше 1080 градусов Цельсия, очень хорошо проводит тепло и электричество: электропроводность меди в 1,7 раза больше, чем у алюминия, и в 6 раз больше, чем у алюминия. железа и лишь немного уступает по электропроводности серебру.
Специфические свойства меди определяются содержанием в металле тех или иных примесей, количество которых может варьироваться примерно от 10 до 50 раз. По содержанию кислорода принято использовать следующую классификацию меди:
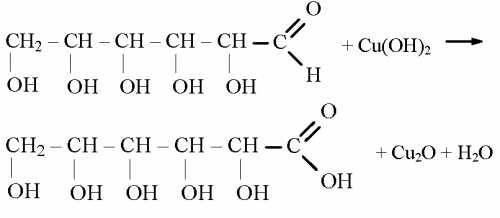
Помимо кислорода, медь может содержать водород, который переходит в металл при электролизе или отжиге в атмосфере, содержащей водяной пар. При высоких температурах водяной пар разлагается с образованием водорода, который легко диффундирует в медь.
Атомы водорода в бескислородной меди расположены в щелях решетки и особо не влияют на свойства металла. В кислородсодержащей меди водород способен взаимодействовать при высоких температурах с оксидом меди, при этом в объеме меди образуются водяные пары, присущие высокому давлению, что приводит к набуханию, растрескиванию и растрескиванию.Это явление называется «водородной болезнью».
Железо, висмут, сурьма и свинец ухудшают пластичность меди. Плохо растворимые в меди примеси (свинец, кислород, сера, висмут) вызывают хрупкость при высоких температурах, что затрудняет процесс горячей обработки.
Основным свойством меди, определяемым ее применением, является ее высокая электропроводность или низкое удельное электрическое сопротивление. Такие примеси, как железо, фосфор, мышьяк, олово и сурьма, значительно ухудшают его электропроводность.Механическое состояние меди оказывает большое влияние на величину электропроводности.
Еще одним важным свойством меди является ее высокая теплопроводность. Легирующие добавки и свойства снижают теплопроводность меди, поэтому медные сплавы на основе самой меди значительно уступают по этому показателю.
Медь устойчива к коррозии при нормальных температурах в таких средах, как пресная вода, сухой воздух, морская вода с низкой скоростью течения, неокисляющие кислоты и растворы солей без доступа кислорода, сухие галогенные газы, щелочные растворы, кроме аммиака и солей аммония, кислоты органические , фенольные смолы и спирты.

Медь не устойчива в аммиаке, хлориде аммония, окисляющих минеральных кислотах и растворах кислых солей. Его коррозионные свойства также значительно ухудшаются в некоторых средах по мере увеличения количества загрязняющих веществ. Допускается контакт меди с ее сплавами, оловом, свинцом во влажной атмосфере, морской и пресной воде. В то же время контакт меди с цинком и алюминием недопустим из-за их быстрого износа.
Медь, ее сплавы и соединения широко применяются в различных отраслях промышленности. Медь в электротехнике используется в чистом виде для производства контактных и неизолированных шин, кабельной продукции, электрогенераторов, телефонной и радиоаппаратуры. Вакуумные аппараты, теплообменники и трубопроводы изготовлены из меди.
Сплавы меди с различными металлами применяются в автомобилестроении и для производства химического оборудования.Красная медная проволока для изготовления всевозможных линий и гибки самых сложных элементов. Высокие свойства меди делают ее незаменимой для производства деликатных деталей.
Меднение – это процедура меднения с толщиной слоя от 1 до 300 микрон и более. Меднение стали — один из важнейших процессов в гальванотехнике, который применяется как предварительный процесс при подготовке поверхности металла к покрытию другими металлами — при хромировании, никелировании и серебрении, а также как вполне самостоятельный процесс.
Применение меднения в качестве подготовительной манипуляции обусловлено тем, что металл может очень плотно сцепляться со сталью, устраняя поверхностные дефекты. Другие материалы хорошо осаждаются на меди, но не очень хорошо на чистой стали.
90 230
Медные покрытияхарактеризуются высокой адгезией к различным металлам, высокой электропроводностью и пластичностью. Они обычно используются на стальных, цинковых и алюминиевых деталях.
Свеженанесенное медное покрытие имеет светло-розовый матовый или глянцевый цвет в зависимости от технологии нанесения.Атмосферные медные покрытия легко окисляются и покрываются слоем оксидов, образуя разводы различных оттенков и радужные разводы.
В большинстве случаев используется гальваническое меднение:

Меднение используется в сочетании с другими гальваническими покрытиями:
Процедура меднения своими руками доступна даже новичкам. Для этого нужно всего лишь знать его основные тонкости. В домашних условиях существует два метода меднения: с погружением в электролит и без погружения.
Металлическое изделие обрабатывают наждачной бумагой для удаления оксидного слоя, затирают щеткой, тщательно промывают водой, обезжиривают в горячем растворе соды и снова промывают.Затем две медные пластины, являющиеся анодами, принято опускать в стакан или банку на медных проволоках.
Деталь, подвешенная между пластинами на проволоке. Провода, выходящие из медных пластин, соединяются между собой и подключаются к плюсу источника питания, а некоторые к минусу. Далее в цепи есть реостат, регулирующий ток и миллиамперметр. Необходим источник постоянного тока напряжением не более 6В.

Для домашнего меднения приготовьте следующий раствор электролита.Возьмите 20 граммов медного купороса и 2-3 миллилитра серной кислоты на 100 миллилитров воды и вылейте в миску. Убедитесь, что этот раствор полностью покрывает электроды.
При использовании реостата задайте ток в диапазоне 10 - 15 мА на каждый квадратный сантиметр площади детали. Примерно через 20 минут отключите электричество и снимите уже покрытое тонким слоем меди изделие. Чем дольше длится процесс, тем толще будет слой меди.
Эта процедура выполняется для стали, алюминия и цинка.С одного конца скрученного провода снимается изоляция, а затем тонкие медные провода необходимо разорвать, чтобы получилась медная щетка. Для удобства работы его необходимо привязать к медной щетке или деревянной палочке, а другой конец кабеля подключить к плюсу источника питания.
Затем нужно приготовить электролит - раствор медного купороса, желательно слегка подкисленный, и залить его в широкую бутыль, в которую будет удобно макать кисть. Подготовьте кусок металла или другой небольшой плоский предмет.Его следует затереть мелкой наждачной шкуркой и обезжирить кипячением в растворе стиральной соды.

Затем поместите планшет в кювету или ванну и подключите его кабелем к минусу источника питания. После того, как схема собрана, достаточно залить электролит. Опустите «кисть» в раствор медного купороса, которую следует провести по длине пластины, не касаясь поверхности.
Рекомендуется работать таким образом, чтобы между щеткой и пластиной всегда был слой электролита.Проводка в рабочем состоянии должна быть пропитана раствором. Пластинка на глазах будет покрыта слоем красной металлической меди. Обработка маленькой детали займет несколько минут.
После нанесения покрытия высушите деталь на воздухе и натрите матовый медный слой до блеска тряпкой или шерстяной тряпкой. Процесс меднения алюминия, при котором изделие не погружается в ванну с электролитом, а обрабатывается снаружи на небольших поверхностях с добавлением электролита, используется в тех случаях, когда изделие настолько велико, что невозможно найти подходящую ванну.
Меднение ничем не отличается от обычных гальванических ванн. Электролиты для меднения довольно легко получить, если у вас есть под рукой нужные ингредиенты. Существует два типа растворов меди: щелочные и кислые.
В кислых растворах нельзя получить хорошо сцепляющиеся медные покрытия на изделиях из цинка и стали, так как в этом случае цинк и железо растворяются вместе с медью и нарушается адгезия к защитному покрытию.
Для устранения этой особенности рекомендуется первый тонкий слой меди (2-3 мкм) наносить в щелочном растворе меднения, а в дальнейшем наращивать покрытие до определенной толщины в кислом электролите, что более экономичный. Цинковые изделия сложной формы лучше всего смешивать в щелочных электролитах.

Наиболее распространенными кислотными электролитами являются фтороводород и сульфат. Наибольшее распространение получили сернокислотные электролиты, отличающиеся простым составом, высоким выходом по току и значительной стабильностью.
Перед омеднением стальных деталей в кислых электролитах рекомендуется предварительно омеднить их в цианидном электролите или нанести тонкий подслой никеля. Эти электролиты имеют ряд недостатков.
Одним из них является невозможность прямого покрытия цинковых и стальных деталей из-за контактного выделения меди, имеющей плохую адгезию к основному металлу. Кроме того, электролиты имеют низкую рассеивающую способность и более толстую структуру отложений по сравнению с другими электролитами.
Среди щелочных электролитов меднения известны пирофосфатные и цианидные электролиты.
Цианидные электролиты на основе меди характеризуются высокими диспергирующими свойствами, возможностью меднения столярных изделий и мелкокристаллической структурой отложений.
К недостаткам щелочных электролитов относятся низкая плотность тока и нестабильность раствора из-за карбонизации свободного цианида углекислым газом. Кроме того, цианидные электролиты отличаются пониженным выходом по току - не более 60-70%.
Таким образом, медь – это металл, который применяется повсеместно: в автомобилестроении, электротехнике и строительстве. А в гальванике известна технология меднения для подготовки металлических поверхностей к покрытию другими металлами или как самостоятельный процесс.
Изготавливаются многими мастерами в первую очередь для подготовки поверхности металла к последующей обработке различными защитными слоями.
Эта операция может применяться к поверхности самых разных металлов и неметаллов, включая сталь, латунь, никель и т.д.
Человечество уже много тысячелетий использует медь в своих целях, и в основном это связано с тем, что этот металл находится в естественном состоянии в природе и обладает рядом уникальных свойств.
Сегодня медь и различные сплавы на ее основе востребованы во многих отраслях промышленности.
Без него не обходятся авиационная, автомобилестроительная, приборостроительная и многие другие отрасли промышленности.
Медь и ее многочисленные сплавы довольно распространены в быту.
Следует также отметить, что различные комбинации добавок меди могут эффективно защищать поверхности многих металлов, таких как сталь, латунь или никель, от различных агрессивных сред.
Одним из наиболее распространенных методов утончения металлической поверхности является нанесение меди.
Химическое меднение в основном выполняется в домашних условиях, и существует несколько различных методов, каждый из которых имеет свои преимущества и недостатки.
Один из способов меди в домашних условиях показан на видео ниже.
Как упоминалось выше, медь обычно встречается в природе в виде небольших самородков.
Это уникальное вещество представляет собой достаточно тяжелый металл, который выглядит как самородок с легким розово-красным оттенком.
Этот металл обладает относительной мягкостью и высокой пластичностью, кроме того, он имеет температуру плавления порядка тысячи сотен градусов по Цельсию.
Прекрасно проводит не только тепло, но и электрический ток, что объясняет повышенный спрос на этот металл в электротехнике и приборостроении.
В большинстве случаев в природе медь находится не в чистом виде, а с различными примесями.
Все виды натуральных добавок, в зависимости от различных факторов в металле, могут варьироваться и варьироваться примерно в десять-пятьдесят раз.
Для этого металла большое значение имеет содержание кислорода, и в зависимости от количества этого элемента в составе меди разработана определенная классификация.
Таким образом, медь может быть бескислородной и рафинированной.
Кроме того, в его составе есть и медь с повышенным содержанием кислорода, а также общего назначения, когда содержание кислорода максимально.
Кроме этого элемента в металле может содержаться и водород, который поступает туда путем электролиза или отжига.
Медь имеет специфическую решетку, а атомы водорода занимают свое место в изломах, а значит, практически не влияют на ее свойства.
Если медь в своем составе содержит кислород в определенном количестве, то водород стремится определенным образом взаимодействовать, но только при достаточно высоких температурах с оксидом меди, и в данном конкретном случае начинает образовываться водяной пар, обладающий достаточно высокой индикаторы давления.
Как правило, это оказывает негативное воздействие на металл и в некоторых случаях может привести к образованию пузырей, а также к трещинам и разрывам.
Этот негативный эффект в химии называется водородной болезнью.
Присутствие железа и сурьмы может повлиять на ухудшение показателей пластичности меди.
Примеси, относящиеся к группе малорастворимых, снижают хрупкость этого металла, но только при достаточно высоких внешних температурах, что делает процесс обработки горячим давлением для меди крайне нежелательным.
На видео выше показано химическое меднение этого металла.
Для выполнения меднения на поверхности стали, никеля или некоторых других металлов применяют гальванику, при которой формируют тонкий слой меди.
Гальваническое меднение представляет собой довольно сложное химическое меднение, влияющее на состав материала.
Гальваническое покрытие представляет собой предварительный процесс перед нанесением другой защитной композиции на поверхность из никеля или другого металла.
Гальваническое покрытие свинца и других материалов обычно выполняется перед хромированием, никелированием и т.д.
В этом случае медь действует как своего рода припой или, другими словами, дополнительная добавка.
Как самостоятельно выполнить гальванику показано на видео ниже.
Медь, нанесенная таким образом в виде припоя на поверхность никеля или другого металла, способна достаточно крепко держаться, а также способствует устранению некоторых дефектов.
Многие другие материалы достаточно хорошо осаждаются в виде припоя на обработанной таким образом поверхности.
Такие медные покрытия, как припои, практически не изменяют состава основного металла и отличаются высокой адгезией, хорошей электропроводностью и пластичностью.
Медь – вид отбеливателя припоя, который практически не изменяет первоначальный состав металла и действует как своеобразная добавка.
Основной способ нанесения этого металла (припоя) на поверхность никеля, стали и др.является гальваника, и в следующем видео рассказывается, как это сделать в домашних условиях.
Для выполнения меднения в домашних условиях не нужно иметь каких-либо специфических знаний, достаточно знать курс школьной химии.
Поверхности из меди или никеля не изменяют своего основного состава, так как действуют как припой.
Медь в бытовых условиях потребует достаточно примитивных материалов, которые можно приобрести в любом специализированном магазине.
Процедуру меднения можно проводить с погружением или без погружения в медные электролиты (раствор).
В обоих случаях заготовка должна быть должным образом подготовлена перед началом меднения.
Для этого проходится наждачной бумагой, тщательно затирается щеткой с металлической щетиной и промывается под проточной водой.
Кроме того, после обезжиривания объекта приступают к меднению, для чего используется горячий раствор на основе соды.
Между этими анодами помещается обрабатываемая деталь, которая соединяется с минусом, соответственно анод с плюсом источника постоянного тока.
Кроме того, в случае меднения в цепи должен быть реостат.
Затем для выполнения меднения в домашних условиях готовится специальный состав электролита, раствор с медным купоросом, серной кислотой и водой в определенных пропорциях.
После меднения сульфатное соединение отфильтровывают, заготовку тщательно промывают и сушат.
На следующем видео показан процесс меднения на предприятии.
Меднение алюминия, меднение стали или цинкование осуществляют методом без погружения в состав электролита.
В этом случае деталь также подготавливают к меднению путем тщательной механической обработки и промывки.
Ручка для удобства выполнена на проволоке, а один ее конец подключается к плюсу источника постоянного тока.
Затем для меднения готовят специальный электролит - раствор с добавлением медного купороса и заливают в емкость.
Затем раствор подключают к напряжению и с помощью кисточки начинают обрабатывать детали, таким образом нанося отбеливатель.
Вся заготовка (раствор) подвергается процессу меднения в течение нескольких минут.
После завершения меднения раствор удаляют, деталь тщательно промывают и сушат. На следующем видео показан процесс покрытия медью без погружения в электролит.
Практически любой металл можно подвергнуть меднению путем нанесения на его поверхность защитного покрытия в виде медного слоя.
Видео:
Гальванизация - раздел электрохимии, изучающий нанесение электролитов на поверхность металлического изделия. Метод гальваники – это процесс, при котором на изделие наносится металлическое покрытие для защиты его от коррозии или других внешних воздействий. Однако в последнее время большую популярность приобрела декоративная гальваника. И, несмотря на достаточно сложный технологический процесс, гальванику проводят в домашних условиях.
Этот процесс требует не только некоторых знаний по химии и физике, но и некоторого оборудования, которое вы можете сделать сами.
Для этого требуется:
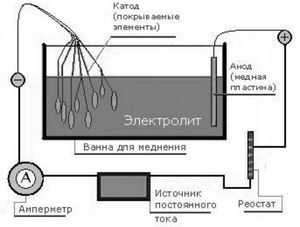 Характеристика и сложность Хромирование, меднение, серебрение или другое покрытие состоит из многоэтапного процесса. На начальном этапе необходимо подготовить среду из вышеперечисленных материалов и приготовить электролит. Для его приготовления нужны химические реактивы, отмеренные в определенных пропорциях с точностью до грамма. Конечно, для достижения такой высокой точности нужны специальные (желательно электронные) весы.
Характеристика и сложность Хромирование, меднение, серебрение или другое покрытие состоит из многоэтапного процесса. На начальном этапе необходимо подготовить среду из вышеперечисленных материалов и приготовить электролит. Для его приготовления нужны химические реактивы, отмеренные в определенных пропорциях с точностью до грамма. Конечно, для достижения такой высокой точности нужны специальные (желательно электронные) весы.
Затем можно переходить к следующему этапу: в емкость заливают подготовленный электролит, в него опускают аноды и подключают к «+», а между ними помещают изделие, которое подключают к «-», так цепь замыкается и выделяющийся металл в электролите осаждается на поверхности изделий.
 Перед нанесением покрытия на изделие необходимо тщательно очистить поверхность изделия ... Это очень важно, так как от этого шага будет зависеть качество и долговечность покрытия. Для этого изделие проходит несколько этапов очистки: от обезжиривания до шлифовки и пескоструйной обработки. Для обезжиривания изделия можно использовать любое органическое вещество, например, ацетон, растворитель, бензин или спирт. Однако решение может отличаться в зависимости от материала изделия.
Перед нанесением покрытия на изделие необходимо тщательно очистить поверхность изделия ... Это очень важно, так как от этого шага будет зависеть качество и долговечность покрытия. Для этого изделие проходит несколько этапов очистки: от обезжиривания до шлифовки и пескоструйной обработки. Для обезжиривания изделия можно использовать любое органическое вещество, например, ацетон, растворитель, бензин или спирт. Однако решение может отличаться в зависимости от материала изделия.
В последнее время получили распространение гальванические ванны, для получения декоративного эффекта ванны из чугуна и стали стали покрывать медью и никелем.Поэтому для обезжиривания изделий из таких материалов применяют специальные горячие растворы едкого натра, жидкого стекла, оксидированные фосфорнокислым натрием или кальцинированной содой. Или, если изделие изготовлено из цветного металла, используйте раствор хозяйственного мыла. Благодаря этому изделие обезжиривают, полируют и шлифуют ... Затем погружают в емкость с электролитом и анодами, где на поверхность наносят покрытие.
В первую очередь следует помнить, что гальванопокрытие – очень опасный процесс, так как вещества, используемые для приготовления электролита, очень токсичны, а особенно при нагревании, которое необходимо, неправильное обращение с химическими веществами может вызвать сильные ожоги или заболевания органов дыхания. Поэтому специалисты рекомендуют не пренебрегать правилами безопасности:
90 478Меднение – это процесс нанесения на поверхность изделия проводящего слоя меди. Что такое меднение в домашних условиях? Как было сказано выше, гальваническое покрытие выполняется как в защитно-декоративных целях ... Омеднение можно просто отнести к другим. Изделия из черных металлов после меднения выглядят очень оригинально, и что немаловажно, защищают их от коррозии.Однако, по мнению специалистов, меднение изделий из чугуна может привести к летальному исходу, поэтому перед процессом изделия покрывают слоем никеля, а затем медью.
Для меднения используют электролит с медным купоросом и раствором серной кислоты и водой, подогретой до комнатной температуры (18-20 градусов). Перед меднением или никелированием каждое изделие проходит тщательную очистку, методы которой выбираются в зависимости от металла, из которого изготовлено изделие. Например, алюминиевые изделия необходимо предварительно очистить от оксидного слоя, этот процесс еще называют травлением, а затем их промывают в специальном растворе водных оксидов и серной кислоты.
делается для повышения долговечности и защиты от внешних воздействий, но не стоит забывать, что хромированные изделия выглядят эффектно. Особенно, если это диски крутых элитных авто или мотоциклетных запчастей. Итак, с точки зрения самого процесса, меднение или никелирование выполняется перед хромированием как более нейтральный и универсальный метод. Или изделие сначала никелируют, потом медят, и только потом начинается хромирование.
В качестве электролита используются такие вещества, как свинец, олово и сурьма в пропорциях: 85×11×4%. В отличие от меднения или никелирования, в процессе хромирования оттенок покрытия и цвет можно регулировать, они зависят от температуры и состава электролита. Например, для получения блестящего оттенка необходимо нагреть электролит до температуры 35-55 градусов, молочного оттенка – температура должна быть выше 55 градусов, матового оттенка – ниже 35 градусов.
А цвет может варьироваться от темно-синего, агатового, синего до черного.После покрытия изделие промывают в растворе соды и полируют специальными пастами.
Изделие перед серебрением, как и в первых двух случаях, сначала покрывается никелем. Электролит состоит из хлорида серебра, кальцинированной соды, цианистого железа и калия и дистиллированной воды. Температура электролита не должна превышать комнатной, а в качестве анода используются графитовые пластины.
.Медь имеет характерный красный цвет. Если будем считать, что металл тем благороднее, чем больше площадь ее сопротивление накладывается на площадь водостойкости, то медь можно рассматривать как Благородный металл.
Медь устойчива только в отсутствие вещества комплексообразователи, такие как цианид и аммиак. Они расширяют площади коррозия меди. В настоящее время считается, что медь имеет две области коррозии: в зависимости от характера раствора.В кислых и сильнощелочных растворах коррозия меди происходит только в присутствии окислителя. Нейтральные растворы или слабощелочные, содержащие окислители, ингибируют коррозию, за счет образования Оксиды Cu2O, CuO и Cu2O3. Повышенная температура делает поверхность медь покрывается оксидами. Однако образующиеся оксиды не защищают медь от дальнейшая коррозия, особенно в более агрессивных условиях. Характеристики гальванические медные покрытия зависят от условий осаждения.Самый большой Таким образом, влияние имеют тип и состав ванны, плотность тока и температура.
Процесс меднения используется для обеих целей технические, а также защитные и декоративные. Использование медного подслоя в для технических целей позволяет получить соответствующие свойства покрытия товары. В этом помогают некоторые свойства меди, например, пластичность или хорошая электропроводность.Поэтому техническое меднение используется для покрытие пластмасс и печатных плат. Он нашел его большим также используется в электротехнике, гальванопластике и промышленности печать.
Медный подслой в системе декоративно-защитного покрытия в первую очередь влияет на повышение коррозионной стойкости изделий. В противном случае улучшает внешний вид продукта. Его дополнительным преимуществом может быть снижение затрат гальваническая обработка.Надлежащий процесс меднения требует почти только растворимые медные аноды - электролитические, электролитически катаные и литые. Каждая ванна требует определенного тип анода.
В настоящее время в промышленности используются два типа ванн: цианиды и сульфаты.
Цианидные ванны очень популярны, хотя и требуют токсичные растворы, необходимость обезвреживания нечистот и что с этим делать идет, тоже дороговизна.Однако у цианидных ванн есть много преимуществ. Во-первых, медные покрытия можно наносить на многие основные материалы, например сплавы цинка, алюминия, меди, магния, никеля и свинца. Встроенный слой имеет отличную адгезию. Большая глубина ванны и охват Они прекрасно подходят для покрытия изделий сложной формы. Кроме того, цианидные ванны просты в эксплуатации. Однако нельзя забывать что выбор состава ванны зависит от предполагаемого использования покрытия, его толщины и условий работа или глянец.Среди цианидных ванн можно выделить: цианидные ванны для осаждения тонких слоев меди, ванн быстрого меднения, ванны меднения с глянцем. Для основных ингредиентов всех Типы цианидных ванн включают: цианид меди (I) и/или цианид калия. натрий. Цианид меди вводят растворением в цианидах. щелочной. Увеличение концентрации меди позволяет использовать больше плотность тока, что влияет на интенсификацию процесса.Точный состав и параметры для нанесения медных покрытий представлены в таблицах:
При проведении цианидных ванн необходимо заплатить внимание на загрязнение. Органические соединения представляют наибольшую опасность, высокие концентрации карбонатов, соединения хрома в шестой степени окисления, соединения цинк, свинец и нерастворимые твердые вещества Повторное использование цианидная ванна требует обслуживания.Способ, частота и сложность поддерживающие процедуры зависят в первую очередь от состава и типа ванны полученные покрытия. Чем лучше покрытия мы хотим, тем больше мы должны позаботьтесь о постоянстве состава ванны. Мелкозернистая, непористая и блестящая мы получим покрытия, если процесс будет проведен быстро и качественно. Обслуживание баня заключается в поддержании постоянства состава и чистоты бани. Для этого необходимо систематически обозначать основные компоненты, значения pH и их коррекция до необходимых значений.Дополнительные ингредиенты, в т.ч. осветляющие добавки маркируются в соответствии с нормами, предоставленными авторами ванны или по мере их износа в процессе эксплуатации.
Второй вид ванн – сульфатные ванны. Характеризуются они просты по составу, долговечны и просты в уходе. Их дополнительные Преимуществом является относительно низкая цена. К сожалению, сульфатные ванны тоже имеют дефекты. Во-первых, по сравнению с цианидными ваннами они меньше глубина.Кроме того, их нельзя использовать для прямого меднения. стали. Процессу должно предшествовать осаждение медного подслоя в ванне. цианидный или никелевый подслой. Исследования по улучшению ванн сернокислотное, в том числе прямое меднение стали, получение покрытий глянцевые или специфические свойства покрытий в зависимости от них использование не сработало. Поэтому в случае купания сульфат, микроразглаживание или блеск достигается за счет включения в ванна с дополнительными веществами.К сожалению, у него есть побочные эффекты. Использование отдельных добавок способствует улучшению определенных свойств, но способствует образованию высоких напряжений или хрупкости покрытия. Успех ванн для нанесения люминофорных покрытий поэтому зависит от строгого соблюдение параметров электролиза, хорошая фильтрация и частый осмотр аналитический. Состав сульфатных ванн для нанесения специальных покрытий технические свойства, поэтому существенно отличается от состава декоративные и защитные ванны.Для основных сульфатных ингредиентов ванны меднения включают: сульфат меди (II) и серную (VI) кислоту. Правильный ход сульфатных ванн зависит в первую очередь от плотности тока, температура и перемешивание ванны. Указанные параметры ванны влияют интенсификация процесса, а значит и конечного результата.
Сульфатная ванна также требует обслуживания и регенерации. Это особенно важно при подготовке ванны для меднения с глянцевый.Поэтому необходимо очистить ванну, добавив активированный уголь в количестве 3г/дм3. Через 24 часа ванну нужно процедить. Затем вы должны отметить содержание хлоридов и доведите его до концентрации, указанной в рецепте. потом баня должна работать с током 3А/дм3. Только после этих процедур отбеливающие вещества могут быть введены, в зависимости от рецептов компании.
Обратите внимание, что содержание ванны в чистоте особенно важно, когда более высокие плотности тока используются в одновременное перемешивание ванны.Метод ухода и регенерации ванн зависит от многих факторов. Для блестящих ванн меднения конечно, наиболее важными будут люминесцентные добавки. Их тип может варьироваться в зависимости от типа ванны, а значит, ухода и регенерации такая баня будет другой.
Дефектные медные покрытия можно удалить химическим или электрохим.Способ устранения дефектов зависит не только от их вида. Большой земля тоже имеет значение. Медное покрытие цветных металлов можно снять погружением в раствор полисульфидов при температуре 16-25°С. После для этой операции металл следует зачистить щеткой. Медь, покрывающая сталь, может быть удалена. анодно-электрохимический метод. Для этого требуется раствор, содержащий 40-50 г/дм3 NaCN и напряжение около 2В. Цинковые изделия можно чистить медного покрытия анодным растворением в 10% растворе Na2S, при напряжение 2 В.В таблицах приведены дефекты покрытий, причины их образования и методы удаления, отдельно для цианида, щелочи и кислый.
.После презентации техники перегородчатой эмали, подготовленной Самией Анной Бетли, сегодня мы представляем вам еще одну интересную технику, с помощью которой вы можете создавать эффектные украшения. Сегодняшний урок был подготовлен специально для Royal-Stone Агой Орловской - художницей, известной своими работами в серебре с использованием филиграни, а также использованием в работе других техник. Сегодня Ага познакомит вас с техникой гальванопластики меди, т.е.Способом удивительным образом воспроизвести форму и текстуру натуральных медных листьев, а также получить интересные медные формы и текстуры.
Сердечно приглашаем вас прочитать, посетить профиль Художника на Facebook и посмотреть ювелирный магазин , созданный Агой Орловской .
Примечание: В представленной методике используются опасные для здоровья и жизни препараты и химические вещества. Приступая к работе, будьте особенно осторожны, запаситесь и используйте соответствующие меры безопасности (проветриваемое помещение, защитная одежда), а также строго следуйте указаниям и рекомендациям производителей используемых препаратов.
Электроформование меди — одна из самых интересных техник, которую мы можем использовать в ювелирной работе. Начало гальванопластики относится к 1840-м годам, так что это относительно молодая ювелирная техника, почему? Потому что вам нужно электричество для гальванопластики. О чем это все? Предмет, который мы хотим покрыть медью, погружаем в специальный раствор, в этот раствор погружаем и медный электрод, прикладываем напряжение (к электроду и предмету) и… предмет покрывается медью в таинственном способ.Я имею в виду, не тайно, потому что это обычная физика. В этом посте я дам вам возможность получать удовольствие от лепки меди, делая осенние украшения, например, из желудей. и уходит.
Что на картинке?
Медь из электрода, соединенного с "+" - анодом - растворяется, отдает электроду два электрона и в виде положительно заряженных ионов (катионов) переходит в раствор к отрицательному электроду - катоду - который притягивает Это. Там ионы меди «забирают» два электрона и спокойно садятся на предмет, покрытый медью (наш катод). Чтобы обеспечить «прием» электронов медью, если мы хотим омеднить изолятор (камень, лист, семена), мы должны позволить заряду каким-то образом течь по этому изолятору, следовательно, например.красим токопроводящей краской (об этом в пункте II).
Может возникнуть вопрос, а для чего этот раствор, если медь идет с анода, воды, например, мало? Раствор играет вспомогательную роль, он как бы магистраль, по которой катионы могут течь.
Рекомендуется, чтобы ток, протекающий через раствор, был в пределах 2-10 А/дм2
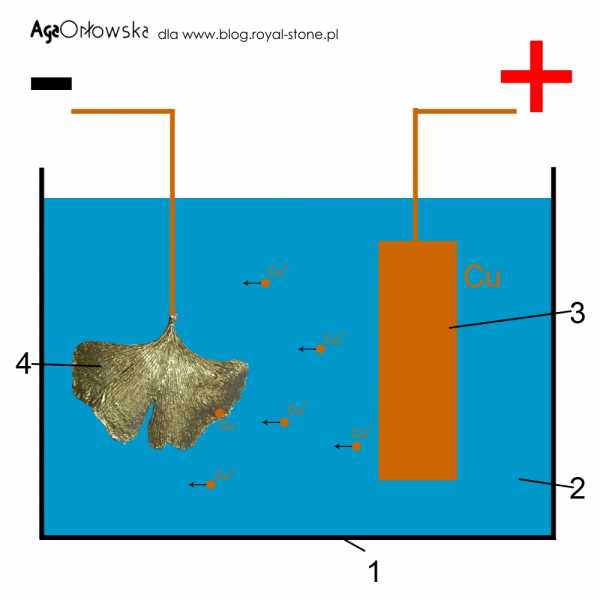
Чтобы начать играть с гальванопластикой, я рекомендую пойти двумя путями. Лучше всего во время прогулок собрать запас интересных листьев, желудей, семян, камешков и т.д.Высушите листья в книге и высушите семена, орехи и желуди. Отправляйтесь за покупками в одно и то же время.
Список покупок:
1) блок питания лабораторный - работающий в диапазоне 0-3А, 0-30В, с возможностью работы в режиме СС ( Постоянный ток - стабилизация выходного тока)
2) медный обмоточный провод диаметром примерно 1,5 - 1,6 мм - этот провод покрыт изоляционным слоем
3) запас медных проводов разного диаметра, рекомендую набор 0,9 мм, 1,2 мм, 2 мм, 3 мм - покупаем медные провода и снимаем изоляцию.
4) вода дистиллированная - желательно сразу 5 л
5) серная кислота 96% годовых
6) медный купорос в год
7) материал для медных электродов, рекомендую медные трубы для газовых установок - можно купить в строительных магазинах кусками по 2,5 м, можно конечно купить много медной проволоки диаметром 4 мм,
7) запас лабораторных перчаток
8) защитные очки
9) контейнер, в котором мы будем гальванизировать, я использую прозрачный прямоугольный пластиковый контейнер емкостью ок.2 л, некоторые предпочитают банки.
10) сода пищевая
11) супер клей (большая упаковка)
12) графитовый порошок
13) большой тюбик водной акриловой краски - рекомендую темную
14) чашки для лабораторной мочи
15) щетки бронзовые и стальные (колпачки для микрополировки)
16) оксид меди
17) Опциональный воск для обработки поверхности
18) опционально - осветлитель
19) бутылки для хранения раствора меди напр.после минеральной воды
20) пластиковые ложки 9000 3
Начнем с подготовки раствора для гальванопластики. Пропорции на 1 л дистиллированной воды.
Ингредиенты:
- 1 литр дистиллированной воды
- 240 г сульфата меди CuSO4
- 32 мл серной кислоты
- по желанию несколько капель отбеливателя (но я им не пользуюсь, т.к. люблю темные вещи)
Внимание! Все работы с кислотой проводим в защитном фартуке, очках и перчатках, также помним принцип, что кислоту всегда заливаем водой, работаем в проветриваемом помещении.Емкости, в которых замешивается раствор, должны быть либо стеклянными, либо химически стойкими из пластика.
Налейте воду в большой сосуд, затем осторожно влейте кислоту при перемешивании. Температура раствора может повыситься или он может начать «дымить», тогда при перемешивании добавляют медный купорос. Ждем, пока все растворится и выливаем в сосуд, в котором будем формировать медь. Остальное (если есть) влить в бутылку, подписать бутылку и хранить в прохладном и темном месте.
Время для электродов. Электрод, который «отдает» медь в раствор, называется анодом. Подключаем его к «+» на блоке питания. Ионы меди положительные, поэтому при подключении электрода к «+» они попадают в раствор. Следовательно, этот электрод должен быть твердым, поскольку со временем он начнет исчезать. Поэтому я использую медные газовые трубы, которые нарезаю по размеру, просверливаю и подсоединяю к обмоточному проводу без изоляции на концах. Благодаря этому у меня переваривается электрод, а не электродное соединение. Катод делаем из более толстой медной проволоки, на которую вешаем медные «крючки», подсоединяем обмоточный провод, а катод подключаем к «-» на блоке питания.

Следующим шагом будет изготовление токопроводящей краски. Вот чем нам пригодятся контейнеры для мочи ;-). Насыпьте в емкость пару столовых ложек порошкообразного графита (графит является проводником и обеспечит проводимость краски) и добавьте такое же количество акриловой краски. Тщательно перемешиваем. Добавьте столовую ложку дистиллированной воды и перемешайте, пока все не смешается. У нас должна получиться масса густотой сметаны. Рисуем, обмакивая кисть в дистиллированную воду и таким образом контролируем густоту краски: для листьев, желудей, семян она должна быть тоньше, а для камней – гуще.Рекомендую работать в перчатках, акриловую краску трудно смыть после высыхания, а графит сильно пачкается.

Медью покроем: сушеный лист гинкго, два желудя, горный хрусталь. Первым делом нужно приклеить медные держатели. Горный хрусталь получит глазки из плетеной медной проволоки, желуди – медные кольца, а листик – петельку.

Закрепите кристалл и желуди, например,в тисках. Сверху нанесите небольшое количество клея, наклейте на него медные круги и подождите, пока они склеятся. Следующим шагом будет усиление соединения (желуди) и изготовление медной основы на кристалле. Для этого покроем клей пищевой содой. Наносим новый слой клея на стык медь-желудь и сразу посыпаем пищевой содой. Тогда образуется очень твердая и крепкая масса. В случае с хрусталем покрываем клеем верх с приклеенной петелькой и сразу обсыпаем, затем покрываем боковые осколки.
90 132
Очень аккуратно приклейте петлю к листу гинкго (желательно слегка приплюсните молоточком), хвостиком вдоль черешка листа, когда клей высохнет, нанесите новый слой, разровняйте и посыпьте пищевой содой. Соединение должно затвердеть, поэтому делаем перерыв на 2-3 часа.

Теперь можно все покрыть электропроводящей краской. Мы будем использовать более плотный кристалл для кристалла и более тонкий лист и желудь для листа. В случае с кристаллом красим только клеево-натриевый слой + медь, в случае с желудями и листьями - целиком, т.к. покрываем объект целиком.Нарисуйте листочек на листе бумаги сначала с одной стороны, дождитесь высыхания, затем с другой. После покраски лучше всего оставить вещи на 12 часов, чтобы краска высохла.

Я рекомендую гальванопластику листьев и т. д. и камней отдельно. Дело в том, что в случае с листьями и т.п. ток должен быть ниже, чтобы ионы меди могли оседать на листьях, воссоздавая их структуру, в случае с камнями мы можем позволить себе более высокий ток, тогда медь растет более хаотично, создавая интересные формы.

Поместите лист и желуди в сосуд для гальванопластики. Если сосуд уже наполнен раствором, то, конечно, листья и желуди всплывут наверх и не будут погружены в раствор. Способ сделать это просто — погрузить их следует так глубоко, чтобы даже после того, как они всплывут, они оказались под поверхностью. Включаем ток - обычно ставлю 0,2 А и жду. Через час у нас должны получиться такие же эффекты, как на фото. Я обычно оставляю листья и т. д. в растворе примерно на 24 часа при слабом токе.

Конечно, может и будет наверное так, что листья/желуди будут омеднены не очень аккуратно. Не беспокойтесь об этом, просто выньте его из раствора, промойте в дистиллированной воде, тщательно высушите, покройте токопроводящей краской, дайте краске высохнуть и поместите обратно в раствор и формируйте медь при слабом токе.
Пока лист и желуди сохнут после второго покрытия, можно заняться кристаллом. Подвешиваем на крючок и опускаем в раствор.Начинаем с небольшого тока, т.е. 0,2А, когда содово-клеевые колпачки покрыты медью, можно увеличивать ток и выращивать удивительные медные структуры.

Когда мы успешно все покрыли медью и медь выросла как надо, пришло время окончательной обработки. Полировка стальными/бронзовыми щетками - на ваше усмотрение.. И опять же, в целях безопасности, рекомендую работать в очках, или, как я, специальной полировальной станцией (деревянный ящик с прозрачными стенками: сверху и спереди и отверстиями для рук в боковые стенки - дизайн и исполнение - мой муж).

После полировки можно оксидировать, покрыть патиной или оставить медь… медного цвета. Обычно я окисляю его, промываю, тщательно высушиваю, немного полирую, а затем покрываю небольшим количеством защитного воска.

Вот, пожалуй, и все. Что дальше? Я желаю вам много веселья. И внимание к одежде - мои майки и рабочие штаны стали ажурными, потому что я забыл про защитную одежду.


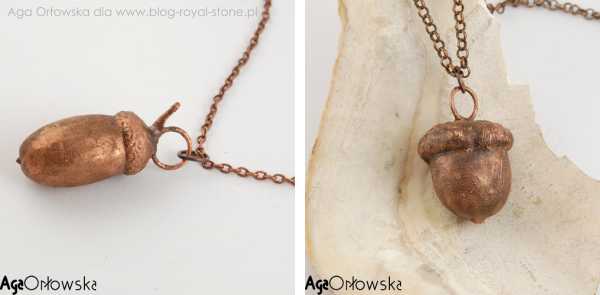
К металлам предъявляется ряд технических требований. Они должны быть пластичными, сохраняя при этом хорошую прочность, легко поддающимися обработке и относительно дешевыми. Для повышения их прочности изготавливают сплавы, которые часто ухудшают пластические свойства, а также тепло- и электропроводность. По этой причине многие дизайнеры покрывают металлы соответствующими покрытиями, позволяющими улучшить свойства металлических предметов.
Меднение металлических предметов называется меднением. Они используются в декоративных целях, в качестве основы для металлов, таких как цинк, или для придания объектам лучшей электрической, тепловой или коррозионной проводимости. Различают электролитическое и химическое меднение, которое заключается в купании в специальных растворах, таких как сульфат меди II или растворы меди. Меднение в кислотных ваннах позволяет получить толстое покрытие, защищающее от азотирования и науглероживания.Однако их нельзя использовать на стальных и железных предметах, поэтому их применяют косвенно, предварительно применив цианидную ванну. Люди, интересующиеся процессом меднения и другими видами обработки металлов, могут узнать больше на https://www.tegal.pl/.
Медь может быть подвергнута, в частности, сталь, железо, цинк или алюминий. Медное покрытие алюминия позволяет улучшить свойства тепло- и электропроводности и, прежде всего, повышает коррозионную стойкость.Однако повышение стойкости к электрохимической коррозии возможно только при сохранении в процессе сплошности и герметичности нанесенного покрытия. При появлении трещин во время меднения коррозия будет происходить быстрее. По этой причине важно правильно выполнить меднение.